
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
ЗАНЯТТЯ № 19
|
|
Тема: ЗАГАЛЬНІ ВЛАСТИВОСТІ МЕТАЛІВ
Мета заняття: вивчити хімічні властивості металів – відношення до води, кислот, лугів, солей. Пов’язати хімічну активність металів у водних розчинах з величинами їх стандартних електродних потенціалів.
ПИТАННЯ ДЛЯ ПІДГОТОВКИ
1. Розташування металів у періодичній системі.
2. Загальні фізичні властивості металів.
3. Основні хімічні властивості металів.
4. Загальні способи добування металів
5. Використання металів у техніці.
ТЕОРЕТИЧНІ ВІДОМОСТІ
Серед елементів періодичної системи переважаюча більшість – метали. Це s – метали (І, ІІ групи, головні підгрупи, крім Гідрогену і Гелію), d-, f – метали (побічні підгрупи всіх груп періодичної системи) та р – метали (лівий нижній кут р -елементів від діагоналі «бор-астат»).
Характерною особливістю електронної будови атомів металів є невелике число електронів на зовнішньому енергетичному рівні атомів. Тому вони легко втрачають ці електрони при хімічних реакціях, проявляючи тільки відновні властивості. Це визначальна особливість металів. Атом металу перетворюється при цьому в додатньо заряджений іон:
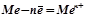 .
.
Відновна здатність металів при реакціях у водних розчинах визначається місцем металу в ряду напруг, де метали розташовані у порядку зростання їх стандартних електродних потенціалів (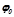 , В; додаток 4). Більш активним є той метал, стандартний потенціал якого менший. Стандартний потенціал системи
, В; додаток 4). Більш активним є той метал, стандартний потенціал якого менший. Стандартний потенціал системи  прийнято рівним нулю. Метал, який розміщений ближче до початку ряду напруг і має менше значення стандартного потенціалу, є активнішим від тих членів ряду, що стоять за ним, і може витісняти їх з водних розчинів солей:
прийнято рівним нулю. Метал, який розміщений ближче до початку ряду напруг і має менше значення стандартного потенціалу, є активнішим від тих членів ряду, що стоять за ним, і може витісняти їх з водних розчинів солей:
 ;
;
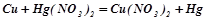 .
.
Потенціал витіснення водню з води (рН = 7) становить
–0, 41 В. Отже, водень з води можуть витісняти ті метали, потенціал яких менший, ніж –0, 41В. Це метали від початку ряду напруг до заліза включно (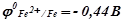 ). Наприклад:
). Наприклад:
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
 .
.
Проте, метали від алюмінію по хром (включно) захищаються щільною нерозчинною оксидною плівкою і реакція практично не йде.
У кислотах-неокисниках (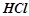 ,
,  (розбавлена),
(розбавлена),  ) окисником є іон
) окисником є іон 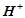 :
:
 ,
, 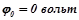 .
.
Тому метали, потенціал яких менший, ніж 0 вольт, можуть витіснити водень з цих кислот:
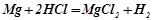 ;
;
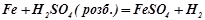 .
.
Виняток – свинець, який не витісняє водню з кислот через перенапругу виділення водню на свинці і через нерозчинність солей. Олово виділяє водень лише з концентрованої хлоридної кислоти:
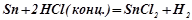 .
.
В оцтовій кислоті-неокиснику свинець розчиняється за рахунок окиснення його не іоном  кислоти, а киснем, що є у розчині, з подальшим утворенням розчинного оцтовокислого свинцю
кислоти, а киснем, що є у розчині, з подальшим утворенням розчинного оцтовокислого свинцю  . Водень при цьому не виділяється:
. Водень при цьому не виділяється:

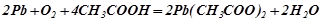
Кислоти-окисники:  (концентрована) та
(концентрована) та 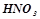 (будь-якої концентрації) окиснюють аніоном (
(будь-якої концентрації) окиснюють аніоном (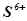 ,
,  ), тому при їх взаємодії з металами водень не виділяється. Такі кислоти розчиняють і ті метали, що стоять після водню в ряду напруг (
), тому при їх взаємодії з металами водень не виділяється. Такі кислоти розчиняють і ті метали, що стоять після водню в ряду напруг (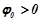 ). При цьому ступінь окиснення окисників
). При цьому ступінь окиснення окисників 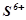 ,
,  змінюється тим сильніше, чим активніший метал, вища температура і менша концентрація кислоти.
змінюється тим сильніше, чим активніший метал, вища температура і менша концентрація кислоти.
Для сульфатної кислоти:
 |
Для нітратної кислоти:
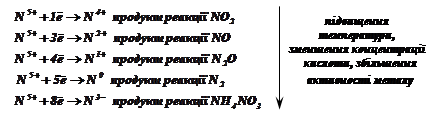 |
Наприклад:
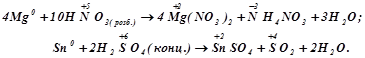
При високій концентрації сульфатної та нітратної кислот поверхня заліза, хрому пасивується і взаємодія без нагрівання практично не відбувається. Взаємодія металів з кислотами приведена в додатку 5.
Суміш нітратної і хлоридної кислот («царська горілка») окиснює всі метали, крім компактних осмію, родію та іридію:
 ;
;
 .
.
З лугами взаємодіють метали, що мають амфотерні оксиди і гідроксиди (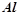 ,
,  ,
,  ,
,  ,
, 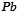 ). При цьому водень виділяється, якщо метал достатньо активний:
). При цьому водень виділяється, якщо метал достатньо активний:
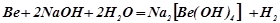 ;
;
натрій берилат
 .
.
натрій станнат
Якщо ж метал неактивний, то для його розчинення в розчині лугу необхідна присутність сильного окисника, водень при цьому не виділяється:
 .
.
|
|
|
