
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
ЗАНЯТТЯ № 22
|
|
Тема: ОСНОВНІ КЛАСИ ОРГАНІЧНИХ СПОЛУК
Мета заняття: засвоїти основні положення теоріїї хімічної будови О. Бутлерова. Вивчити основні класи органічних сполук: номенклатуру, функціональні групи, основні хімічні властивості. Звернути увагу на практичне застосування природних і синтезованих органічних речовин.
ПИТАННЯ ДЛЯ ПІДГОТОВКИ
1.Основні положення хімічної будови органіних сполук
О. Бутлерова.
2. Поняття про гомологічні ряди і гомологічну різницю.
3. Гомологічний ряд метану.
4. Які вуглеводні називаються ненасиченими?
5. Основні класи органічних сполук, функціональні групи, основні хімічні властивості.
ТЕОРЕТИЧНІ ВІДОМОСТІ
1. Теорія хімічної будови О. Бутлерова.
Органічна хімія – це хімія вуглеводнів – сполук Карбону і Гідрогену. Предметом органічної хімії є вивчення складу, будови, властивостей та різноманітних перетворень органічних речовин. Основою органічної хімії є теорія хімічної будови органічних сполук О.М. Бутлерова (1861 р.).
Основні положення
1. Атоми у молекулах сполучені один з одним у певній послідовності відповідно до їх валентності.
2. Хімічні та фізичні властивості речовин залежать не лише від кількісного і якісного складу, але й від порядку сполучення атомів у молекулі.
3. Атоми або групи атомів у молекулах взаємно впливають один на одного безпосередньо або через інші атоми.
4. Валентність Карбону у органічних сполуках (число можливих зв’язків) рівна чотирьом. Атом Карбону знаходиться у збудженому стані і має електронну конфігурацію  (чотири неспарених електрони).
(чотири неспарених електрони).
5. 
 Атоми Карбону здатні сполучатись один з одним, утворюючи карбонові ланцюги необмеженої довжини за рахунок одинарних
Атоми Карбону здатні сполучатись один з одним, утворюючи карбонові ланцюги необмеженої довжини за рахунок одинарних  , подвійних
, подвійних  або потрійних
або потрійних 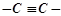 зв’язків. Ланцюги з атомів Карбону можуть бути відкритими, розгалуженими, замкнутими.
зв’язків. Ланцюги з атомів Карбону можуть бути відкритими, розгалуженими, замкнутими.
2. Класифікація та номенклатура органічних сполук
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Органічні сполуки утворюють гомологічні ряди. Гомологічним рядом називається послідовний ряд однотипних органічних сполук, коли кожна наступна відрізняється від попередньої на групу атомів 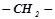 , яку називають гомологічною різницею.
, яку називають гомологічною різницею.
Склад будь якого члена гомологічного ряду можна знайти за допомогою загальних формул. Загальна формула гомологічного ряду насичених вуглеводнів – алканів –  (таблиця 7), ненасичених з одним подвійним зв’язком (етиленових) – алкенів –
(таблиця 7), ненасичених з одним подвійним зв’язком (етиленових) – алкенів –  (
( етен (етилен),
етен (етилен), 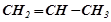 , пропен (пропілен)), ненасичених з двома подвійними зв’язками (дієнових) – алкадієнів –
, пропен (пропілен)), ненасичених з двома подвійними зв’язками (дієнових) – алкадієнів –  (
(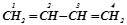 бутадієн-1, 3), ненасичених з одним потрійним зв’язком (ацетиленових) – алкінів –
бутадієн-1, 3), ненасичених з одним потрійним зв’язком (ацетиленових) – алкінів –  (
( етин (ацетилен),
етин (ацетилен),  пропін (метилацетилен)); загальна формула бензену і його похідних – аренів (ароматичних вуглеводнів)
пропін (метилацетилен)); загальна формула бензену і його похідних – аренів (ароматичних вуглеводнів) 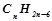 (n ≥ 6) (
(n ≥ 6) ( бензен (бензол)).
бензен (бензол)).
Вуглеводневими радикалами називають залишки, утворені послідовним відніманням від молекул вуглеводню атомів Гідрогену. Вони мають одну або кілька вільних валентностей. Нижче подані вуглеводні гомологічного ряду метану і відповідні їм радикали.
Таблиця 9
Гомологічний ряд метану
| Насичені вуглеводні - алкани СnH2n+2 | Одновалентні радикали |
| Метан СН4 | Метил СН3 — |
| Етан С2Н6 | Етил С2Н5 — |
| Пропан С3Н8 | Пропіл С3Н7 — |
| Бутан С4Н10 | Бутил С4Н9 — |
| Пентан С5Н12 | Аміл С5Н11 — |
| Гексан С6Н14 | Гексил С6Н13 — |
| Гептан С7Н16 | Гептил С7Н15 — |
| Октан С8Н18 | Октил С8Н17 — |
| Нонан С9Н20 | Нонил С9Н19 — |
| Декан С10Н22 | Децил С10Н21 — |
Номенклатура вуглеводнів
Назви органічних сполук утворюють згідно з правилами Міжнародного союзу чистої і прикладної хімії (ІЮПАК), які базуються, головним чином, на женевській номенклатурі.
1. Вибирають найдовший карбоновий ланцюг і нумерують атоми карбону з ближчого від розгалуження кінця.
2. Визначають бічні розгалуження і в алфавітному порядку називають їх, ставлячи перед ними цифру номера Карбону, при якому знаходиться даний радикал і називають головний ланцюг.
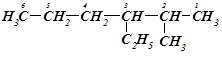 | |||||
| |||||
 |
3. При наявності кратного зв’язку нумерацію атомів Карбону починають від того кінця, до якого ближче кратний зв’язок. Остання цифра відповідає номеру атома Карбону, біля якого знаходиться кратний зв'язок:
 |
Хімічні властивості вуглеводнів
У хімічному відношенні насичені вуглеводні (алкани) за звичайних умов малоактивні. Для них характерні реакції:
- заміщення: 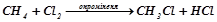 ;
;
- горіння:  (повне згоряння);
(повне згоряння);
 (неповне згоряння);
(неповне згоряння);
|
 (термічна дисоціація)
(термічна дисоціація)
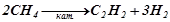 (каталітичний розпад)
(каталітичний розпад)
Ненасичені вуглеводні (алкени, алкіни, алкадієни) хімічно активніші, ніж алкани. Для них характерні реакції:
- приєднання:
 (галогенування);
(галогенування);
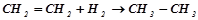 (гідрування);
(гідрування);
 (гідратація);
(гідратація);

- окиснення в розчині:
|
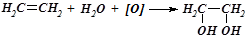
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
|

- горіння:
 (повне горіння);
(повне горіння);
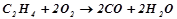 (неповне горіння);
(неповне горіння);
- полімеризації:
|
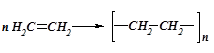
3. Похідні вуглеводнів
Якщо до складу вуглеводнів замість атома Гідрогену входять різні функціональні групи (замісники), то утворюються похідні вуглеводнів. Функціональні групи надають речовинам певних хімічних властивостей. Найпоширенішими є:
−  гідроксильна група спиртів і фенолів;
гідроксильна група спиртів і фенолів;
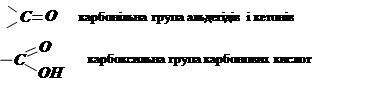 |
−  аміногрупа первинних амінів;
аміногрупа первинних амінів;
− 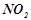 нітрогрупа нітросполук.
нітрогрупа нітросполук.
Спирти – похідні вуглеводнів, у молекулах яких один або декілька атомів Карбону заміщені на гідроксогрупу  :
:
- одноатомні спирти, закінчення -ол: метанол (метиловий спирт)  , етанол (етиловий спирт)
, етанол (етиловий спирт) 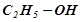 ;
;
- двоатомні спирти – гліколі: етиленгліколь  ;
;
- триатомні спирти: гліцерин 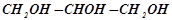 .
.
Альдегіди і кетони – похідні вуглеводнів, у молекулах яких атом Гідрогену заміщений на одну або кілька карбонільних груп  :
:
- альдегіди (закінчення -аль):
|
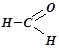

- кетони (закінчення -он):
|
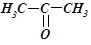
Карбонові кислоти – похідні вуглеводнів, у молекулах яких один або кілька атомів Гідрогену заміщені на карбоксильні групи 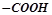 . Одноосновні органічні кислоти:
. Одноосновні органічні кислоти:


|
Двоосновні органічні кислоти  :
:

|
Карбонові кислоти у водних розчинах дисоціюють з утворенням іона 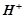 з карбоксильної групи:
з карбоксильної групи:
 .
.
Етери (прості ефіри) – похідні спиртів, у молекулі яких атом Гідрогену гідроксогрупи 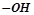 заміщений на карбоновий радикал
заміщений на карбоновий радикал 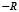 :
:
|


Естери (складні ефіри) – продукти заміщення атомів Гідрогену карбоксильної групи карбонових кислот на карбоновий радикал  :
:
|

Нітросполуки – похідні вуглеводнів, у молекулах яких один або кілька атомів Гідрогену заміщені на нітрогрупу 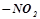 :
:
|
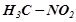

Аміни – похідні аміаку, у молекулах якого один або кілька атомів Гідрогену заміщені на вуглеводневі радикали, наприклад:
- первинний амін  (метиламін)
(метиламін)
- вторинний амін  (диетиламін)
(диетиламін)
Сполуки з кількома різними функціональними групами, зв’язаними з вуглеводневим радикалом R, називаються сполуками зі змішаними функціями:
|

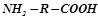
ЗАДАЧІ ТА ВПРАВИ
1. Написати структурні формули і назвати три приклади органічних сполук з різними функціональними групами.
2. Які вуглеводні називають алканами і яка їх загальна формула? Що таке ізомери? Написати формули всіх можливих ізомерів гексану і дати їм назви.
3. Які вуглеводні називають алкенами (олефінами)? Навести приклади трьох сполук і дати їм назви.
4. Написати реакції дисоціації оцтової кислоти у водному розчині, нейтралізації її гашеним вапном та етерифікації метиловим і пропіловим спиртами.
5. Які сполуки називають спиртами, а які – фенолами? Навести по два приклади цих сполук і дати їм назви. Що спільного в їх будові і яка різниця у властивостях?
6. Написати рівняння реакцій дегідратації етилового та пропілового спиртів.
7. Написати рівняння етирифікації етанолу.
8. Написати рівняння реакції одержання естеру етилацетату.
9. Який об’єм кисню потрібний для повного згоряння 20 л метану?
10. Скільки грамів водню потрібно для утворення 20 г етану гідрогенізацією етену (етилену)?
11. Яку масу пропену можна повністю прохлорувати з використанням 22, 4 л (н.у.) хлору?
ЛІТЕРАТУРА: [1 – c. 314-323; 2 – c. 454-475; 3 – с. 546-561].
|
|
