
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Практическая часть. В данной работе изучается влияние концентрации и температуры на скорость взаимодействия растворов серноватистокислого натрия (тиосульфата) и серной кислоты:
|
|
В данной работе изучается влияние концентрации и температуры на скорость взаимодействия растворов серноватистокислого натрия (тиосульфата) и серной кислоты:
Na2S2O3 + H2SO4 = S¯ + SO2 + H2O + Na2SO4.
Эта реакция сопровождается выделением коллоидной серы, что проявляется в помутнении раствора. В начале опыта под стакан с раствором H2SO4 подкладывается лист линованной бумаги. Линии четко просматриваются через прозрачный раствор. После добавления раствора Na2S2O3 раствор делается непрозрачным и линии на бумаге станут невидимы. Момент исчезновения из поля зрения линий на бумаге соответствует выделению определенного количества серы. Так как степень мутности зависит от толщины слоя раствора, то все опыты следует проводить в одном и том же стакане, чтобы толщина слоя была одной и той же во всех экспериментах.
Началом реакции будем считать момент смешения растворов, условным концом реакции - выделение одного и того же количества серы (когда становятся невидимы линии на подложенной под стакан бумаге). Время, необходимое для выделения данного количества серы, обратно пропорционально средней скорости реакции.
Опыт 1. Зависимость скорости реакции от температуры
Налейте в один стаканчик 20 мл 0, 5%-ного раствора серной кислоты, а в другой 20 мл 0, 5%-ного раствора серноватистокислого натрия Na2S2O3. Измерьте температуру растворов (каждый раз предварительно сполоснув термометр). Поставьте стаканчик с кислотой на лист линованной бумаги, быстро прилейте к нему раствор Na2S2O3, взболтайте и отметьте момент сливания растворов по секундной стрелке часов. Отметьте отрезок времени до условного окончания процесса. Запишите число секунд.
Повторите эксперимент, нагрев реагирующие растворы на 10 градусов выше температуры первого эксперимента. Для этого оба стаканчика с растворами поместите одновременно на горячую водяную баню. В одном из стаканчиков периодически измеряйте температуру (не оставляя термометр в стакане). По достижении требуемой температуры быстро смешайте растворы и отметьте по часам условную продолжительность реакции.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Повторите эксперимент, повысив температуру обоих растворов на 20 градусов выше первого эксперимента. Результаты запишите в табл. 1.
Таблица 1
| № | t, °С | V(H2SO4), мл | V(Na2S2O3), мл | Время реакции, с (n) | Скорость r =100/n * |
| t | |||||
| t+10 | |||||
| t+20 |
· Коэффициент пропорциональности 100 берем для удобства расчетов и построения графика.
Задания:
1. Постройте график зависимости скорости реакции r от температуры t.
2. По полученным данным рассчитайте температурный коэффициент Вант-Гоффа для данной реакции:
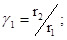
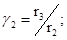
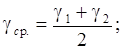
3. Оцените энергию активации реакции по уравнению:
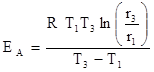 .
.
|
|
