
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Лабораторна робота 7
|
|
КАРБОНОВІ КИСЛОТИ ТА ЇХ ПОХІДНІ
Контрольні питання
1. Охарактеризуйте хімічні властивості оцтової кислоти і її похідних.
2. Наведіть способи одержання карбонових кислот.
3. Чим відрізняється мурашина кислота від усіх інших карбонових кислот насиченого ряду?
4. Що одержується при взаємодії мурашиної кислоти з сірчаною кислотою, аміачним розчином оксиду срібла, перманганатом калію? Напишіть рівняння реакцій.
5. Наведіть реакцію одержання вищих жирних кислот з природних жирів.
6. Поясніть поведінку мила в жорсткій воді.
7. Що відбувається на межі зіткнення води і спиртового розчину мила?
8. Розташуйте в ряд за активністю в реакціях ацилювання такі речовини: етилацетат, ацетонітрил, кетен, оцтовий ангідрид та ацетилхлорид. Чим пояснюється такий порядок зміни активності?
9. Чим пояснюється висока реакційна здатність ацетилхлориду?
10. Чому з лугами ангідрид оцтової кислоти реагує легше, ніж з водою?
11.Реакції щавлевої кислоти з сірчаною кислотою, перманганатом калію, розкладання при нагріванні.
Карбонові кислоти - органічні сполуки, що містять одну або більше карбоксильних груп –СООН, зв'язаних з вуглеводневим радикалом.
Карбоксильна група об’єднує у собі дві функціональні групи - карбоніл і гідроксил, що взаємно впливають одна на одну:
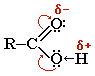
Кислотні властивості карбонових кислот обумовлені зсувом електронної густини до карбонільного кисню і викликаної цим додаткової (у порівнянні зі спиртами) поляризації зв'язку О-Н. У водяному розчині карбонові кислоти дисоціюють на іони:
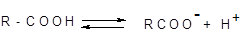 |
Карбонові кислоти виявляють високу реакційну здатність. Вони вступають у реакції з різними речовинами і утворюють різноманітні сполуки, серед яких велике значення мають функціональні похідні, тобто сполуки, отримані в результаті реакцій за карбоксильною групою: солі R-COONa, естери R'-СООR" та аміди R-CONR’R” (де R’ і R” = H або Alk).
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Естери - сполуки з загальною формулою R–COOR',
де R і R' - вуглеводневі радикали. Естери можуть бути отримані при взаємодії карбонових кислот зі спиртами (реакція естерифікації). Каталізаторами є мінеральні кислоти.
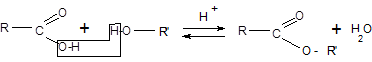 |
Дана реакція обернена. Зворотний процес - розщеплення естеру при дії води з утворенням карбонової кислоти і спирту - називають гідролізом естеру. Гідроліз у присутності лугу відбувається необернено (тому що негативно заряджений карбоксилат-аніон RCOO–, який утворюється, не вступає в реакцію з нуклеофільним реагентом - спиртом).
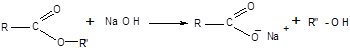
Ця реакція називається омиленням естеру.
Ефіри нижчих карбонових кислот і нижчих одноатомних спиртів мають приємний запах квітів, ягід і фруктів. Ефіри вищих одноосновних кислот і вищих одноатомних спиртів - основа природних вісків. Наприклад, бджолиний віск містить естер з пальмітинової кислоти і мірицилового спирту (мірицилпальмітат) CH3(CH2)14–CO–OCH2(CH2)29CH3.
Жири - складні ефіри гліцерину і вищих одноатомних карбонових кислот.
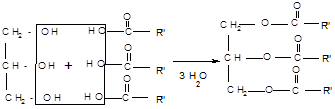 |
гліцерин виші карбонові кислоти жир
Загальна назва таких сполук - тригліцериди або триацилгліцерини, де ацил - залишок карбонової кислоти -C(O)R. До складу природних тригліцеридів входять залишки насичених кислот (пальмітинової C15H31COOH, стеаринової C17H35COOH) і ненасичених (олеїновой C17H33COOH, лінолевої C17H29COOH).
Рослинні жири - олії (соняшникова, соєва, бавовняна й ін.) - рідини (виключення - кокосова олія). До складу тригліцеридів олій входять залишки ненасичених кислот.
Жирам як естерам властива обернена реакція гідролізу, яка каталізується мінеральними кислотами. При участі лугів гідроліз жирів відбувається необернено. Продуктами в цьому випадку є мила - солі вищих карбонових кислот і лужних металів.
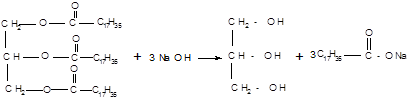
жир гліцерин стеарат натрію
(мило)
Реакція лужного гідролізу жирів, і узагалі всіх естерів, називається омиленням.
7.1. Порівняння сили карбонових і мінеральних кислот
На смужку універсального індикаторного паперу наносять по краплі розчини органічних кислот і соляної кислоти. За допомогою шкали визначають рН цих розчинів. Результати досліду записують в робочий журнал.
7.2. Розчинність карбонових кислот
В пробірки вносять по 0, 5 г кислот: мурашиної, оцтової, масляної, стеаринової та додають по 2 мл води. Вміст пробірок збовтують; якщо кислота не розчиняється, пробірку нагрівають. Після охолодження роблять висновок (якісний) про розчинність у воді кислот, що були взяті для досліду.
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
Дослід повторюють, але як розчинник використовують діетиловий етер (або бензол). Результати записують в робочий журнал.
|
|
