
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Защита от коррозии. Металлические покрытия
|
|
Анодное покрытие – это металлы, стандартный потенциал которых меньше, чем у защищаемого металла.
Для Fe: Zn, Al.
При нарушении целостности покрытия на границе железо-цинк возникает и начинает работать гальванический элемент:
-2℮
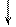


(-) Zn |H2O| Fe (+)
joZn2+/Zn = -0, 763В joFe2+/Fe = -0, 44В
(-) Анод: Zn0 – 2℮ ® Zn2+
(+) Катод: 2H2O + 2℮ ® H2 + 2OH- (на поверхности железа).
Вторичные процессы: Zn2+ + 2OH- = Zn(OH)2.
Железо само не разрушается. Анодное покрытие продолжает играть защитную роль по отношению к основному металлу, являясь протектором.
Катодное покрытие – это металлы, стандартный потенциал которых имеет более высокое значение, чем у защищаемого металла.
Для Fe: Sn, Pb, Cu.
При нарушении целостности покрытия на границе Sn – Fe возникает и начинает работать гальванический элемент
-2℮
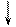


(-) Fe |H2O| Sn (+)
joFe2+/Fe = -0, 44В joSn2+/Sn = -0, 13В
(-) Анод: Fe0 – 2℮ ® Fe2+
(+) Катод: 2H2O + 2℮ ® H2 + 2OH- (на поверхности олова).
Вторичные процессы: Fe2+ + 2OH- = Fe(OH)2
4Fe(OH)2 + O2 +2H2O = 4Fe(OH)3
Катодное покрытие выполняет защитную функцию до тех пор, пока целостность его не нарушена. При нарушении ее катодное покрытие ускоряет коррозию железа.
21. ОБЩИЕ СВОЙСТВА МЕТАЛЛОВ
|
|
