Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Задача 5.
|
|
Определите константу скорости реакции 2НI(г) ® Н2(г) + I2(г) при температуре 2000 С , если предэкспоненциальный множитель A0 = 9, 2·1013, а энергия активации ЕА = 186, 4 кДж/моль. Каков физический смысл константы скорости реакции? От каких параметров и как зависит константа скорости реакции? Укажите ее размерность для Вашей реакции (порядок реакции n =2)
Решение.
Уравнение С.Аррениуса 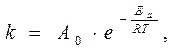
k – константа скорости реакции при данной Т, размерность
А0 – предэкспоненциальный множитель, не зависит от Т
А0 = k, если Еа = 0
Физич. смысл А0 - частотно-ориентационный фактор, учитывающий влияние числа столкновений (z) и ориентации молекул (Poр.) на скорость А0 = z Poр
Для осуществления реакции необходима благоприятная ориентация молекул в момент столкновения.
Уравнение, связывающее скорость реакции с концентрацией исходных веществ, называют кинетическим. Для n=2 основное кинетическое уравнение 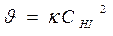
k - константа скорости:
а) не зависит от концентрации
б) зависит от температуры, природы реагирующих веществ, катализатора, площади поверхности раздела фаз.
Физический смысл константы скорости: k – удельная скорость: 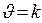 , если С= 1моль/л
, если С= 1моль/л
n = 2 общий порядок реакции
В простых реакциях: n = 1, 2 редко 3 и общий порядок равен молекулярости.
Размерность k зависит от порядка реакции. Для n =2 [k ]= л/(моль× с).
При Т=273 +200=473 К k = 9, 2·1013. exp(-186400/8, 31. 473) = 9, 2·1013 e-46= 9, 2·10-7 л/(моль× с).
Влияние катализаторов на скорость реакции
Катализ: ускорение реакции за счет введения дополнительного вещества – катализатора (Kt), состояние и масса которого в конце реакции остаются неизменными.
k= koe-Ea/RT c катализатором k растет т.к. Еа снижается. Kt входит в состав нового активированного комплекса, отвечающего меньшей Еа, к после распада которого регенерируются в неизменном виде: А+ В + Kt → [ А…В…Kt]→ АВ + Kt
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
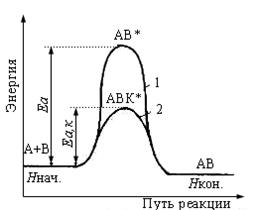 Энергетическая диаграмма некаталитической (1) и каталитической (2) реакции
Энергетическая диаграмма некаталитической (1) и каталитической (2) реакции
Вывод: Катализатор снижает Е а реакции, что приводит к увеличению доли активных молекул и возрастанию скорости реакции.
Гомогенный катализ: Kt и все реагенты-в одном фазовом состоянии (жидком или газообразном).
Ферментативный катализ -природные реакции, катализируемые ферментами - биологическими катализаторами (превращение крахмала в глюкозу, гидролиз эфиров, расщепление белков, брожение, дегидратация СО2 из крови и др.) В организме человека более 30 тысяч (!) ферментов.
Гетерогенный катализ: Kt и реагенты в разных фазах (твердая газообразная; твердая-жидкая) и реакция идет на поверхности Kt. Гетерогенные катализаторы: металлы, оксиды и соли металлов. Каталитические гетерогенные реакции включают стадии:
подвод реагента,
адсорбцию на Kt,
образование активированного комплекса,
образование продукта и его десорбцию.
Стадии гетерогенного катализа:
А + В +Кt→ (А –В –Кt)адс → (А…В …Кt) → (АВ)адс + Кt → АВ + Кt
Пример: CO + ½ O2 → СО2 (Pt –Кt)
идет через: образование активированного комплекса
(СО…О…Pt) → (СО2)адс + Pt → СО2 + Pt Еа ↓ и υ ↑
Kt отличаются:
■ активностью Реакция идет только на активных центрах, обеспечивающих оптимальные условия реакции)
■ избирательностью (влияние Kt на скорость определенной реакции):
■ универсальностью (влияние Kt - металлов Pt – группы на скорость очень многих реакций)
Вещества, увеличивающие активность Кt – промоторы. Вещества, снижающие активность Кt – каталитические яды (мышьяк, ртуть, свинец для Pt).
В обратимых каталитических реакциях Кt в равной степени ускоряют и прямую и обратную реакцию, сокращая время достижения равновесия.
Автокатализ – kt - один из продуктов реакции
Для автокаталитических реакций: А→ В (В –Kt) Кинетическое уравнение 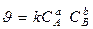 Пример: FeO + H2 = Fe + H2O Fe - kt
Пример: FeO + H2 = Fe + H2O Fe - kt
Особенности кинетики гетерогенных и обратимых реакций
Гетерогенные реакции идут на поверхности раздела фаз, которая и служит реакционным пространством (поверхностью). Поэтому первой особенностью кинетики этих реакций является влияние площади реакционной поверхности на скорость реакции. С учетом площади поверхности равной S общая скорость гетерогенной реакции первого порядка описывается уравнением:
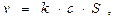
|
где с – концентрация реагента (газообразного или жидкого).
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
Единица измерения скорости гетерогенной реакции в этом случае – [моль× с-1], константы скорости реакции– [м× с-1].
Твердое вещество в кинетическое уравнение не входит.
Например, кинетика гетерогенной реакции СаО(к) + СО2 = СаСО3(к)
описывается уравнением: 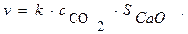
У дельную скорость реакции, отнесенную к единице площади реакционной поверхност и, (для реакции первого порядка описывается уравнением:  )
Единица измерения удельной скорости реакции [моль× с-1× м-2].
Скорость гетерогенной химической реакциизависит от скорости подвода реагента и отвода продукта с поверхности раздела фаз (зона химической реакции), что является второй особенностью этих реакций.
Скорость обратимых гетерогенных и гоиогенных реакций зависит т скоростей прямой и обратной реакции: А + В = Д + К )
Единица измерения удельной скорости реакции [моль× с-1× м-2].
Скорость гетерогенной химической реакциизависит от скорости подвода реагента и отвода продукта с поверхности раздела фаз (зона химической реакции), что является второй особенностью этих реакций.
Скорость обратимых гетерогенных и гоиогенных реакций зависит т скоростей прямой и обратной реакции: А + В = Д + К
Вывод: общая скорость необратимой гетерогенной химической реакции зависит, и удельная скорость реакции не зависит от площади реакционной поверхности. На скорость гетерогенной химической реакции влияют процессы массопереноса. Скорость обратимой реакции определяется разностью скоростей прямой и обратных реакций. | ||||
| Основные учебники и учебные пособия 1. Н.В.Коровин. Общая химия 2. Н.В.Коровин и др. Лабораторные работы по химии 3. Задачи и упражнения по общей химии. Под ред. Н.В.Коровина 4. Общая химия. Теория и расчеты. Под ред. Н.В. Коровина | ||||
|
|

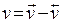 = kпр СА С В – kобр СD СK
= kпр СА С В – kобр СD СK
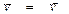 или kпр САС В = kобрСDСK или СDСK/ САС В =Kc =kпр/kобр
или kпр САС В = kобрСDСK или СDСK/ САС В =Kc =kпр/kобр