
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Вывод формулы для вычисления рН в растворах слабых оснований в присутствии их солей
|
|
 |
 MOH M+ + OH-
MOH M+ + OH-
MA = M+ + A-
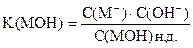
Из уравнения диссоциации
С(M+)» С(МA)
С(MOH) н.д.» С(MOH)
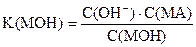
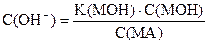
- lg С(OН-) = (- lg K(MOН)) + (- lg С(MOН)) - (- lg С(MА))
pOH = pK(MOН) + pС(MOН) - pС(MА)
 |
pН = 14 - (pK(MOН) + pС(MOН) - pС(MА))
Примеры расчета
1. К 20 мл 0, 3н раствора NH3× H2O прилито 20 мл 0, 2н раствора HNO3.
Вычислить рН в полученном растворе.
| Дано: Сн (NH3× H2O) = 0, 3 моль/л V (NH3× H2O) = 20 мл Сн (HNO3) = 0, 2 моль/л V (HNO3) = 20 мл K (NH3× H2O) = 1, 76× 10-5 |
| рН =? |
Решение:
NH3× H2O + HNO3 = NH4NO3 + H2O
1) Сколько милли-моль-эквивалентов NH3× H2O содержится в 20 мл раствора.
0, 3 × 20 = 6
2) Сколько милли-моль-эквивалентов HNO3 содержится в 20 мл раствора.
0, 2 × 20 = 4
Столько же милли-моль-эквивалентов NH4NO3 содержится в растворе.
3) Сколько милли-моль-эквивалентов NH3× H2O содержится в избытке.
6 - 4 = 2
4) Вычислить общий объем.
20 + 20 = 40
5) Вычислить концентрации NH3× H2O и NH4NO3 после смешивания.
Сн (NH3× H2O) = 2/40 = 0, 05
Сн (NH4NO3) = 4/40 = 0, 1
6) Вычислить pH раствора.
pН = 14 - (pK(NH3× H2O) + pС(NH3× H2O) - pС(NH4NO3))
pK(NH3× H2O) = - lg 1, 76× 10-5 = (- lg 1, 76) + (- lg 10-5) = 5 - 0, 25 = 4, 75
pС(NH3× H2O) = - lg 0, 05 = - lg 5× 10-2 = (- lg 5) + (- lg 10-2) = 2 - 0, 7 = 1, 3
pС(NH4NO3) = - lg 0, 1 = - lg 10-1 = 1
pН = 14 - (4, 75 + 1, 3 - 1) = 14 - 5, 05 = 8, 95
среда слабощелочная
2. В 100 мл 0, 2н раствора NH3× H2O содержится 1, 07 г NH4Cl. Вычислить рН раствора.
Дано:
Сн (NH3× H2O) = 0, 2 моль/л
V (NH3× H2O) = 100 мл
m (NH4Cl) = 1, 07 г
K (NH3× H2O) = 1, 76× 10-5
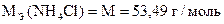
|
| рН =? |
Решение:
1) Вычислить Сн (NH4Cl).
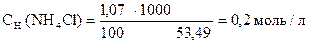
‚ ƒ
1) Сколько г NH4Cl содержится в 1 мл раствора.
2) Сколько г NH4Cl содержится в 1000 мл раствора.
3) Сколько моль-экв NH4Cl содержится в 1000 мл раствора или Сн (NH4Cl).
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
2) Вычислить рН раствора.
pН = 14 - (pK(NH3× H2O) + pС(NH3× H2O) - pС(NH4Cl))
pK(NH3× H2O) = - lg 1, 76× 10-5 = (- lg 1, 76) + (- lg 10-5) = 5 - 0, 25 = 4, 75
pС(NH3× H2O) = - lg 0, 2 = - lg 2× 10-1 = (- lg 2) + (- lg 10-1) = 1 - 0, 3 = 0, 7
pС(NH4Cl) = - lg 0, 2 = - lg 2× 10-1 = (- lg 2) + (- lg 10-1) = 1 - 0, 3 = 0, 7
pН = 14 - (4, 75 + 0, 7 - 0, 7) = 9, 25
среда слабощелочная
3. К 50 мл 0, 05н раствора NH3× H2O прибавлено 50 мл 0, 05н NH4Cl.
Определить рН в полученном растворе.
| Дано: Сн (NH3× H2O) = 0, 05 моль/л V (NH3× H2O) = 50 мл Сн (NH4Cl) = 0, 05 моль/л V (NH4Cl) = 50 мл K (NH3× H2O) = 1, 76× 10-5 |
| рН =? |
Решение:
1. Вычислить концентрации NH3× H2O и NH4Cl после смешивания.
Раствор разбавили в 2 раза, общий объем увеличился в 2 раза, следовательно, концентрации уменьшились в 2 раза.
Сн (NH3× H2O) = 0, 025 моль/л
Сн (NH4Cl) = 0, 025 моль/л
2. Вычислить рН раствора.
pН = 14 - (pK(NH3× H2O) + pС(NH3× H2O) - pС(NH4Cl))
pK(NH3× H2O) = - lg 1, 76× 10-5 = (- lg 1, 76) + (- lg 10-5) = 5 - 0, 25 = 4, 75
pС(NH3× H2O) = - lg 0, 025 = - lg 2, 5× 10-2 = (- lg 2, 5) + (- lg 10-2) = 2 - 0, 4 = 1, 6
pС(NH4Cl) = - lg 0, 025 = - lg 2, 5× 10-2 = (- lg 2, 5) + (- lg 10-2) = 2 - 0, 4 = 1, 6
pН = 14 - (4, 75 + 1, 6 - 1, 6) = 9, 25
среда слабощелочная
|
|
