
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
⚡️ Для новых пользователей первый месяц бесплатно. А далее 290 руб/мес, это в 3 раза дешевле аналогов. За эту цену доступен весь функционал: напоминание о визитах, чаевые, предоплаты, общение с клиентами, переносы записей и так далее.
✅ Уйма гибких настроек, которые помогут вам зарабатывать больше и забыть про чувство «что-то мне нужно было сделать».
Сомневаетесь? нажмите на текст, запустите чат-бота и убедитесь во всем сами!
Аминокислоты и белки
|
|

Глицин кристаллический и 2% раствор; раствор яичного белка;
раствор желатина; 1% СН3СООН, 10% СН3СООН; 
 0, 002н H2SO4; 0, 005н NaOH, 30% NaOH; HNO3 конц.; 0, 5н HCl;
0, 002н H2SO4; 0, 005н NaOH, 30% NaOH; HNO3 конц.; 0, 5н HCl;
 NaNO2 кристаллический; 1%-ный CuSO4; насыщ. раствор NaСl; 1% -ный Pb(CH3COO)2.Фенолфталеин, метилоранж.
NaNO2 кристаллический; 1%-ный CuSO4; насыщ. раствор NaСl; 1% -ный Pb(CH3COO)2.Фенолфталеин, метилоранж.
Спиртовка; электроплитка, плотный фильтр.
Цель работы: у бедиться в амфотерном характере
аминокислот и белков, освоить качественные (цветные) реакции
белков для прогноза их первичной структуры (видов аминокислот).
Опыт 10.1. Доказательство амфотерных свойств глицина.
(а) В полную воды пробирку поместить 1 каплю 0, 002н H2SO4 и 1 каплю метилоранжа (перемешать). Полученный розовый раствор разделить на две пробирки. В одну из пробирок с кислым раствором добавить одну лопаточку сухого глицина. Сравнить окраски растворов.
(б) В полную воды пробирку поместить 1 каплю 0, 005н NaOH и 1 каплю фенолфталеина (перемешать). Полученный окрашенный (щелочной) раствор разделить на две пробирки. В одну из пробирок со щелочным раствором добавить одну лопаточку сухого глицина. Сравнить окраски растворов.
Написать реакции, объясняющие изменения окрасок индикаторов.
Опыт 10.2. Дезаминирование аминокислоты.
К 1 мл 2% -ного глицина добавить несколько кристаллов NaNO2 и
0, 5 мл 0, 5н HCl. Наблюдать выделение N2 (с помощью влажного красного лакмуса убедиться, что выделяется не NH3).
Записать уравнение реакции.
Опыт 10.3. Изоэлектрическая точка и свертывание белков при нагревании.
Свертывание (выпадение в осадок, денатурация) белков при нагревании характерно почти для всех белков (кроме желатина). Наиболее легко и полно осаждение происходит в нейтральной и слабокислой средах – в близи
и з о э л е к т р и ч е с к о й точки. В сильнокислой и сильнощелочной средах осаждения не происходит. Добавление нейтральных солей (NaCl и др.) ускоряет свертывание.
Выполнение опыта
В 5 пробирок поместить по 1 мл раствора яичного белка (пробирки пронумеровать).
1-я – нейтральная среда;
2-я – слабокислая среда (1 капля 1% СН3СООН);
3-я – кислая среда (0, 5мл 10% СН3СООН);
4-я – кислая среда с добавлением NaCl (0, 5мл 10% СН3СООН +
3-5 капель насыщенного раствора NaCl);
5-я – щелочная среда (0, 5мл 10% NaOH).
Пробирки прокипятить. Наблюдать за изменениями, сравнить
изменения и дать им объяснение.
Опыт 10.4. Биуретовая реакция –качественная на пептидную связь.
В две пробирки налить по 1 мл растворов белка и желатина, добавить по 1 мл 30%-ного NaOH и п о с т е н к а м пробирки по 2-3 мл CuSO4. Наблюдать появление окраски.
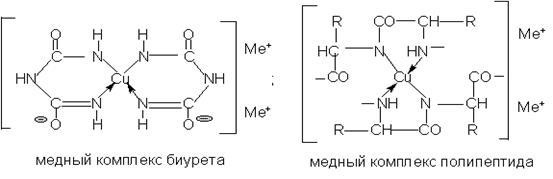
Окрашивание дают: биурет (отсюда название реакции), полипептиды, белки, амиды, имиды и некоторые другие соединения.
Образующиеся при биуретовой реакции окрашенные соединения являются внутренними медными комплексами хелатного строения:
Опыт 10.5. Качественные (цветные) реакции на боковые
|
|
