
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
⚡️ Для новых пользователей первый месяц бесплатно. А далее 290 руб/мес, это в 3 раза дешевле аналогов. За эту цену доступен весь функционал: напоминание о визитах, чаевые, предоплаты, общение с клиентами, переносы записей и так далее.
✅ Уйма гибких настроек, которые помогут вам зарабатывать больше и забыть про чувство «что-то мне нужно было сделать».
Сомневаетесь? нажмите на текст, запустите чат-бота и убедитесь во всем сами!
Катализ
|
|
Одним из наиболее распространенных в химической практике методов ускорения химических реакций является катализ. Катализатор - вещество, которое многократно участвует в промежуточных стадиях реакции, но выходит из нее химически неизменным.
Например, для реакции А2 + В2 = 2АВ
участие катализатора К можно выразить уравнением
А2 + К + В2 ® А2....К + В2 ® А2...К...В2 ® 2АВ + К.
Эти уравнения можно представить кривыми потенциальной энергии (рис. 6.1.).
Из рисунка 6.1 видно, что:
1) катализатор уменьшает энергию активации, изменяя механизм реакции, – она протекает через новые стадии, каждая из которых характеризуется невысокой энергией активации;
2) катализатор не изменяет DН реакции (а также DG, DU и DS);
3) если катализируемая реакция обратимая, катализатор не влияет на равновесие, не изменяет константу равновесия и равновесные концентрации компонентов системы. Он в равной степени ускоряет и прямую, и обратную реакции, тем самым ускоряя время достижения равновесия.
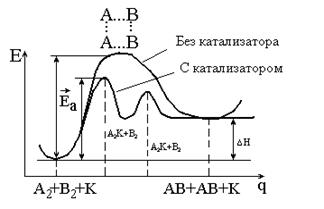
Рис. 6.1. Энергетическая схема хода реакции
с катализатором и без катализатора
Очевидно, в присутствии катализатора энергия активации реакции снижается на величину DЕк. Поскольку в выражении для константы скорости реакции (уравнение 6.7) энергия активации входит в отрицательный показатель степени, то даже небольшое уменьшение Еа вызывает очень большое увеличение скорости реакции: 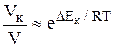 .
.
Пример 6. Энергия активации некоторой реакции в отсутствие катализатора равна 75, 24 кДж/моль, а с катализатором - 50, 14 кДж/моль. Во сколько раз возрастает скорость реакции в присутствии катализатора, если реакция протекает при 250 С, а предэкспоненциальный множитель в присутствии катализатора уменьшается в 10 раз.
Решение. Обозначим энергию активации реакции без катализатора через Еа, а в присутствии катализатора - через Еа1; соответствующие константы скоростей реакций обозначим через k и k1. Используя уравнение Аррениуса (6.7) и принимая k01/k0 = 10, находим:
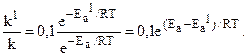 Отсюда
Отсюда 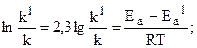
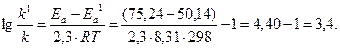
Окончательно находим: 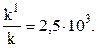

Таким образом, снижение энергии активации катализатором на 25, 1 кДж привело к увеличению скорости реакции в 2500 раз, несмотря на 10-кратное уменьшение предэкспоненциального множителя.
Каталитические реакции классифицируются по типу катализаторов и по типу реакций. Так, например, по агрегатному состоянию катализаторов и реагентов катализ подразделяется на гомогенный (катализатор и реагент образуют одну фазу) и гетерогенный (катализатор и реагенты – в разных фазах, имеется граница раздела фаз между катализатором и реагентами).
Примером гомогенного катализа может быть окисление СО до СО2 кислородом в присутствии NO2 (катализатор). Механизм катализа можно изобразить следующими реакциями:
CO(г) + NO2(г) ® CO2(г) + NO(г) ,
2NO(г) + O2(г) ® 2NO2(г);
и катализатор (NO2) снова участвует в первой реакции.
Аналогично этому может быть катализирована реакция окисления SO2 в SO3; подобная реакция применяется в производстве серной кислоты " нитрозным" способом.
Примером гетерогенного катализа является получение SO3 из SO2 в присутствии Pt или V2O5:
SO2(г) + O2(г) ® SO3(г).
Эта реакция также применяется в производстве серной кислоты (" контактный" метод).
Гетерогенный катализатор (железо) применяется также в производстве аммиака из азота и водорода и во многих других процессах.
|
|
