
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Виды электродов.
|
|
В зависимости от электродных процессов, протекающих на электроде, различают электроды обратимые и необратимые. При изменении направления электрического тока во внешней цепи на обратимых электродах протекают противоположно направленные процессы, на необратимых – происходят различные процессы.
Примером обратимого электрода служит медь, находящаяся в растворе, содержащем Cu2+. Электродный процесс проходит либо в прямом, либо в обратном направлениях:
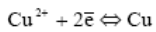
Медь, находящаяся в растворе кислоты, является уже примером необратимого электрода. В этом случае в зависимости от направления тока во внешней цепи на электроде происходит восстановление ионов водорода
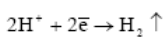
либо окисление атомов меди:
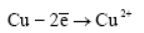
Обратимые электроды классифицируются на следующие группы:
электроды первого и второго рода,
окислительно-восстановительные
ионообменные (мембранные)
Наибольший интерес для исследования коррозионных процессов представляют следующие электроды.
Электроды первого рода представляют собой металл или неметалл, помещенный в раствор соли, содержащей собственные ионы. Примерами служат цинковый и селеновый электроды

с соответствующими значениями электродных потенциалов:

Потенциалы цинкового и селенового электродов зависят от активностей собственных ионов в растворе, поэтому первый называют обратимым относительно катионов, второй – обратимым относительно анион ов.
Газовые электроды (водородный, кислородный, хлорный и др.) относятся также к электродам первого рода. Они могут быть обратимыми относительно катионов (водородный электрод) или анионов (кислородный, хлорный). Все они устроены подобным образом: это металл, находящийся в одновременном контакте с газом и раствором, содержащем ионы этого газа.
Электроды второго рода чувствительны к анионам и представляют собой металл М, покрытый слоем нерастворимой его соли МА с анионом, к которому чувствителен электрод.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Электродами второго рода являются хлорсеребряный и каломельный. Насыщенные хлорсеребряный и каломельный электроды поддерживают постоянный потенциал и применяют в качестве электродов сравнения, по отношению к которым измеряется потенциал индикаторного электрода.
Окислительно-восстановительные электроды – пластина или проволока, изготовленная из трудноокисляемых металлов – платины, золота, палладия. Сама редокс-система находится в растворе, а инертный металл электрода служит лишь передатчиком электронов между веществами ОФ и Вф вещества.
Мембранные электроды различного типа имеют мембрану, на которой возникает мембранный потенциал Е. Величина Е зависит от разности концентраций одного и того же иона по разным сторонам мембраны. Простейшим и наиболее употребляемым мембранным электродом является стеклянный электрод.
Ион-селективные электроды - Смешивание нерастворимых солей типа AgBr, AgCl, AgI и других с некоторыми пластмассами (каучуки, полиэтилен, полистирол) привело к созданию ион-селективных электродов, избирательно адсорбирующих из раствора указанные ионы. Так как концентрация определяемых ионов вне электрода отличается от таковой внутри электрода, равновесия на поверхностях мембраны отличаются, что приводит к возникновению мембранного потенциала.
|
|
