
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Количественный анализ. Химические методы анализа
|
|
Общие понятия. Определение содержания (концентрации, массы и т.п.) компонентов в анализируемом веществе называется количественным анализом. С помощью количественного анализа выявляют массовые соотношения компонентов в анализируемом образце, концентрацию вещества в растворе или в газе. При количественном анализе измеряют те или иные химические, физико-химические и физические параметры анализируемого образца, которые зависят от его состава или содержания того или иного компонента. В большинстве методов полученные при анализе результаты сравнивают со свойствами известных веществ. Результаты анализа обычно выражают в массовых долях, в %.
Количественный анализ проводят в определенной последовательности, в которую входит отбор и подготовка проб, проведения анализа, обработка и расчет результатов анализа. Как и в качественном анализе, различают макрометоды, полумикрометоды, микро- и ультрамикрометоды.
Количественный анализ широко используется для изучения состава руд, металлов, неорганических и органических соединений. В последние годы особое внимание обращается на определение содержания токсичных веществ в воздухе, водоемах, почвах, в продуктах питания, различных товарах.
Классификация методов количественного анализа. Все методы количественного анализа можно разделить на две большие группы: химические и инструментальные. Это разделение условно, так как многие инструментальные методы основаны на использовании химических законов и свойств веществ. Обычно количественные методы анализа классифицируют по измеряемым физическим или химическим свойствам (табл. 16.4).
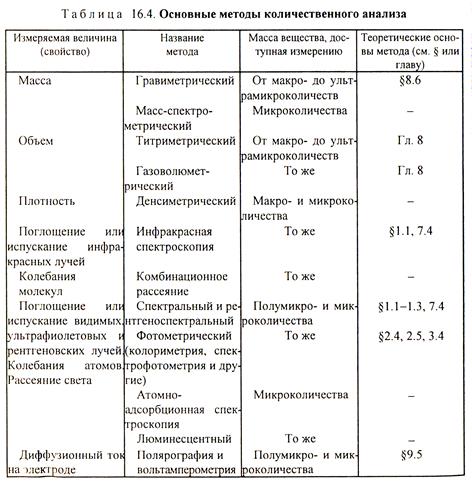

Гравиметрический метод. Сущность метода заключается в получении труднорастворимого соединения, в которое входит определяемый компонент. Для этого навеску вещества растворяют в том или ином растворителе, обычно в воде, осаждают с помощью реагента, образующего с анализируемым соединением малорастворимое соединение с низким значением ПР. Затем после фильтрования осадок высушивают, прокаливают и взвешивают. По массе вещества находят массу определяемого компонента и проводят расчет его массовой доли в анализируемой навеске.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Имеются разновидности гравиметрического метода. В методе отгонки анализируемый компонент выделяют в виде газа, который взаимодействует с реактивом. По изменению массы реактива судят о содержании определяемого компонента в навеске. Например, содержание карбонатов в породе можно определить путем воздействия на анализируемый образец кислотой, в результате которого выделяется СО2: СО32- + 2Н+ → ← Н2СО3→ ← Н2О + СО2
Количество выделившегося СО2 можно определить по изменению массы вещества, например СаО, с которым реагирует СО2.
Одним из основных недостатков гравиметрического метода является его трудоемкость и относительно большая продолжительность. Менее трудоемким является электрогравиметрический метод, при котором определяемый металл, например медь, осаждают на катоде (платиновой сетке)
Сu2+ + 2 е = Сu
По разности массы катода до и после электролиза определяют массу металла в анализируемом растворе. Однако этот метод пригоден лишь для анализа металлов, на которых не выделяется водород (медь, серебро, ртуть).
Титриметрический анализ. Сущность метода заключается в измерении объема раствора того или иного реагента, израсходованного на реакцию с анализируемым компонентом. Для этих целей используют так называемые титрованные растворы, концентрация которых (обычно титр раствора) известны. Титром называется масса вещества, содержащегося в 1 мл (1 см3) титрованного раствора (в г/мл и г/см). Определение проводят способом титрования, т.е. постепенного приливания титрованного раствора к раствору анализируемого вещества, объем которого точно измерен. Титрование прекращается при достижении точки эквивалентности, т.е. достижения эквивалентности реагента титруемого раствора и анализируемого компонента.
Существует несколько разновидностей титриметрического анализа: кислотно-основное титрование, осадительное титрование, комплексонометрическое титрование и окислительно-восстановительное титрование.
В основе кислотно-основного титрования лежит реакция нейтрализации
Н+ + ОН- → ← Н20
Метод позволяет определить концентрацию кислоты или катионов, гидролизирующихся с образованием ионов водорода, титрованием раствором щелочи или определить концентрацию оснований, в том числе анионов, гидролизирующихся с образованием гидроксид-ионов титрованием растворами кислот. Точка эквивалентности устанавливается при помощи кислотно-основных индикаторов, изменяющих окраску в определенном интервале рН. Например, методом кислотно-основного титрования можно определить карбонатную жесткость воды, т.е. концентрацию НСО3- в воде путем титрования ее раствора НС1 в присутствии индикатора метилового оранжевого
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
НСО3- + Н+ = Н2О + СО2 ↑
В точке эквивалентности желтая окраска индикатора переходит в бледно-розовую. Расчет производится по уравнению закона эквивалентов
сэк, НСО3V1 = сэк, HClV2,
где V1, и V2 - объемы анализируемого и титрованного растворов; сэк, HCl - нормальная концентрация эквивалентов вещества НС1 в титрованном растворе, сэкНСO3 - определяемая молярная концентрация эквивалентов ионов НСО3- в анализируемом растворе.
При осадительном титровании анализируемый раствор титруется реагентом, образующим с компонентом титрованного раствора малорастворимое соединение. Точка эквивалентности определяется с помощью индикатора, образующего с реагентом окрашенное соединение, например, красный осадок Аg2СгО4 при взаимодействии индикатора К2СrO4 с избытком ионов Аg+ при титровании раствора хлорида раствором нитрата серебра.
Комплексонометрическое титрование. При комплексонометрическом титровании определяемый компонент в растворе титруется раствором комплексона, чаще всего этилендиаминотетрауксусной кислоты (ЕДТА, комплексона II) или ее двунатриевой соли (комплексона III или трилона Б). Комплексоны являются лигандами и образуют со многими катионами комплексы. Индикаторами точки эквивалентности обычно служат лиганды, образующие с анализируемым ионом окрашенное комплексное соединение. Например, индикатор хромоген черный (см. табл. 16.1) с кальцием и магнием образует комплексы [Са Ind]- и [Мg Ind]- красного цвета. В результате титрования раствора винно-красного цвета, содержащего ионы кальция, магния и индикатор, раствором комплексона III кальций связывается в более прочный комплекс с комплексоном, в точке эквивалентности анионы индикатора освобождаются и придают раствору синюю окраску. Этот метод комплексонометрического титрования используется, например, для определения общей жесткости воды.
Окислительно-восстановительное титрование. Данный способ заключается в титровании раствора восстановителя титрованным раствором окислителя или в титровании раствора окислителя титрованным раствором восстановителя. В качестве титрованных растворов окислителей нашли применение растворы перманганата калия КмnO4 (перманганатометрия), дихромата калия К2Сг2О7 (дихроматометрия), иода I2 (иодометрия). Из титрованных растворов восстановителей следует отметить растворы гидразина N2Н4 (гидразинометрия).
При перманганатометрическом титровании в кислой среде Мn (VII) (малиновая окраска) переходит в Мn (II) (бесцветный раствор). Например, перманганатометрическим титрованием можно определить содержание нитритов в растворе
2КМnО4 + 5КNО2 + ЗН2SО4 = 2МnSО4 + К2SО4 + 5КNО3 + ЗН2О
При дихроматометрическом титровании индикатором служит дифениламин, окрашивающий раствор в синий цвет при избытке дихромат-ионов. При йодометрическом титровании индикатором служит крахмал. Йодометрическое титрование используется для анализа растворов окислителей, в этом случае титрованный раствор содержит иодид-ион. Например, медь можно определить титрованием ее растворов раствором иодида
2Сu2+ + 4I- = 2СuI +I2
Затем образующийся раствор титруется титрованным раствором тиосульфата натрия Na2S2O3 с индикатором крахмалом, добавляемым в конце титрования
2Nа2S2O3 + I2 = 2NaI + Na2S4О6
Итак, существует большое число разновидностей количественного химического анализа, позволяющих определять разнообразные вещества в широких пределах концентраций. Среди химических методов анализа наиболее распространены титрометрические и гравиметрические методы.
Вопросы и задачи для самоконтроля
4. При анализе навески соединения бария получен осадок ВаSО4 с массой после прокаливания 0, 464 г. Какой массе а) Ва; б) ВаО; в) ВаС12.2Н2О соответствует масса полученного осадка?
5. Что такое точка эквивалентности и как ее определяют?
6. Титр раствора КОН равен 0, 0056 г/мл. Вычислите молярную и нормальную концентрацию эквивалентов и молярную концентрацию раствора.
7. На титрование 20 мл раствора Н2SО4 пошло 40 мл 0, 1 М раствора КОН. Вычислите нормальную, молярную концентрацию и титр раствора Н2SО4.
8. На титрование 100 мл воды затрачено 20 мл 0, 05М раствора комплексона III. Вычислите общую жесткость воды.
|
|
