
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Углеводы. Глюкоза. Крахмал и целлюлоза.
|
|
Заслушивание анализа и разработки предложений по теме «Нехватка продовольствия как глобальная проблема человечества и пути ее решения».
Решение заданий для закрепления
№1. Крахмал образуется в процессе фотосинтеза, причём сначала образуется глюкоза, а из неё крахмал:
CO2 -> C6H12O6 -> (C6H10O5)n
nC6H12O6 - > (C6H10O5)n + nH2O
Решите задачу:
Вычислите массу крахмала, который образуется в процессе фотосинтеза? Если известно, что в процессе фотосинтеза участвуют 10 кг воды и 20 л углекислого газа (н.у.).
№2. При взаимодействии сахарозы с водой образуется смесь глюкозы и сахарозы.
Решите задачу:
Вычислите массу раствора сахарозы (массовая доля сахарозы 20%), который подвергли гидролизу (взаимодействию с водой), если при этом выделилось 7, 2 г глюкозы.
№3. Заполните таблицу
| ВАЖНЕЙШИЕ УГЛЕВОДЫ | |||||
| МОНОСАХАРИДЫ | ДИСАХАРИДЫ | ПОЛИСАХАРИДЫ | |||
| НАЗВАНИЯ ПРЕДСТАВИТЕЛЕЙ | |||||
| ХИМИЧЕСКАЯ ФОРМУЛА | |||||
| НАХОЖДЕНИЕ В ПРИРОДЕ | |||||
| ПРИМЕНЕНИЕ |
Задания для самостоятельного выполнения
1. Анализ и разработка предложений по теме «Нехватка продовольствия как глобальная проблема человечества и пути ее решения».
Форма контроля самостоятельной работы:
Заслушивание анализа и разработки предложений по теме «Нехватка продовольствия как глобальная проблема человечества и пути ее решения» на практическом занятии.
Вопросы для самоконтроля по теме:
- Какие классы углеводов вам известны?
- Какую роль в организме играет глюкоза?
- Раскройте процесс расщепления крахмала
- Где применяется целлюлоза?
Тема.4.4 Азотосодержащие соединения: амины, аминокислоты, белки.
Основные понятия и термины по теме
Амины, аминокислоты. Анилин. Реакция Зинина. Фермент
План изучения темы
- Классификация азотсодержащих соединений.
- Амины
- Аминокислоты
- Белки.
Краткое изложение теоретических вопросов:
Азотсодержащие органические соединения — один из важнейших типов органических соединений. В их состав входит азот. Они содержат в молекуле связь углерод-водород и азот-углерод.
В нефти содержится азотсодержащий гетероцикл-пиридин. Азот входит в состав белков, нуклеиновых кислот и некоторых липидов
Классификация
| Общая формула | Название класса соединений |
| R-NH2, R-NH-R', R-N(-R')-R" | Амины |
| R(CONH2)1 | Амиды |
| R-CN | Нитрилы |
| NH2-CHR-COOH1 | Аминокислоты |
| R(C=O)(NH)R1 | Пептиды |
Амины - органические производные аммиака, в молекулах которого один, два или все три атома водорода замещены органическими радикалами.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
По числу радикалов амины делятся на первичные, вторичные и третичные.
| Общая формула первичных аминов: | Общая формула вторичных аминов: | Общая формула третичных аминов: |

| 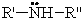
| 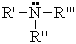
|
По типу простейших радикалов амины делятся на предельные, непредельные и ароматические:
| Предельный амин: | Непредельный амин: | Ароматический амин: |
| CH3—CH2—NH2 этиламин (аминоэтан) | CH2=CH—CH2—NH2 аллиламин (3-аминопропен-1) | C6H5—NH2 фениламин (анилин) |
· Взаимодействие с водой. Водные растворы алифатических аминов проявляют щелочную реакцию, так как при их взаимодействии с водой образуются гидроксидыалкиламмония, аналогичные гидроксиду аммония:

· Взаимодействуя с кислотами, амины образуют алкиламмониевые соли, в большинстве случаев растворимые в воде. Например, амины присоединяют галогеноводороды:

Основные свойства анилина:
а) ароматический амин – анилин имеет большое практическое значение;
б) анилин C6H5NH2 – это бесцветная жидкость, которая плохо растворяется в воде;
в) имеет светло-коричневую окраску при частичном окислении на воздухе;
г) анилин сильно ядовит.
Основные свойства у анилина проявляются слабее, чем у аммиака и аминов предельного ряда.
1. Анилин не изменяет окраски лакмуса, но при взаимодействии с кислотами образует соли.
2. Если к анилину прилить концентрированную соляную кислоту, то происходит экзотермическая реакция и после охлаждения смеси можно наблюдать образование кристаллов соли: [C6H5NH3]+Cl- – хлорид фениламмония.
3. Если на раствор хлорида фениламмония подействовать раствором щелочи, то снова выделится анилин: [С6Н5NН3]+ + Сl- + Nа+ + ОН- -> Н2О + С6Н5NН2 + Nа+ + СI-. Здесь выражено влияние ароматического радикала фенила – С6Н5.
4. В анилине C6H5NH2 бензольное ядро смещает к себе неподеленную электронную пару азота аминогруппы. При этом электронная плотность на азоте уменьшается и он слабее связывает ион водорода, а это значит, что свойства вещества как основания проявляются в меньшей степени.
5. Аминогруппа влияет на бензольное ядро.
6. Бром в водном растворе не реагирует с бензолом.
Способы применения анилина:
1) анилин – один из важнейших продуктов химической промышленности;
2) он является исходным веществом для получения многочисленных анилиновых красителей;
3) анилин используется при получении лекарственных веществ, например сульфаниламидных препаратов, взрывчатых веществ, высокомолекулярных соединений и т. д. Открытие профессором Казанского университета Н.Н. Зининым (1842 г.) доступного способа получения анилина имело большое значение для развития химии и химической промышленности.
1. Промышленность органического синтеза началась с производства красителей.
2. Широкое развитие этого производства стало возможным на основе использования реакции получения анилина, известной сейчас в химии под названием реакции Зинина.
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
Особенности реакции Зинина:
1) эта реакция заключается в восстановлении нитробензола и выражается уравнением:
С6Н5-NO2 + 6Н -> С6Н5-NН2 + 2Н2О;
2) распространенным промышленным способом получения анилина является восстановление нитробензола металлами, например железом (чугунными стружками), в кислой среде;
3) восстановление нитросоединений соответствующего строения – это общий способ получения аминов.
Амины являются очень токсичными веществами. Опасно как вдыхание их паров, так и контакт с кожей. Амины, например анилин, способны всасываться сквозь кожу в кровь и нарушать функции гемоглобина, что может привести к летальному исходу. Симптомами отравления крови амином являются посинение кончиков пальцев, носа, губ, одышка, учащенные дыхание и сердцебиение, потеря сознания. В случае попадания амина на незащищенные участки кожи необходимо быстро и аккуратно, не увеличивая площадь поражения, очистить пораженный участок кожи ватой, смоченной в спирте. В случае отравления вывести пострадавшего на свежий воздух, обратиться к врачу.
Аминокислоты – органические бифункциональные соединения, в состав которых входят карбоксильные группы –СООН и аминогруппы -NH2. Общая формула молекул аминокислот - NH2—R—COOH, где R - двухвалентный радикал.
Аминокислоты классифицируют по двум структурным признакам.
1. В зависимости от взаимного расположения амино- и карбоксильной групп аминокислоты подразделяют на a-, b-, g-, d-, e- и т. д.
2. По характеру углеводородного радикала различают алифатические (жирные) и ароматические аминокислоты. Приведенные выше аминокислоты относятся к жирному ряду. Примером ароматической аминокислоты может служить пара-аминобензойная кислота
Аминокислоты в зависимости от поступления в организм делятся на заменимые и незаменимые.
В таблице указаны незаменимые аминокислоты, присутствие которых в белках пищи обязательно; частично заменимые аминокислоты, которые в небольших количествах синтезируются в организме; условно заменимые аминокислоты, для синтеза которых необходимы незаменимые аминокислоты и, наконец, заменимые аминокислоты, потребность в которых может быть восполнена синтезом из других веществ.
| Незаменимые | Условно заменимые | Частично заменимые | Заменимые |
| ТриптофанФенилаланинЛизинТреонинМетионинЛейцинИзолейцинВалин | ТирозинЦистеин | ГистидинАргинин | ГлицинАланинСеринГлутаматГлутаминАспартатАспарагинПролин |
Аминокислотный состав характеризует пищевую ценность белка. Чем выше содержание незаменимых аминокислот, тем больше пищевая ценность белка. Норма белков в питании составляет примерно 100 г в сутки.
Белки
Белки выполняют множество самых разнообразных функций, характерных для живых организмов.
Каталитическая функция. Большинство известных в настоящее время ферментов, называемых биологическими катализаторами, является белками. Эта функция белков, хотя и не оказалась уникальной, определяет скорость химических реакций в биологических системах.
Транспортная функция. Дыхательная функция крови, в частности перенос кислорода, осуществляется молекулами гемоглобина – белка эритроцитов. В транспорте липидов принимают участие альбумины сыворотки крови. Ряд других сывороточных белков образует комплексы с жирами, медью, железом, тироксином, витамином А и другими соединениями, обеспечивая их доставку в соответствующие органы-мишени.
Защитная функция. Основную функцию защиты в организме выполняет иммунная система, которая обеспечивает синтез специфических защитных белков-антител в ответ на поступление в организм бактерий, токсинов, вирусов или чужеродных белков.
Сократительная функция. В акте мышечного сокращения и расслабления участвует множество белковых веществ. Однако главную роль в этих жизненно важных процессах играют актин и миозин – специфические белки мышечной ткани.
Структурная функция. Белки, выполняющие структурную (опорную) функцию, занимают по количеству первое место среди других белков тела человека. Среди них важнейшую роль играют фибриллярные белки, в частности коллаген в соединительной ткани, кератин в волосах, ногтях, коже, эластин в сосудистой стенке и др.
Гормональная функция. Обмен веществ в организме регулируется разнообразными механизмами. В этой регуляции важное место занимают гормоны, синтезируемые не только в железах внутренней секреции, но и во многих других клетках организма. Ряд гормонов представлен белками или полипептидами, например гормоны гипофиза, поджелудочной железы и др.
Питательная (резервная) функция. Эту функцию выполняют так называемые резервные белки, являющиеся источниками питания для плода, например белки яйца (овальбумины). Основной белок молока (казеин) также выполняет главным образом питательную функцию.
Для живых организмов характерны широкое разнообразие белковых структур и их высокая упорядоченность; последняя существует во времени и пространстве. Удивительная способность живых организмов к воспроизведению себе подобных также связана с белками. Сократимость, движение – непременные атрибуты живых систем – имеют прямое отношение к белковым структурам мышечного аппарата. Наконец, жизнь немыслима без обмена веществ, постоянного обновления составных частей живого организма, т.е. без процессов анаболизма и катаболизма (этого удивительного единства противоположностей живого), в основе которых лежит деятельность каталитически активных белков – ферментов.Гемоглобин, транспортирующий кислород в крови - пример четвертичной структуры белка. Антитела– это белки, которые вырабатываются иммунной системой организма при вторжении в него чужеродного белка, бактерии, вируса. Они опознают чужака и участвуют в его уничтожении.
Лабораторные работы/ – «не предусмотрено»
Практические занятия:
|
|
