
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
МОДУЛЬ №4 2 страница
|
|
У лужному середовищі при високих температурах залишки амінокислот перетворюються і можливо конденсуються між собою, утворюючи міжмолекулярні поперечні зв’язки. У дослідах на щурах показано, що, наприклад, лізиноаланін стимулює нефрокальциноз, діарею, облисіння. Тому зараз вирішується питання про введення допустимих концентрації лізиноаланіну (300мг на 1кг) у продуктах харчування.
4. Вплив інших факторів на структуру білків
Структурні перетворення білків, які теж порушують природні білково-ліпідні взаємодії можуть внаслідок несприятливих погодніх умов при визріванні зерна, вражені шкідниками, мікрофлорою, зниженням або підвищенням температури при зберігання і переробці сировини, дії механічних та фізико-хімічних факторів (перемішування, гомогенізація, замішування, ІЧ-проміння, ультразвук, дія солей, вуглекислого газу, азоту, етилену та ін.).
Вільні ліпіди окиснюються і здатні до утворення міжмолекулярних і внутрішньомолекулярних зв’язків у білках, утворюючи нові полімери. Окиснювальне псування білків пов’язане з втратою незамінних амінокислот і особливо небезпечне при переробці олійної та жирової сировини. При подрібненні насіння і зерна відбувається теплова агрегація білків, при інтенсивному замісі тіста можлива їх деструкція з розривом ковалентних зв’язків. Для уповільнення небажаних реакцій додають ферментні препарати, антиоксиданти з метою попередження взаємодії ліпідів з білками.
Наприклад, при обробці молока ультразвуком створюються умови для різних хімічних перетворень – швидкість потоку рідини досягає 400км/год, а температура наближається до 2100°С.
Використання нових технологічних процесів у харчовій промисловості має бути обгрунтованим, потребує вивчення їзх впливу на молекулярну структуру білків для забезпечення якості харчових продуктів і збереження здоров’я населення.
Лекція №15
Обмін нуклеїнових кислот в організмі
[ 1.с. 349-351; 2. с. 389-416; 4. с. 328-395 ]
План
1. Обмін нуклеїнових кислот. Розщеплення і синтез нуклеїнових кислот.
2. Матричний синтез нуклеїнових кислот.
1.ОБМІН НУКЛЕЇНОВИХ КИСЛОТ. РОЗЧЕПЛЕННЯ І СИНТЕЗ НУКЛЕЇНОВИХ КИСЛОТ.
Вивчення обміну нуклеїнових кислот має важливе значення для розуміння таких загальнобіологічних проблем, як проблеми спадковості і мінливості, специфічності білків, регуляції біохімічної діяльності клітини, механізму вірусної інфекції тощо. Це пояснюється, насамперед, тим, що нуклеїнові кислоти є основними носіями спадкової інформації і відіграють провідну роль у процесах синтезу білка в організмі.
Розщеплення нуклеїнових кислот
Нуклеїнові кислоти потрапляють в організм з їжею у складі складних білків – нуклеопротеїдів. Внаслідок послідовної дії ферментів, які знаходяться у шлунковому і кишковому соках, нуклеопротеїди розщеплюються на прості білки, переважно протаміни і гістони, і нуклеїнові кислоти. Прості білки далі розщеплюються до амінокислот, які всмоктуються.
Розщеплення нуклеїнових кислот до нуклеотидів. Нуклеїнові кислоти, які трворились про розщепленні нуклеотеїдів, розщеплюються під впливом комплексу ферментів, що мають загальну назву нуклеази. Оскільки ці ферменти каталізують реакції розриву фосфодіефірних зв’язків у молекулах нуклеїнових кислот, то їх часто відносять до групи ферментів- фосфодіестераз.
Відомо два види нуклеаз: ендонуклеази й екзонуклеази. Перші каталізують процеси гідролізу фосфодіефірних зв’язків усередині молекул нуклеїнових кислот. Під їх впливом нуклеїнові кислоти розщеплюються переважно на олігонуклеотиди і велику кількість мононуклеотидів.
Екзонуклеази каталізують реалізують реакції послідовного відщепленні мононуклеотидів від одного з кінців полінуклеотидного ланцюга нуклеїнових кислот.
Нуклеази, що розщеплюють РНК, називають рибонуклеазами, а ті, що розщеплюють ДНК, - дезоксирибонуклеазами. Крім цього є велика група неспецифічних нуклеаз, які здатні каталізувати реакції розщеплення і РНК, і ДНК.
Більшість нуклеаз є гідролазами, однак частина із них належать до групи фосфотрансфераз. Прикладом нуклеаз, які каталізують розщеплення нуклеїнових кислот за участю транферазної реакції, є група ендорибонуклеаз.
Вони каталізують реакцію перенесення залишку фосфорної кислоти від п’ятого вуглецевого атома рибози одного нуклеотиду до другого атома рибози наступного нуклеотиду. За цих умов полінуклеотидний ланцюг розривається і на одному з його кінців утворюється фосфодіефірний зв’язок між другим і третім вуглецевими атомами рибози:

У тканинах нуклеїнові кислоти також розщеплюються до мононуклеотидів при каталітичній дії тканинних нуклеаз, дезоксорибонуклеаз і рибонуклеаз, які в основному зосереджені в мітохондріях клітин.
Розщеплення нуклеотидів. Нуклеотиди, що утворилися, далі розщеплюються під впливом комплексу ферментів на простіші сполуки.
Початковою стадією їх розщеплення є відщеплення фосфорної кислоти з утворенням відповідних нуклеозидів. Реакцію каналізують фосфатази (нуклеотидази)
Далі залишок рибози від аденозину переноситься до фосфорної кислоти під впливом ферменту фосфорилази, специфічного для кожного нуклеозиду:

Перетворення пуринових і піримідинових основ до кінцевих продуктів. Початковою стадією пуринових основ (аденінуі гуаніну) є дезамінування їх під впливом ферментів пуриндезаміназ (аденази або гуанази). Під час дезамінування аденіну і гуаніну утворюється відповідно гіпоксантин і ксантин:

Розчеплення і синтез нуклеїнових кислот.
Одночасно з розщепленням нуклеїнових кислот у тканинах організму постійно відбувається їх синтез. Уже з’ясовано основні етапи біосинтезу нуклеїнових кислот. Доведено, що біосинтез молекул РНК і ДНК розпочинається з біосинтезу рибонуклеозид-5 -трифосфатів і дезоксирибонуклеозид- 5 - трифосфатів, тобто з відповідних піринових і піримідинових трифосфонуклеотидів.
Біосинтез пуринових нуклеотидів. Процес розпочинається з формування пуринових основ на рибозо- 5 - фосфаті, який під впливом ферменту рибозофосфатпірофосфокінази взаємодіє з АТФ, внаслідок чтого утворюється 5-фосфорибозил- 1- пірофосфату:

Біосинтез піримідинових нуклеотидів. В організмах людини і тварин подібно нуклеотидам синтезуються також піримідинові нуклеотиди, які утворюються з карбамоїлфосфату й аспарагінової кислоти. Проміжним продуктом є оротова кислота.
Розпочинається реакція з утворення карбамоїлфосфату з NH3 і СО2 за участю АТФ:

3. МАТРИЧНИЙ СИНТЕЗ НУКЛЕЇНОВИХ КИСЛОТ.
Синтез ДНК. Оскільки у молекулах ДНК закодована вся генетична інформація організму, синтез і відтворення їх є неохідним і життєвоважливим процесом.
Процес синтезу ДНК називається реплікацією (копіювання, самоподвоєння), оскільки передача інформаціїї відбувається в межах одного виду нуклеїнових кислот (від ДНК до ДНК). Реплікація відбувається у процесі росту і нормального ДНК- вмісних структур (ядер, мітоходндрій, пластид в еукаріот), а також у процесі поділу бактеріальних клітин та під час розмноження вірусів.
Пізніше було встановлено, що для ДНК характерним є напівконсервативний механізм реплікації- у кожній новій синтезованій молекулі один ланцюг «старий», одержаний з вихідної материнської ДНК, а другий- «новий», синтезований (дочірній), тобто реплікація проходить так, що два ланцюги- вихідний і реплікований, сполучаючись між собою, утворюють наступне покоління молекул ДНК.
Реплікація ДНК - багатоступінчастий процес, для здійснення якого неохідні певні умови і наявність чотирьох видів рибо- і де-зоксирибонуклеозид-5-трифосфатів, матриці у вигляді дволанцюгової ДНК, ферментів і білкових речовин, затравки (праймера), іонів металів (Mg, Mn).
Матрицею служить молекула ДНК, яка реп лікується. Разом з цим для здійснення реплікації необхідно близько 20 реплікативних факторів, що називаються ДНК- репліказною системою, або реплісомою. Важливими компонентами ДНК- репліказної системи є ферменти синтезу ДНК.
Важливим компонентом ДНК- репліказної системи є також білкові речовини, які забезпечують протікання ряду неохідних етапів синтезу ДНК, зокрема таких як:
1. впізнавання» місця початку реплікації ДНК ферментами ДНК- полімер азами;
2. локальне розкручування дуплексу ДНК і вивільнення одно ланцюгових матриць;
3. стабілізація утвореної структури;
4. синтез затравних ланцюгів (праймерів) для ініціації ДНК- полімерази III;
5. переміщення реплікативної вилки в ході копіювання;
6. закінчення синтезу та утворення нативної конформації молекули ДНК.
Ці процеси забезпечують ДНК- зв’язуючими білками (ДЗБ), ДНК- розкручуючими білками (хеліказами), ДНК- стабілізуючими білками (гір азами) тощо.
Ініціація. Цей етап синтезу ДНК об’єднує процеси, які забезпечують початок синтезу полінуклеотидного ланцюга. Суть їх полягає у формуванні ре плікативної вилки та синтезі праймера.
Елонгація, або подовження полінуклеотидного ланцюга, включає два процеси: реплікацію ділянок материнської ДНК і сполучення синтезованих ділянок між собою. Ці процеси забезпечують ДНК- полімеразою III, яка виявляє полімеразну та нуклетидилтрансферазну активність.
Термінація. Механізм термі нації, або завершення синтезу ДНК, вивчено недостатньо. В геномі деяких бактерій термінацію здійснює спеціальний термінатор, в інших таких термінатор відсутній. Тому припускають, що реплікація завершується після зустрічі двох реплікативних вилок, які рухаються назустріч одна одній.
Лекція №16, 17, 18, 19
Обмін вуглеводів
[ 1.с. 365-401; 2. с. 416-457; 4. с. 222-236 ]
Лекція №16
Обмін вуглеводів
План
1. Біологічна роль вуглеводів.
2. Перетравлювання і всмоктування вуглеводнів.
3. Взаємоперетворювання моносахаридів в організмі.
БІОЛОГІЧНА РОЛЬ ВУГЛЕВОДІВ.
Вуглеводи, як і білки та ліпіди, становлять важливу групу природних органічних речовин, які є необхідними компонентами клітин і тканин живих організмів. Біологічна роль вуглеводів визначається насамперед тим, що вони є основним джерелом енергії, необхідної для забезпечення метаболічних реакцій організму, та важливим резервним енергетичним фондом, який здатний досить швидко мобілізуватись, задовольняючи певні потреби організму, що визначаються його функціональним станом та рівнем метаболічних процесів. У тканинах організмів людини і тварин роль резервного вуглеводу виконує глікоген, наявність якого дає змогу забезпечити організм енергією в період недостатнього надходження вуглеводів із продуктами харчування.
Особливо важлива роль вуглеводів в енергозабезпеченні клітин головного мозку, де глюкоза є основним енергетичним джерелом, без якого неможливе нормальне функціонування центральної нервової системи.
Досить важливою ж також пластична, або структурна, функція вуглеводів. Вуглеводи та їх похідні становлять основу структури рослинних організмів та внутрішньоклітинних включень організмів людини і тварин. Вони входять до складу основної речовини кісткової та сполучної тканин, виконуючи важливу опірну функцію.Вуглеводи, зокрема глюкоза, є обов’язковим компонентом біологічних рідин організму, їй належить важлива роль у забезпеченні протікання осмотичних процесів. Важлива роль належить вуглеводам також у знешкодженні токсичних продуктів обміну та хімічних речовин, у підтримуванні сталості внутрішньоклітинного середовища- гомеостазу.
Вуглеводи необхідні також для синтезу багатьох біополімерів- нуклеїнових кислот, нуклеотидних коферментів, глюкопротеїдів, мукополісахаридів, гліколіпідів та глікопептидів, які відіграють важливу роль у забезпеченні міжклітинних контактів, мембранної проникності та імунних реакцій організму.
Досить важливим є також збалансованість окремих вуглеводів та подібних до них речовин у добовому раціоні. В середньому на частку полісахаридів (крохмалю) в добовому раціоні повинно припадати 75%, цукру-20, пектинових речовин-3, клітковини-2%.
Основна маса вуглеводнів (70%), які надходять до організму з продуктами харчування, окислюється до кінцевих продуктів (СО2 і Н2О), 20-25%- перетворюється на жири, 2-5% використовується для синтезу резервного полісахариду –глікогену. При надмірному споживанні вуглеводів на жири може перетворюватись до 35-40% вуглеводів і до 9-12% резервуватись і вигляді глікогену.
ПЕРЕТРАВЛЮВАННЯ І ВСМОКТУВАННЯ ВУГЛЕВОДІВ.
Основним джерелом вуглеводнів для людини і тварини є харчові продукти рослинного походження, в яких містяться крохмаль, клітковина, сахароза, глюкоза. З продуктами харчування тваринного походження надходять глікоген, лактоза та інші вуглеводи. В харчовому раціоні людини найбільше значення має глікоген, а в раціоні сільськогосподарських тварин- клітковина.
Перетравлювання вуглеводів. Вуглеводи, які потрапляють в організм людини у вигляді полі- і дисахаридів (крохмаль, глікоген, сахароза, мальтоза, лактоза), не можуть використовуватися безпосередньо. Засвоєння цих речовин організмом стає можливим лише після їх розщеплення до моносахаридів. Цей процес розпочинається порожнині рота під впливом ферменту амілази слини, яка належить до класу гідролаз, підкласу глікозидаз.
З порожнини рота їжа потрапляє у шлунок, де дія амілази слини може тривати 20-30 хв, поки харчова маса не набуде кислого характеру. Зміна рН середовища (рН шлункового соку дорівнює 1, 5- 2) повністю інактивує фермент, оптимальна каталітична дія якого виявляється при рН=6, 8…7, 2.
Основні процеси перетравлювання вуглеводів відбувається в тонкій кишці, де для цього є оптимальні умови – слабколужне середовище і велика кількість ферментів, що виділяються з панкреатичним і кишковим соком. Це такі ферменти, як α - амілаза, мальтоза, сахараза, лактаза, декстриназа та деякі інші. Фермент декстриназа (аміно- 1, 6- глюкозид аза) розщеплює 1, 6- зв’язки у молекулах крохмалю і глікогену.
Доведено, що процеси перетравлювання вуглеводів здійснюються не лише в тонкій кишці, а й на мембранах епітеліальних клітин слизової оболонки, де локалізовані відповідні ферменти.
Перетравлювання клітковини. На відміну від інших вуглеводів, перетравлювання клітковини має свої особливості. У травному каналі людини і тварин відсутні ферменти, які здійснюють гідролітичне розщеплення клітковини, зокрема β - амілаза. Цей фермент продукується в основному мікроорганізмами. Тому основним місцем перетравлювання є нижні відділи тонкої і особливо товста кишка у людини і рубець у жуйних тварин, де під впливом ферментів мікрофлори проходить її ферментативний гідроліз.
За участю ферментів клітковина розщеплюється на дисахариди, зокрема на целобіозу, яка під дією ферменту целобіози розкладається на глюкозу.
Частина глюкози, що утворилась, потрапляє у кров і доставляється до різних органів і ткани організму. Решта глюкози, що утворилась під час гідролізу клітковини, використовується для забезпечення процесів життєдіяльності мікрофлори кишок.
Всмоктування вуглеводів. При послідовній дії відповідних ферментів їжі- полі-, ольго- і дисахариди- розщеплюються на прості сполуки- моносахариди (глюкозу, фруктозу, галактозу та ін.), які через капіляри кишкових ворсинок потрапляють у кровоносну систему і з током крові через ворітну вену доставляються в печінку.
Важливу роль відіграють також процеси трансмембранного транспорту моносахаридів за участю спеціальних переносників білкової природи. На зовнішній мембрані епітеліальних клітин утворюється комплекс моносахарид - переносник, який доставляється крізь мембрану в середину клітини. Тут комплекс розщеплюється і переносник транспортується в зворотному напрямку, а моносахариди потрапляє в кров’яне русло.
Швидкість всмоктування моносахаридів різна. Якщо умовно прийняти швидкість всмоктування глюкози за 100%, то для галактози ця величина становитиме 110%, для фруктози- 43, занози-19, ксилоли-15, арабінози -9%. З наведених даних видно, що гексози всмоктуються швидше, ніж пентози, хоча останні мають меншу молекулярну масу. Відмінність у швидкості всмоктування моносахаридів, очевидно, зумовлена різними механізмами перенесення їх крізь мембрани клітин кишкового епітелію.
Моносахариди, в основному глюкоза, всмоктуються із тонкої кишки в кров. Далі з кров’ю через систему ворітної вени потрапляють у печінку та інші органи і тканини організму.
ВЗАЄМОПЕРЕТВОРЮВАННЯ МОНОСАХАРИДІВ В ОРГАНІЗМІ.
Як вже зазначалось, в організм людини і тварин разом з глюкозою потрапляють невеликі кількості таких моносахаридів, як фруктоза, галактоза, заноза та деякі інші. Дослідження їх обміну показало, що вони здатні до взаємоперетворення. Так, фруктоза і заноза можуть перетворюватися на глюкозу і навпаки. В цей процес вступають не вільні моносахариди, а їх фосфорні ефіри. Реакції фосфорилювання моносахаридів здійснюються за участю АТФ і специфічних фосфотранфераз (кіназ).
Процес взаємоперетворення моносахаридів забезпечується досить важливою особливістю їх фосфорних ефірів – здатністю до ізомеризації, яка може здійснюватися як внаслідок стереоізомерії (зміни просторового розташування атомів і атомних груп у молекулі), так під час внутрішньо молекулярного перенесення атомів. У першому випадку реакції каналізують ізомерази, у другому- мутази або епімерази.
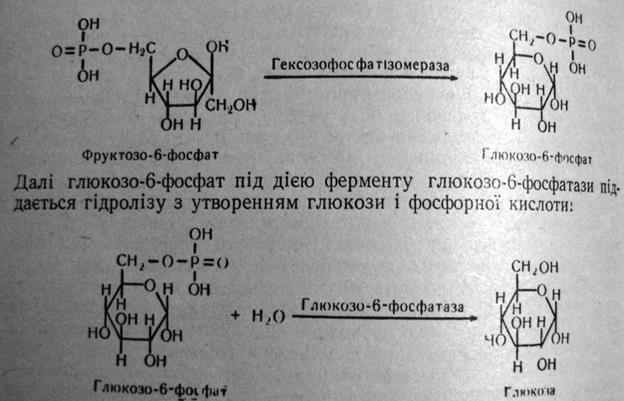 Встановлено, що в клітинах печінки фруктоза у вигляді фруктозо- 6- фосфату може перетворюватись на глюкозу. Спочатку фруктозо-6 фосфат за участю ферменту гексозофосфатізомерази перетворюється на глюкозо-6- фосфат:
Встановлено, що в клітинах печінки фруктоза у вигляді фруктозо- 6- фосфату може перетворюватись на глюкозу. Спочатку фруктозо-6 фосфат за участю ферменту гексозофосфатізомерази перетворюється на глюкозо-6- фосфат:
Лекція 17
Анаеробна дисиміляція вуглеводів (гліколіз)
[ 1.с. 378-383]
Гліколіз є складним ферментативним процесом, що ві дбувається переважно в м’язовій тканині. Це біологічне окиснення глюкози в анаеробних умовах. Гідроліз супроводжується вивільненням енергії, що частково акумулюється в макроергічних зв’язках АТФ, а частково диспергується у вигляді теплоти. Значна части на енергії зберігається в кінцевих продуктах гліколізу і спиртового бродіння - у лактаті й етанолі. Глікогеноліз - анаеробне окиснення глюкози та глікогену в тканинах.
Анаеробне розщеплення глюкози відбувається у дві стадії. Ні) першій стадії глюкоза під дією глюкокінази (гексокінази) фосфорилюється, використовуючи АТФ як донора фосфатної групи.

Процес первинного фосфорилюваяня глюкози з утворенням
фосфорного ефіру називається «шлюзовою» реакцією, або реак-
цією «запала», після якої цей моносахарид включається в інші
реакції.
 Глюкозо-6-фосфат, що утворюється при цьому, перетворюєть-
Глюкозо-6-фосфат, що утворюється при цьому, перетворюєть-
ся потім під дією ферменту фосфоглюкомутази на фруктозо-
6-фосфат.
Надалі за участі фосфофруктокінази й АТФ відбувається фс-
сфоріїлювання фруктозо-6-фосфата з утворенням фруктозо-1, 6-
дифоефата.
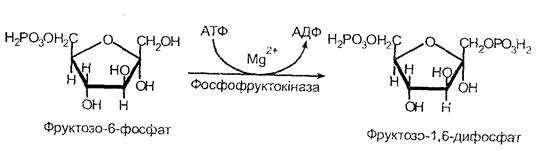
Фруктозо-1, 6-дифосфат є тиловим продуктом гліколізу. Під дією ферменту альдолази відбувається його розщеплення на дві тріози: фосфодіоксиадетон і фосфогліцероловий альдегід. Такий розподіл називається дихотомією, а гліколіз - дихотомічним циклом обміну вуглеводів.

Під дією ферменту тріозофосфатізомерази можливе взаємне перетворення тріоз. За співвідношення 5% фосфогліцеролового альдегіду й 95% фосфодіоксиацетону встановлюється рухлива рівновага.
Фосфодіоксиацетон перетворюється на гліцеральдегід-3-фосфат, і всі наступні реакції відбувається з двома молекулами фосфогліцеролового альдегіду. Крім того, він відновлюється в гліцеральдегід-3-фосфат, що використовуається для синтезу різних ліпідів. Таким чином, він є сполучною ланкою між гліколізом й обміном ліпідів.
Утворенням гліцеральдегід-3-фосфату завершується перший, підготовчий етап гліколізу.
Друга стадія, що має важливе значення - найбільш складна. Вона містить окисно-відновну реакцію (гліколітична окспдоредукція), сполучену із субстратним фосфорилюванням, у процесі якого утворюється АТФ.
У процесі взаємодії гліцеральдегід-3-фосфату з особливим ферментом - HSE, у білковій частині якого міститься сульфгідрильна група (SH), утворюється проміжний фермент - субстратний комплекс:
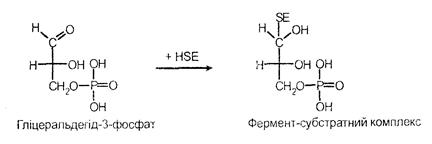
Потім відбувається його дегідрування за участі НАД, при цьому нагромаджується Н+, з’являються відновлена форма НАДН2 і проміжний макроергічний комплекс.

При взаємодії його з неорганічною фосфатною кислотою утворюється 1, 3-дифосфогліцеролова кислота. Після цього макроергічна сполука взаємодіє з АДФ, утворюються АТФ і 3-фосфогліцерат.

У цій реакції відбувається перетворення альдегідної групи гліцеральдегід-3-фосфата в карбоксильну з виділенням енергії, що запасається в АТФ.

Утворення АТФ із високоенергетичних сполук називається субстратним фосфорилюванням.
 Під дією ферменту фосфогліцератфосфомутази (фосфогліце- ромутази) 3-фосфогліцеролова кислота перетворюється (ізомеризується) на 2-фосфогліцеролову кислоту (макроергічну сполуку), що потім під дією ферменту енолази дегідруеться й переходить в енольну форму 2-фосфопіровиноградної кислоти.
Під дією ферменту фосфогліцератфосфомутази (фосфогліце- ромутази) 3-фосфогліцеролова кислота перетворюється (ізомеризується) на 2-фосфогліцеролову кислоту (макроергічну сполуку), що потім під дією ферменту енолази дегідруеться й переходить в енольну форму 2-фосфопіровиноградної кислоти.
Остання взаємодіє з АДФ, при ньому утворюються АТФ і піровиноградна кислота (ПВК):

 Якщо до моменту утворення пірувата в тканині не надійде достатньоїкількості Оксигену, то ПВК відновлюється до лактату (молочна кислота) за участі відновленого НАД (НАДН2). Унаслідок окисного декарбоксилюванняпірувату утворюється лактат.
Якщо до моменту утворення пірувата в тканині не надійде достатньоїкількості Оксигену, то ПВК відновлюється до лактату (молочна кислота) за участі відновленого НАД (НАДН2). Унаслідок окисного декарбоксилюванняпірувату утворюється лактат.
В анаеробних умовах 85% лактату відновлюється до глікогену, а 15% окиснюється до С02 і Н20. Таким чином, лактат є кінцевим продуктом анаеробного окислення глюкози. В аеробних умовах лактат знову перетворюється на піруват або використовується для біосинтезу глюкози в печінці. Цей процес відбува ється в цитоплазмі, де локалізовані всі ферменти гліколізу.
При активній роботі м’язів у них накопичується багато молоч ної кислоти, що викликає їхнє стомлення. ІЦоб відновити дрл нездатність м’язів, необхідно звільнити їх від молочної кисло ти, що досягається виведенням її в кров, з якої вона надходить у печінку. Ваеробних умовах молочна кислота перетворюється на глюкозу, що знову з кров’ю надходить у м’язи й включається з обмінні процеси.
Біологічне значення процесу гліколізу полягає насамперед в утворенні багатих на енергію фосфорних сполук. На перших етапах гліколізу витрачаються дві молекули АТФ (гексозна і фосфофруктокіназна реакції). На наступних етапах утворюються чотири молекули АТФ(фосфогліцераткіназна і піруваткіназна реакції). Крім того, утворюється дві молекули НАДН2, колена з яких при біологічному окиснюванні на мітохондріях виділяє три молекули АТФ. Таким чином, у результаті гліколізу з однієї молекули глюкози утворються вісім молекул АТФ.
Значення гліколізу визначається також і тим, що в ході відповідних реакцій утворюються речовини, які необхідні для біосинтезу деяких життєво важливих сполук. Так, наприклад, фосфодіоксиацетон використовується для біосинтезу простих і складних ліпідів.
Таким чином, саме гліколіз готує «напівфабрикати», які надалі окиснюються до СО2 і Н2О в аеробних умовах.
Лекція 18
Аеробне окислення вуглеводів. Цикл Кребса
[ 1.с. 383-392]
Клітини, які недостатньо забезпечуються Оксигеном, можуть частково або повністю існувати завдяки енергії гліколізу.
В аеробних умовах перетворення лактату, що утворився з глюкози в процесі гліколізу, відбувається у двох напрямах: близько 1/5 лактату окиснюється до CO2, і Н2О інша кількість перетворюється на глікоген.
Перший етап аеробного розпаду лактату - його окиснення до пірувату за участі лактатдегідрогенази.
Однак перевалена більшість тваринних і рослинних клітин у нормі перебуває в аеробних умовах, і піруват, що утворюється при розщепленні глюкози, не відновлюється до лактату, а поступово окиснюється до CO2 і Н2О на аеробній стадії катаболізму. При цьому спочатку відбувається окисне декарбоксилювання пірувату з утворенням ацетил-КоА.
Окисне декарбоксилювання відбувається на мітохондріях. Воно каталізується складними поліферментними і полікофер- ментними системами, які складаються з кількох ферментів (власне дегідрогенази та ін.) і кількох коферментів, у тому числі тіа- мінпірофосфату (ТПФ), тіаміндифосфату (ТДФ), ліпоєвої кислоти (ЛК), НАД, HSKoA, ФАД, Mg2+ (рис. 11.4).
Кожен компонент ферментної системи бере участь у здійсненні відповідної ланки процесу. Реакції відбуваються в кілька етапів.

Цикл трикарбонових кислот (цикл Кребса)
У ході аеробного окиснення вуглеводів піровиноградна кислота зазнає окисного декарбоксилювання з утворенням ацетил-КоА.

Ацетил-КоА, що утворився, вступає в різні реакції обміну й окиснюється до CO2 і Н2О. Повне окиснення ацетил-КоА відбувається в циклі трикарбонових кислот - циклі Кребса.
До 70% ПВК окиснюється до СО2 і Н2О через стадію утворення ацетил-КоА. При обміні білків, жирів і вуглеводів протягом доби на кожен 1 кг маси тіла утворюється близько 10 г ацетату.
Цикл Кребса є центром, де сходяться всі метаболічні шляхи, він — загальний кінцевий шлях окиснення ацетильних груп (у вигляді ацетил-КоА), у які перетворюється в процесі катаболізму більша частина органічних молекул, що відіграють роль «клітинного палива» - вуглеводів, жирних кислот, амінокислот.
Він відбувається в матриксі мітохондрій і складається з восьми послідовних реакцій.
Перша реакція каталізується цитрат-синтетазою, при цьому ацетил-КоА конденсується із щавлевооцтовою кислотою (оксалоацетатом), унаслідок чого утворюється лимонна кислота (цитрат).
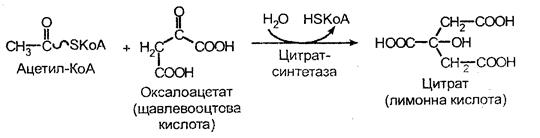
 У другій реакції лимонна кислота піддається дегідруванню з утворенням цисаконітової кислоти, що, приєднуючи молекулу води, переходить в ізолимонну кислоту (ізоцитрат):
У другій реакції лимонна кислота піддається дегідруванню з утворенням цисаконітової кислоти, що, приєднуючи молекулу води, переходить в ізолимонну кислоту (ізоцитрат):
Третя реакція: ізолимонна кислота окиснюється шляхом відщеплення двох атомів Гідрогену й перетворюється на щавлевобурштинову кислоту, що декарбоксилюється до а-кетоглутарової кислоти (а-кетаглутарат).
Четверта реакція: а-кетоглутарова кислота піддається окисному декарбоксилюванню під дією складних ферментів. До складу цих ферментів входять коферменти (ТПФ, HSKoA, ліпоєва кислота, НАД, ФАД). Для реакції необхідні також іони Mg2+. У результаті окисного декарбоксилювання а-кетоглутарової кислоти утворюється сукциніл-КоА, що має макроергічний карбокси- лтіоловий зв’язок, у якому резервується енергія окисного декарбоксилювання. При цьому виділяється друга молекула СО2 і НАДН2.
|
|