
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Постулаты Бора
|
|
В 1913 г. Нильс Бор предложил новую теорию излучения, в которой ему удалось согласовать теорию атома Резерфорда с эмпирической формулой Бальмера.
В основу теории Бора положены следующие три постулата:
1. При движении электрона вокруг ядра атома возможны только те орбиты, для которых момент количества движения электрона кратен 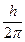 . Математически это записывается равенством:
. Математически это записывается равенством:
mur = n 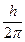
| (6) |
где m – масса электрона; u – скорость электрона;
r – радиус орбиты; n – целое число 1, 2, 3, 4.......
h – постоянная Планка.
Орбиты, удовлетворяющие указанному условию, называется в о з м о ж н ы м и или стационарными. Число n называют г л а в н ы м квантовым числом.
2. Второй постулат утверждает: когда электрон движется по одной из возможных круговых орбит – атом не излучает.
Все попытки как–нибудь логически обосновать этот постулат оказались тщетным.
3. Если электрон под каким–либо воздействием переходит с орбиты, близкой к ядру на какую–либо другую более удаленную, то энергия атома увеличивается, на что требуется затрата внешней энергии. Но такое возбужденное состояние атома малоустойчиво и электрон падает обратно по направлению к ядру на более близкую возможную орбиту.
Третий постулат Бора утверждает: когда электрон перескакивает /падает/ с одной орбиты на другую, лежащую ближе к ядру атома, то потерянная атомом энергия переходит в один квант лучистой энергии, испускаемой атомом.
Положим, что электрон упадет с n2–ой орбиты на n1 –тую. Тогда потерянная энергия определяется равенством:
En1 – En2 = h n или n = 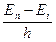 , ,
| (7) |
где En2 и En1 – энергия атома при положении электрона на n2–ой и n1 –ой орбите; n – частота излучения. Это так называемое условие частот Бора.
Квантовая теория Бора строения атома сыграла важную роль в развитии физики. Количественно и весьма наглядно объяснив строение атома, она наметила правильный подход к изучению внутриатомных процессов.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Но использовать теорию Бора для расчета спектров многоэлектронных атомов оказалось невозможным. Ограниченность квантовой теории Бора обусловлена тем, что базируясь на к в а н т о в ы х исходных положениях, она пользуется законами к л а с с и ч е с к о й механики для описания движений электронов в атоме.
В современной же квантовой механике движение электронов в атоме характеризуется не одним, а четырьмя квантовыми числами. Да и сам электрон не считается сосредоточенным в одном месте, а рассматривается как электронное облако переменной плотности, причем плотность облака в любой точке объема атома пропорциональна в е р о я т н о с т и нахождения электрона в этой точке. Но законы, установленные квантовой механикой, уже не обладают той простотой и наглядностью, которая свойственна теории Бора.
|
|
