
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Газовые законы
|
|
Многие вещества (например, кислород, азот, водород и др.) существуют в газообразном состоянии. Газы подчиняются определенным законам.
Закон Бойля-Мариотта: pV = const.
Закон Гей-Люссака:  - (при постоянном давлении) и
- (при постоянном давлении) и  – (при постоянном объеме ).
– (при постоянном объеме ).
Сочетание обоих законов находит свое выражение в уравнении Клапейрона:
 (1.3)
(1.3)
(Этим выражением пользуются для приведения объемов газов от одних условий температуры и давления к другим).
На основе этих газовых законов и своих наблюдений Авогадро сформулировал закон (1811): в равных объемах различных газов при одинаковых условиях содержится одинаковое число молекул.
Если взять 1 моль любого газа, то легко убедиться взвешиванием или измерением объемов, что при нормальных условиях он займет объем 22, 4 л. Это так называемый мольный объем газа.
Нормальные условия (н.у) в Международной системе единиц (СИ): давление 1, 013∙ 105 Па (760 мм рт.ст. = 1 атм.); температура 273 К (0 оС).
Если условия отличаются от нормальных, мольный объём имеет другое значение, для расчетов которого можно воспользоваться уравнением Менделеева-Клапейрона:
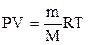 , (1.4)
, (1.4)
где Р - давление газа, V - объем, m - масса газа, М - молярная масса, Т - температура (К), R - универсальная (молярная) газовая постоянная, численное выражение которой зависит от единиц, определяющих объем газа и его давление. В Международной системе измерений (СИ):
R = 8, 314  (
(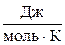 ).
).
Для внесистемных единиц измерения давления и объема величина R имеет значения:
R = 62400 мм рт.ст.× мл / моль∙ К; R = 0, 082 атм∙ л / моль∙ К;
R = 1, 99 кал / моль·К.
Эти законы сыграли большую роль в установлении атомно-молекулярного строения газов и в настоящее время широко используются для расчетов количеств реагирующих газов.
Пример 4. Найти массу 200 л хлора при н.у.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Решение. 1 моль газообразного хлора (Сl2) имеет массу 71 г и занимает объем 22, 4 л. Составляем пропорцию: 71 г - 22, 4 л
Х г - 200 л.
Отсюда Х = 200∙ 71/ 22, 4 = 633, 2 г.
Пример 5. При 25 оС и давлении 99, 3 кПа некоторое количество газа занимает объем 152 мл. Найти, какой объем займет это же количество газа при 0 оС и давлении
101, 33 кПа?
Решение: Подставляя данные задачи в уравнение (1.3), получаем:
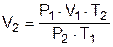 =
=  = 136, 5 мл.
= 136, 5 мл. 
|
|
