
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Ентропія. Ентропія ідеального газу
|
|
Формулу коефіцієнта корисної дії ідеальної теплової машини, що працює за циклом Карно,
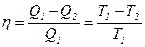
приведемо до вигляду
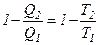 і
і 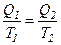 .
.
Відношення кількості переданої
теплоти до температури тепловіддавача або теплоприймача 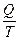 називається зведеною кількістю теплоти.
називається зведеною кількістю теплоти.
У випадку необоротної теплової машини
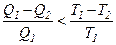 і
і 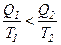 .
.
Тоді, об’єднавши формули для оборотної і необоротної теплових машин, маємо:
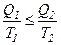 і
і 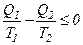 .
.
Умовимося кількість теплоти, яка віддана тілу нагрівником, вважати додатною, а кількість теплоти, віддану тілом холодильнику, – від’ємною. Тоді
 ,
,
причому „ = ” – відповідає оборотним переходам, а „ < ” – необоротним.
В загальному вигляді
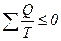 .
.
Функція стану, диференціал якої є 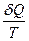 , називається ентропією S.
, називається ентропією S.
Згідно з визначенням зміна ентропії при оборотному процесі
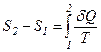 .
.
Ця формула визначає ентропію лише з точністю до адитивної сталої, тобто початок відліку ентропії довільний.
Кожний стан тіла характеризується певним значенням ентропії S, яка є повним диференціалом.
Ентропія – адитивна функція стану системи: ентропія системи дорівнює сумі ентропій всіх тіл, що входять в систему.
ентропію можна розглядати як міру знецінення енергії тіла.
Ентропія – міра теплової непрацездатності тіла.
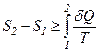 .
.
Для оборотного рівноважного циклу зміна ентропії
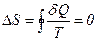 .
.
Якщо система виконує необоротний цикл, то ентропія системи зростає: 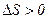 .
.
Ентропія замкненої системи при будь-яких процесах, що в ній відбуваються, не може зменшуватися: 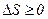 .
.
Знайдемо зміну ентропії у процесах ідеального газу:
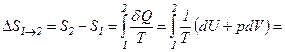
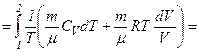
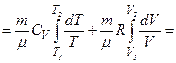
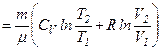 .
.
Зміна ентропії 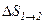 ідеального газу при переході його із стану
ідеального газу при переході його із стану 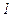 у стан
у стан 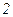 не залежить від виду процесу переходу
не залежить від виду процесу переходу 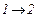 .
.
При адіабатному процесі
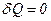 і
і 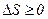 .
.
Для оборотного адіабатного процесу зміна ентропії дорівнює 0, для необоротного 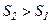 – ентропія тіла зростає.
– ентропія тіла зростає.
Оборотний адіабатний процес – ізоентропічний процес.
При ізотермічному процесі
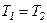 і
і 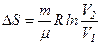 ,
,
при ізохоричному процесі
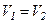 і
і 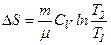 .
.
Розглянемо, як змінюється ентропія при деяких термодинамічних процесах.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
На нагрівання тіла від температури 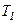 до температури
до температури 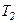 витрачається кількість теплоти
витрачається кількість теплоти
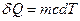 .
.
Тоді
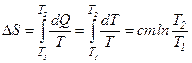 .
.
В процесі теплообміну кількість теплоти  переходить від тіла з більш високою температурою
переходить від тіла з більш високою температурою 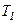 до тіла з більш низькою температурою
до тіла з більш низькою температурою 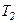 . Ентропія системи, що складається з цих двох тіл змінюється на величину
. Ентропія системи, що складається з цих двох тіл змінюється на величину
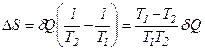 .
.
Оскільки 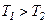 , то ентропія при теплообміні зростає.
, то ентропія при теплообміні зростає.
|
|
