
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Для будь-якого зворотного ідеального циклу зміна ентропії (інтеграл Клаузиса) буде рівним нулю
|
|
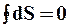 .
.
Із рівняння видно, що для зворотного термодинамічного процесу кількість теплоти, підведеної до РТ, визначається залежністю
Q = Т ·Δ S, кДж/кг× гр,
де Δ S – зміна ентропії, що може бути визначена за формулою
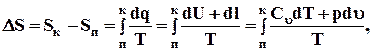
Δ S = Сmυ ln(Тк/Тп) +R ln(υ к/υ п), кДж/кг× гр
де індекси к і п означають відповідно початок та кінець процесу.
Реальні технічні процеси не є зворотними. Для повернення РТ у вихідний стан і повторного здійснення циклу необхідно витратити зовнішню роботу. І якщо теплота Δ q1 передається від гарячого джерела до робочого тіла при температурі Т1 і не відновлюється, ентропія РТ або системи після такого процесу збільшується на величинуΔ q1/Т1.
Таким чином, у незворотних реальних технічних процесах ізольованої системи ентропія буде збільшуватись і зміна ентропії буде більшою за кількість теплоти, що підводиться до робочого тіла, поділену на абсолютну температуру тіла
Δ S > Δ q/Т.
Енергія системи при цьому зменшується за рахунок її розсіювання. Працездатність системи падає на величину
Δ l =Т2 Δ S.
Таким чином, у всіх реальних незворотних процесах розширення робочого тіла, одержання роботи, передачі теплоти, тертя, дифузії тощо збільшується ентропія. Це плата за одержання роботи чи теплоти. Ентропія ізольованої системи збільшується до такого стану, коли ентропія досягне максимального значення, а сама система прийде в стан термодинамічної рівноваги, коли в ній припиняться всі незворотні процеси.
Якщо в початковій точці процесу прийняти нормальні умови (Тп=273 °К, ρ п= 101, 3 кПа, υ п=1/ρ п , ρ п = μ /22, 4), то величину ентропії для будь-якого стану
робочого тіла з параметрами Рк, υ к, Тк можна визначити за формулою
Sк =Сmυ × ln(Тк/273) +R× ln(υ к/υ п) =Сmυ × ln(Тк/273) +R× ln(Рп/Рк), кДж/кг× гр.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
|
|
