
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
III Водорастворимые 3 страница
|
|
Коферменты фолацина участвуют в биосинтезе 2-го н 8-го углеродны* атомов пуриноаого кольца, а также в образовании дТМФ из дУМФ. Поэтому фолацин играет исключительную роль в биосинтезе нуклеиновых кислот и процессах деления клеток.
Недостаточность фолацина. Недостаточное поступление фолиевой кислоты с пищей или нарушение ее всасывания приводит к развитию мегалоблас тической анемии. Причиной ее служит нарушение биосинтеза пуриновых оснований и дезокснтимидинфосфата, что вызывает угнетение синтеза ДНК и пролиферации (деления) кроветворных клеток. При этой анемии наблюдается снижение -количества эритроцитов и гемоглобина в крови; в периферической крови и костном мозге появляются крупные клетки — мегалобласты Имеет место снижение количества лейкоцитов (лейкопения), так как для их образования в костном мозге также необходим нормальный синтез-ДНК.
Практическое применение. В медицинской практике используются препараты фолиевой кислоты для лечения мегалобластической анемии, стимуляции пролиферации клеток и т. д.
Кобаламины (витамин В, 2) Кобаламины поступают в организм человека с пищевыми продуктами. Богаты ими печень, почки. Растительные продукты бедны кобаламинами. Частично витамин В, 2 образуется кишечными бактериями. Суточная потребность в витамине В12 взрослого человека составляет около 2 мкг.
Метаболизм. Для всасывания кобаламинов необходим внутренний фактор, или фактор Кастла, который продуцируется обкладочными клетками желудка. Он представляет собой гликопротеид с молекулярной массой около 93 000. Всасывание кобаламинов включает следующие стадии:
1) образование комплекса витамин В]2 + внутренний фактор;
2) связывание комплекса с эпителием слизистой подвздошной кишки с участием ирнов Са2+ (очевидно, имеются мембранные рецепторы для этого комплекса в слизистой подвздошной кишки);
3) транспорт комплекса витамин В, 2 + внутренний фактор- через слизистую путем эндоцитоза;
4) освобождение витамина Bj2 в кровь воротной вены■ (при этом судьба внутреннего фактора неясна: он либо гидролнзуется, либо возвращается в просвет кишечника).
При поступлении больших не физиологических количеств витамина Bis он может всасываться путем пассивной диффузии в тонком кишечнике без участия внутреннего фактора. Но этот процесс медленный.
Используемый в медицинской практике цианкобаламин превращается в гидроксикобаламин ОН-В]2, который является транспортной формой ко- баламина. Гидроксикобаламин транспортируется кровью с помощью двух специфических плазменных белков: транскобаламина I (TK-I) и траяскобала- мина II (ТК-П), TK-I относится к фракции а-глобулннов. Его молекулярная масса около 120 000. ТК-П относится к |}-глобул и нам. Его молекулярная масса 35 000. ТК-П—основной транспортный белок, облегчающий доставку кобаламинов к тканям, a TK-I служит для поддержания концентрации кобаламинов в крови (своеобразное циркулирующее депо витамина В! 2).
В тканях ОН-В12 превращается в коферментные формы — метилкобала• мин (метил-В]2) и дезоксиаденозилкобаламин (ДА-В, 2). Образование кофер ментов происходит главным образом в печени и почках, а затем распределяется по остальным органам. Выводится кобаламин преимущественно с мочой.
Биохимические функции." Пока известно, что коферменты витамина В|2 участвуют 8 двух ферментативных реакциях. Метил-В12 является коферментом гомоцистеинметилтрансферазы, участвующей в переносе метила с Ы5-метил-ТГФК на гомоцнстеин с образованием метионина. В этой реакции кобаламин действует как синергист с ТГФК.
ДА-В, г является коферментом метилмалонил-КоА-мутазы, катализирующей превращение метилмалонил-КоА в сукцинил-КоА. Эта реакция необходима для сгорания в цикле Кребса остатков пропионил-КоА, образующихся при {3-окислении жирных кислот с нечетным числом углеродных атомов, при окислении боковой цепи холестерина и углеродных радикалов ряда аминокислот (метионина, чзо-пейциня, тпепниня, иалина), а также при окислении тимина.
Хотя окончательно не расшифрованы другие стороны механизма действия кобаламинов в биохимических процессах, несомненно, что кобаламины облегчают депонирование и образование коферментных форм фолиевой кислоты и тем самым посредством коферментов фолиевой кислоты участвуют в синтезе ДНК и пролиферации кроветворных клеток.
Недостаточность кобаламинов. Недостаточность кобаламинов возникает вследствие дефицита их в пище, нарушении всасывания (например, при оперативном удалении желудка или той его части, где образуется внутренний фактор). Недостаточность кобаламинов проявляется в виде мегалобласти- ческой анемии или анемии Адиссон — Бирмера. Нарушение кроветворения выражается теми же признаками, что и при недостатке фолиевой кислоты Отмечаются поражения задних и боковых столбов спинного мозга (фуни кулярный миелоз), повышенное выделение с мочой метилмалоновой кислоты, которая не усваивается.
Обнаружены врожденные дефекты Обмена кобаламинов, связанные с недостаточным образованием внутреннего фактора, транскабал аминов, дефектом метилмалонил-КоА-мутазы.
Практическое применение. В медицинской практике используют цианко- баламин, а в последнее время дезоксиаденозилкобаламин. Эти препараты применяются при лечении мегалобластической анемии, поражениях спинного мозга и периферических аервов, врожденных нарушениях обмена витамина В[2 и других состояниях. Применение кобаламинов целесообразно в сочетании с фолиевой кислотой н железом, поскольку они необходимы при синтезе гемоглобина в кроветворных клетках.
Аскорбиновая кислота (витамин С)
Свежие фрукты и овощи являются основным источником аскорбиновой кислоты для человека. Особенно богаты ею плоды шиповника. Суточная потребность в ней взрослого человека составляет 50—100 мг. -
Метаболизм. Всасывание аскорбиновой кислоты происходит с помощью простой диффузии на всем протяжении желудочно-кишечного тракта, особенно в тонком кишечнике. В крови она частично связана с белками, частично находится в свободном виде. Поступая в ткани, аскорбиновая кислота задерживается в них, связываясь с белками. Свободная аскорбиновая кислота вступает в окислительно-восстановительные реакции. Больше всего содержится аскорбиновой кислоты (в расчете на единицу массы ткани) в надпочеч
никах, печени, легких. Продуктами окислительного распада аскорбиновой кислоты являются дегидроаскорбиновая, дикетогулоновая, щавелевая и некоторые другие. Свободная аскорбиновая кислота и продукты ее распада выводятся с мочой.
Биохимические функции. Аскорбиновая кислота является донором водорода в окислительно-восстановнтельных ферментативных реакциях. Она обра- зует редокс-пару с дегидроаскорбиновой кислотой:
| О |
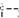
|
Т I о=с о
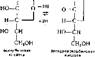
|
| МО—( |
о
Восстановление дегидроаскорбиновой кислоты в аскорбиновую в тканях осуществляется дегидроаскорбинредуктазой с участием восстановительного глутатнона.
Аскорбиновая кислота участвует в следующих процессах биологического окисления:
1) гидроксилирование триптофана в 5-гидрокситриптофан (при биосинтезе серотонина);
2) превращение 3, 4-дигидроксифенилэтиламина в норадреналин;
3) гидроксилирование n-гидроксифенилпирувата в гомогентиэиновую кийлоту;
4) гидроксилирование стероидов при биосинтезе гормонов коры надпочечников из холестерина;
5) гидроксилирование S'-бутиробетаина при биосинтезе карнитина;
6) 'восстановление ионов Fe®+ до Fe2+ в кишечнике, необходимое для всасывания железа в двухвалентном состоянии;
7) освобождение железа чз связи- его с транспортным белком—транс- фернном, что облегчает поступление железа в ткани;
8) превращение фолиевой кислоты в коферментные формы;
9) гидроксилирование остатков пролина и лизина при синтезе коллагена.
Следовательно, аскорбиновая кислота участвует в процессах превращения ароматических аминокислот с образованием некоторых нейромедиаторов, в синтезе кортикостероидов, в процессах кроветворения и в образовании коллагена, являющегося главным внеклеточным компонентом соединительной ткани.
Недостаточность аскорбиновой кислоты. Недостаточность аскорбиновой кислоты приводит к заболеванию, называемого цингой. При тяжелых формах этого заболевания наблюдаются выраженные признаки нарушения биохимических функций аскорбиновой кислоты. Они проявляются в нарушении об
разования коллагена и хондронтинсульфата соединительной ткани, постепенного разрушения ее вследствие деполимеризации и гидролиза волокнистых структур этой ткани. В результате повышается проницаемость и ломкость капилляров и возникают подкожные кровоизлияния. При недостатке витамина С снижается возможность использования запасов железа для синтеза гемоглобина в клетках костного мозга и участия фолиевой кислоты в проли ферации кроветворных клеток. Все это приводит к развитию анемии.
На основе возникших биохимических нарушений развиваются внешние проявления цинги: расшатывание и выпадение зубов, кровоточивость десен, отеки и боли в суставах, бледность (анемичность) кожных покровов, кровоизлияния, поражения костей, нарушение заживления ран.
npaMH.4tA.nOt: Применение. В медицинской практике аскорбиновую кислоту применяют для лечения гиповитаминозов, стимуляции кроветворения вместе с фолиевой кислотой, витамином В]2 и железом, для укрепления капилляров при повышенной их кровоточивости при* различных заболеваниях, стимуляции регенеративных процессов, поражениях соединительной ткани, при острых заболеваниях дыхательных путей и т. д.
5. Битаминоподобные водорастворимые вещества
Биофлавоноиды (витамин Р)
Р-Витаминными веществами богаты свежие фрукты и ягоды, особенно черноплоднан рябина, черная смородина, яблоки, виноград, лимоны, а также листья чая и плоды шиповника. При употреблении их в пищу обеспечивается потребность человека в биофлавоноидах, которая в сутки составляет для взрослого организма 25—50 мг.
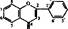
Химическая природа биофлавоноидов. Действующим началом биофлаво- ноидов (Р-витаминных веществ) являются- флавоноиды, представляющие собой растительные полифенольные соединения.
Биофлавоноиды — очень разнообразная группа 1 ■ > ■ з" соединений. В растениях обнаружено до 2000 фла- воноидных веществ и родственных им соединений. Р-Витаминными свойствами обладают антоксан- тнны, антоцианы и катехины.
Метаболизм и биохимические функции. Большинство флавоноидов малотоксичны. В организме человека они превращаются в фенольные кислоты. Выделяются преимущественно с мочой в неизмененном виде или в виде фе- нольных кислот и их конъюгатов с глюкуроновой и серной кислотами В тканях, возможно, ароматическое кольцо биофлавоноидов используется на построение биологических соединений, например убихинона, или они играют самостоятельную роль в обмене веществ.
|
Многие стороны действия биофлавоноидов на метаболизм еще неясны. Наиболее ярко проявляется способность флавококдов снижать проницаемость и ломкость капилляров (капилляроукрепляющее действие). Р-Витаминные вещества взаимодействуют с аскорбиновой кислотой в регуляции образования коллагена соединительной ткани, препятствуют деполимеризации гиалуроновой
кислоты гиалуронидазой. Тем самым флавононды снижают проницаемость капилляров. Р-Витаминные вещества активируют тканевое дыхание.
Недостаток биофлавоноидов. Недостаток в организме биофлавоноидов проявляется симптомами повышенной ломкости и проницаемости капилляров, точечными кровоизлияниями и кровоточивостью десен.
Практическое применение. В медицинской практике применяются комплексные Р-витаминные препараты — сумма катехинов чайного листа, сумма флавоноидов из рябины черноплодной, а также индивидуальные флавононды — рутин, кверцетин, гесперидин и их производные. Используются и комбинированные препараты с витамином С — аскорутин, галаскорбии и катехины чая с аскорбиновой кислотой.
Назначают их при заболеваниях, сопровождающихся повреждением и повышенной проницаемостью стенок капилляров -(капилляротоксикоз, аллергические васкулиты, отравления ядами, лучевая болезнь), также при пониженной свертываемости крови.
Биотин (витамин Н)
Потребность человеческого организма в биотине покрывается в основном за счет биосинтеза его кищечными бактериями. Некоторая часть поступает с пищей. Богаты биотином горох, соя, цветная капуста, грибы, яичный желток, печень и т. д. Суточная потребность взрослого человека в биотине составляет около 150—200 мкг.
Метаболизм и биохимические функции. Поступающий с пищей биотин освобождается с помощью протеиназ кишечника от связи с белками и в свободном виде всасывается в тонком кишечнике. В крови он связывается с альбумином и поступает в ткани. Задерживается биотин главным образом в печени и почках. Выводится в неизмененном виде с мочой и калом.
В тканях свободный биотин ковалентно связывается e-NH2-rpynnoH лизина, находящегося в активном центре «биотиновых» ферментов. Ко- ферментной формой его считается N*-карбоксибиотин. Кофермент биотин а способствует усвоению тканями организма углекислоты (точнее, ионов гидро- карбоната). Он участвует в реакциях карбоксилирования, входя в состав пируваткарбоксилазы, ацетил-КоА-карбоксил азы, пропионил-КоА-карбоксила- зы, а также в других многочисленных реакциях. Тем самым биотин обеспечивает течение глюконеогенеза, синтез жирных кислот, окисление остатков пропионовой кислоты в цикле Кребса.
Биотин образует специфический комплекс с авидином, относящимся к гликопротеидам. Авидина много содержится в белке куриных яиц. Поэтому при употреблении сырых яиц происходит связывание пищевого биотина и всасывание его полностью прекращается (авидин используется в экспериментах для получения биотиновой недостаточности).
Недостаточность би'отнна у человека не выявлена. В медицинской прак тике пока не используются препараты биотина, хотя делаются попытки к его применению при дерматозах.
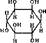
пара-Аминобекзойная кислота (ПАБК) ПАБК содержится практически во всех продуктах питания. Наиболее богаты ею печень, молоко, яниа, дрожжи.
NHj Метаболизм и функции. ПАБК не является вита-
мин ом для человека. Она служит витамином для микро
организмов (возможно, за исключением бактерий туберкулеза, которые сами ее синтезируют) и стимулирует I рост, микроорганизмов. Коферменты ПАБК неизвестны.
СООН Она входит в структуру фолацина, и этим определяется
napj.a-кнобеяаилкая ее значение для жизнедеятельности микроорганизмов, кислота Доказано также, что ПАБК является фактором роста
для птиц и необходима для образования пигмента меланина у грызунов. У человека, возможно, она используется кишечными бактериями для образования фо.лаииня, который и поступает в организм
ческий спирт.
|
В практике ПАБК используется в качестве косметического средства в мазях для " профилактики солнечных ожогов кожи. Возможно, ее необходимо применять для восстановления нормальной микрофлоры кишечника.
Инозит (витамин Bg)
Инозит широко распространен в пище животного и растительного происхождения Наиболее богаты им печень, - мясные продукты, мозг, яичный желток, а также хлеб, картофель, зеленый горох, грибы. Точная потребность в инозите человека неизвестна. Полагают, что она составляет около 1, 0— 1, 5 г в сутки. По химическому строению инозит — шестиатомный цикли-
Метаболизм и функции. Биологической активностью обладает только одна из оптических форм — миоинозит. Инозит входит в состав инозитфосфатидов, содержащихся во всех тканях. Особенно много их в нервной ткани. Участием в построении инозитфосфатидов определяются, по-видимому, биологические функции инозита. Инозит играет роль липотропного фактора (см. «Обмен липидов»). При недостатке его в пище у животных накапливаются триацилглииерины и падает содержание фосфолипидов в печени. Развивается жировая дистрофия печени. Добавление к пище инозита препятствует этим изменениям. Однако липо- тропное действие инозита слабее, чем холина. Лишение инозита вызывает задержку роста молодняка, облысение и анемию-у мышей и крыс; у голубей — на.рушение нервной системы. У человека инозит-авитаминоз не описан.
В практике инозит используется как липотропный препарат, а также для лечения мышечной дистрофии, в косметике его применяют в составе питательных жидкостей для волос.
Оротовая кислота (витамин Ви)
Оротовая кислота широко распространена в животных продуктах.
Метаболизм и функции. Оротовая кислота является предшественником при биосинтезе пиримидиновых оснований (урацила, тимина и цитозина) и нуклеотидов. Биологически активная форма оротата — оротидин-5-фосфат, который включается в синтез нуклеотидов и нуклеиновых кнслот. Благо- 366
О даря этому оротовая кислота стимулирует синтез белка, де-
J\ ление клеток, рост и развитие животных и растений.
НР а Недостаточности оротовой кислоты у человека не бывает,
(УЧ^СООН но повышенная потребность в ней растущего организма или Н отдельных тканей в период регенерации, ' видимо, существует,
оро-саая кислота • в медицинской практике оротовую кислоту применяют
как стимулятор роста недоношенных детей, для усиления процессов кроветворения при некоторых анемиях, для повышения регенеративных процессов в пораженных органах (например, в лечении инфаркта миокарда, дистрофии мышц) и др.
S-Метилметионин (витамин U)
S-Метилметионнн содержится в сырых овощах, особенно много его в капусте. Активное начало капустного сока обладает способностью задерживать развитие экспериментальной язвы желудка, поэтому его назвали антиязвенным фактором или витамином U (от лат. ulcus — язва). Позднее это вещество было выделено в кристаллическом виде. По химическому строению оно является метилированным производным метионина.
Витамин U, как и метнонин, является
| [ |
+ /CHji _ активным донором метильных групп и тем НООС CH—CHj сн2 s\ J С| самым способствует синтезу в тканях 3 организма холина и холинфосфатидов,
витамин U (метил мет я он н н с улъфон и и «о на) КреаТИНЭ Н ДруГИХ ВещеСТВ, СОДерЖЭЩИХ
" оря|1 метильные группы.
Хотя многие стороны действия на обмен веществ витамина U неясны, но он с успехом применяется для лечения язвенной болезни желудка и двенадцатиперстной кишки, гастритов. Возможно липотропное действие этого витамина.
Карнитин (витамин Вт)
Карнитин — широко распространенное вещество, особенно много его в мясных продуктах. Карнитин является истинным витамином для мучного червя, но не дл-т млекопитающих, в тканях которых он синтезируется кз у-бутиро- бетаина, Примерная суточная потребность карнитина для человека составляет 500 мг.
Метаболизм и функции. Биосинтез карнитина происходит в основном в печени. Сначала метилируется лизин белка с образованием e-N-триме- тилизина. Затем укорачивается углеродная цепь лизина за счет потери первого и второго атомов углерода и образуется у-бутиробетаин. В клеточном соке печени с участием у-бутиробетаин-гидроксилазы происходит гидроксилирование у-бутиробетаина с образованием карнитина по схеме
7-Бутиробетаии + Ог-(-2-Оксоглутарат —Карнитин + Сукцинат -j-COz Для протеканий реакции необходимы кислород, 2-оксоглутарат, Fe2+ и аскорбиновая кислота.
Биологически активным является L-карнитин. Карнитин участвует в переносе длинноцепочечных ацилов жирных кислот н ацетильных групп через
липидную фазу мембран митохондрий, а возможно, и других органоидов. Поэтому он оказывает выраженное влияние на процессы окисления жирных кислот и образование из них энергии, а также на использование ацетильных остатков, образующихся в митохондриях, в биохимических реакциях цитоплазмы. Вероятно, имеются и другие стороны действия карнитина. Имеются данные, что карнитнн стимулирует виешнесекреторную функцию поджелудочной железы, оказывает положительный эффект на сперматогенез и подвижность сперматозоидов. Введение кариитина животным повышает образование энергии в дыхательной цепи митохондрий различных органов, стимулирует регенеративные процессы в пораженном миокарде и спермато- генном эпителии канальцев семенников и т. д. (Е. А. Строев, В. Г. Макарова, О. И. Ьазилевич).
Описаны случаи карнитиновой недостаточности, которые проявляются в виде поражения скелетных мышц. У таких людей наблюдается выраженное снижение содержания карнитина в мышцах, сопровождающееся мышечной слабостью, дистрофией и истончением мышечных волокон. Назначение больших количеств карнитина облегчает течение этого заболевания. Дефицит лизина в пище ухудшает обеспеченность организма карнитином.
В медицинской практике карнитин только начинает применяться, поскольку неясны многие стороны его действия. Он используется для стимуляции мышечной деятельности, внешней секреции поджелудочной железы, при дистрофических процессах в миокарде.
Липоевая кислота (витамин N)
Липоевая кислота поступает с пищей. Наиболее богаты ею дрожжи, мясные продукты, молоко. Потребность в ней человека пока не установлена.
Липоевая кислота, поступая в ткани, связывается ковалентно с NH2-rpyn- пой лизина активного центра апоферментов «липоевых» ферментов. К ним относятся полнферментные комплексы окислительного декарбоксилирования пирувата, 2-оксоглутарата и других сикетокислот. Недостаточность липоевой кислоты у человека не описана.
| о |
В медицинской практике используются препараты липоевой кислоты и ее амида при поражениях печени, сахарном диабете, интоксикации тяжелыми металлами и т. д. Считается, что при этом улучшаются окисление метаболитов углеводного обмена и энергетика клеток.
Пангамовая кислота (витамин Bis)
Пангамовая кислота содержится во многих продуктах питания, но потребность в ней человека неизвестна. Химическое строение пангамовой кислоты окончательно не доказано. Считают, что она является N-днметилглициновым эфиром глюконовой кислоты, хотя это соединение нестойкое н легко гидро- лизуется:
онн онон
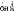
|
| н |
НООС—(I: —6—i-c—CHj—О—C--CH, -N'
" " chs
н
Пангамовая кислота подобно метионину служит источником подвижных метильных групп. Она участвует в биосинтезе метилированных соединений: холина и холинфосфатидов, креатина н др.
В медицинской практике используются препараты пангамовой кислоты как липотропного средства при жировой инфильтрации печени, атеросклерозе и некоторых других заболеваниях, хотя биохимические основы показаний для применения препарата не всегда ясны.
Холин (витамин В4)
Холин поступает в организм человека с пищей. Богаты нм мясо и продукты, получаемые из злаков. Частично холин образуется кишечной микрофлорой. Потребность в нем взрослого человека составляет 250—600 мг в сутки.
Метаболизм и биохимические функции. Всасывание холина происходит в тонком кишечнике путем простой диффузии и, возможно, с помощью активного транспорта при низких концентрациях в кишечнике. В стенке кишечника он фосфорилируется до фосфохолина и участвует в образовании холинофосфатидов. В составе липопротеидов холнн с кровью разносится по тканям. Частично в ткани поступает фосфохолин и небольшие количества свободного холина, где они включаются в обмен веществ.
В клетках холин участвует в синтезе фосфатидов, ацетилхолина и является донором метильных групп при реакциях трансметилирования. У человека недостаточность холина не описана. У экспериментальных животных холиновая недостаточность проявляется в виде жировой инфильтрации печени и других нарушений синтеза липидов.
В медицинской практике используется препарат холина для лечения поражений печени, вызванных различными заболеваниями и интоксикациями.
6. Взаимодействие витаминов
Каждый из витаминов и образующихся из них коферментов контролирует определенную группу биохимических процессов как переносчик активных групп или как регулятор количества определенного фермента в клетках. Между тем возможны взаимодействия разных витаминов в метаболизме, которые отражаются на конечном эффекте каждого из них. Это взаимодействие может выражаться:
1) во влиянии одного витамина на катаболизм другого;
2) во влиянии одного витамина на регуляцию образования кофермент- ной формы другого, а Следовательно, на проявление биохимической функции последнего;
3) в совместном " участии на одной или нескольких стадиях единого биохимического процесса.
В качестве первого типа взаимодействия можно привести, например, взаимодействие между токоферолом и витамином А или эссенциаль- ными жирными кислотами. Токоферол как антиоксидант препятствует перок- сидному окислению витамина А и ненасыщенных жирных кислот, чем повы' шает их биологическую активность и позволяет снизить вводимую лечебную дозу последних. Напротив, полиненасыщенные кислоты повышают потребность в токофероле и могут вызвать признаки недостаточности токоферола.
Введение рибофлавина усиливает катаболизм ниациновых и пиридоксалевых коферментов и увеличивает их недостаточность в организме.
Второй тип взаимодействий проявляется довольно часто. Например, коферменты рибофлавина входят в состав ферментов, катализирующих образование из пиридоксина пиридоксальфосфата. Тем самым они благоприятствуют проявлению биохимических функций пиридоксина. Кобаламины и аскорбиновая кислота способствуют образованию кофермеитной формы фолиевой кислоты и проявлению ее многообразных биохимических функций.
Взаимодействия третьего типа особенно многочисленны. Например, отмечается совместное участие нескольких витаминов (витамина А, рибофлавина, пиридоксина и ниацина)-в образовании и регенерации родопсина, т. е. в биохимическом акте зрения. В этом процессе они проявляют в целом синергетический эффект.
Аналогичный синергизм отмечается в действии фолиевой кислоты, кобаламинов, аскорбиновой кислоты и, вероятно, пиридоксина в биохимическом процессе, ведущем к пролиферации клеток крови. Классическим примером положительного взаимодействия является участие аскорбиновой кислоты и Р-витаминных веществ в образовании соединительной ткани и в регуляции проницаемости капилляров.
Взаимодействие витаминов является основой для нх рационального применения и создания эффективнйх поливитаминных лекарств. В настоящее время созданы поливитаминные препараты, содержащие от двух до десяти витаминов.
7. Антивитамины
Антивитаминами называют аналоги витаминов, действующие как антикоферменты. Антивитамины замещают коферменты, производные витаминов, но не способны выполнять их функции в ферментативных реакциях
Предлагалось называть антивитаминами в широком смысле любые вещества, инактивирующее или ограничивающие действие витаминов в организме. Однако при взаимодействии некоторые витамины могут вызывать дефицит других. Если встать на позиции широкого определения термина «антивитамины», то многие витамины также можно назвать антивитаминами, что неизбежно приведет к путанице понятий.
Специфическое антикоферментное действие антивитаминов позволило широко использовать их в практике для создания экспериментальных авитаминозов у животных н для лечения бактериальных инфекций и опухолевых заболеваний (табл. 32).
ГЛАВА 27. НЕЙРОЭНДОКРИННАЯ РЕГУЛЯЦИЯ
ОБМЕНА ВЕЩЕСТВ. БИОХИМИЧЕСКАЯ
АДАПТАЦИЯ
1. Введение в эндокринологию
В эндокринную систему входят специальные железы, клетки которых выделяют во внутренние среды организма, т. е. в кровь или лимфу, химические •регуляторы, получившие название гормонов. Понятие «гормон» (от греч.
Таблица 32. Антивитамины
|
|
|