
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Обсуждение результатов
|
|
3.1 Результаты синтеза гидрохлорида S, S′ -ди(метилтио)имина
Гидрохлорид S, S′ -ди(метилтио)имина получают при взаимодействии роданистого метила и метилмеркаптана в растворе хлороформа, при пропускании через него сухого хлористого водорода:
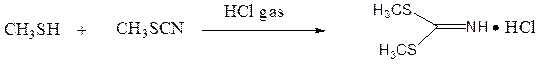
То, что получается гидрохлорид S, S′ -ди(метилтио)имина, подтверждается данными УФ спектроскопии (рисунок 3.1). УФ-спектр гидрохлорида S, S′ -ди(метилтио)имина содержит два пика с длиной волны 238, 0 нм и 261, 0 нм и величиной поглощения 0, 709 и 0, 696, соответственно, при концентрации раствора С=1· 10–4 моль/л. УФ спектр соединения соответствует спектру заведомого образца.
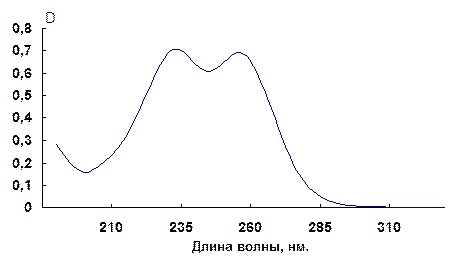
Рисунок 3.1 - УФ-спектр гидрохлорида S, S′ -ди(метилтио)имина.
3.2 Результаты синтеза S, S′ -ди(метилтио)-N-нитроимина
S, S′ -ди(метилтио)-N-нитроимин получают нитрованием гидрохлорида S, S′ -ди(метилтио)имина 98%-ой азотной кислотой в среде уксусного ангидрида:
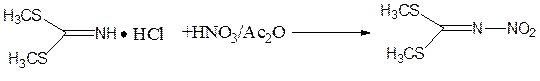
Для увеличения выхода выдержка после дозировки гидрохлорида S, S′ -ди(метилтио)имина производилась в герметично закрытой колбе. Установлено, что повышению выхода способствует препятствие удалению окислов азота из реакционного объема.
Вероятно, механизм нитрования зависит от окислов азота и идет по радикальному механизму, подобно радикальному нитрованию ароматических аминов.
Качество продукта контролировали УФ-спектроскопически. В УФ-спектре водного раствора S, S′ -ди(метилтио)-N-нитроимина наблюдается два пика при длинах волн 210, 0 и 307, 0 нм с величиной поглощения 0, 657 и 1, 513, соответственно (при концентрации раствора 1× 10-4 моль/л). Пик поглощения с длиной волны 307, 0 нм связан с n→ π * переходом в нитроиминной группе (рисунок 3.2)
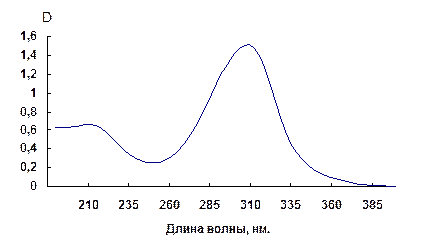
Рисунок 3.2 - УФ-спектр S, S¢ -ди(метилтио)-N-нитроимина
3.3 Результаты изучения реакции взаимодействия S, S′ -ди(метилтио)-N-нитроимина с едким натром, а также с едким калием
Была изучена реакция взаимодействия S, S′ -ди(метилтио)-N-нитроимина с едким натром в водноэтанольном растворе для получения S-метилтио-N-нитрокарбамата, а также натриевой соли S-метилтио-N-нитрокарбамата.
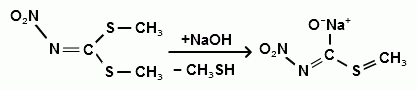
Для получения S-метилтио-N-нитрокарбамата, натриевую соль подкисляли водным 30%-ным раствором соляной кислоты.
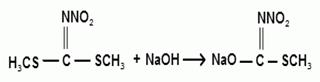
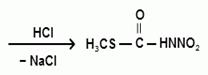
В экспериментах было получено два продукта: карбонат натрия и натриевая соль S-метилтио-N-нитрокарбамата. Возможный механизм реакции:
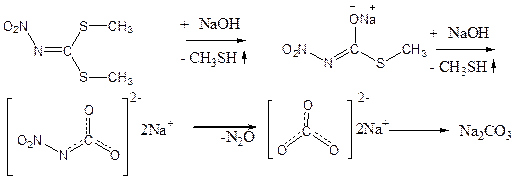
Для разделения смеси «натриевая соль S-метилтио-N-нитрокарбамата – карбонат натрия» использовали безводный ацетон, в котором растворяли натриевую соль S-метилтио-N-нитрокарбамата. Карбонат натрия не растворим в безводном ацетоне. Раствор отфильтровали и упарили, таким образом, мы получили натриевую соль S-метилтио-N-нитрокарбамата.
Аналогичным образом была получена и калиевая соль S-метилтио-N-нитрокарбамата.
Получение данных веществ было подтверждено УФ-спектроскопически. Были взяты УФ-спектры у чистого S-метилтио-N-нитрокарбамата и его солей. Пробы снимались с растворов, имеющих концентрацию С=0, 0001 моль/л, навески растворяли в 1 л и в 0, 5 л дистиллированной воды. Результаты УФ-спектральных анализов представлены в таблице 3.1. Графики УФ-спектров S-метилтио-N-нитрокарбамата и его солей представлены на рисунках 3.3-3.5.
Таблица 3.1 - УФ-спектры S-метилтио-N-нитрокарбамата и его солей
| Вещество | mнавески, мг | Пики максимумов поглощения, длина волны, нм (интенсивность) |
| S-метилтио-N-нитрокарбамат | 13, 6 (на 1 л) | 209, 0 (0, 467); 281, 0 (1, 016) 209, 0 (0, 452); 280, 5 (0, 989) 208, 0 (0, 458); 280, 5 (0, 992) |
| Натриевая соль | 15, 8 (на 1 л) 7, 9 (на 0, 5 л) | 209, 0 (0, 447); 280, 5 (0, 964) 208, 5 (0, 440); 280, 0 (0, 971) 209, 0 (0, 449); 279, 5 (0, 963) |
| Калиевая соль | 8, 7 (на 0, 5 л) 8, 8 (на 1 л) | 207, 0 (0, 464); 280, 5 (0, 936) 207, 0 (0, 468); 281, 0 (0, 966) 207, 0 (0, 473); 281, 0 (0, 979) |
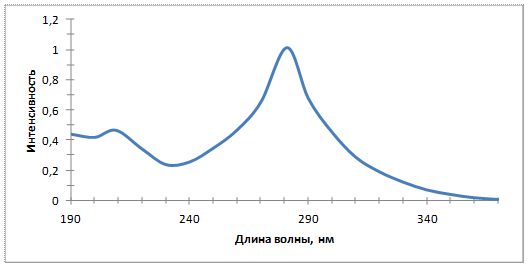
Рисунок 3.3 – УФ-спектр S-метилтио-N-нитрокарбамата
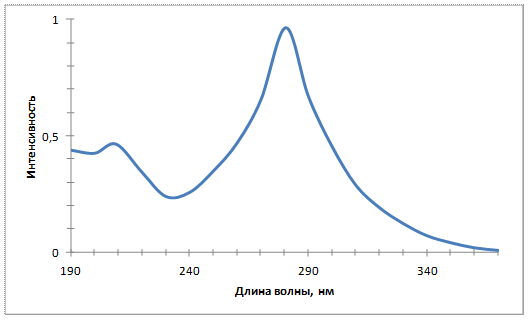
Рисунок 3.4 – УФ-спектр натриевой соли S-метилтио-N-нитрокарбамата
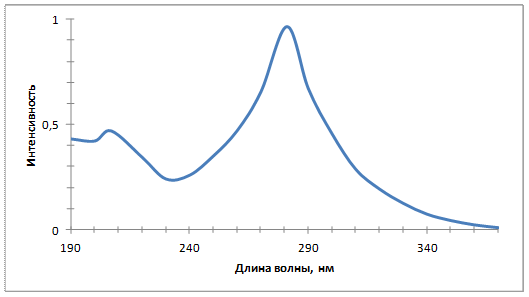
Рисунок 3.5 – УФ-спектр калиевой соли S-метилтио-N-нитрокарбамата
Судя по идентичности УФ-спектров S-метилтио-N-нитрокарбамата и его солей, в спектрах мы наблюдаем пики аниона.
Данные ИК-спектроскопии:
График сравнения ИК-спектров натриевой и калиевой солей S-метилтио-N-нитрокарбамата представлен на рисунке 3.6. Как мы можем видеть из данного рисунка, ИК-спектры этих солей практически идентичны, натриевая и калиевая соли S-метилтио-N-нитрокарбамата имеют схожие анионы, что свидетельствует о схожести их структур. Некоторое отличие мы можем наблюдать во фрагменте –ОН, что указывает нам на то, что натриевая соль более гигроскопична, чем калиевая.
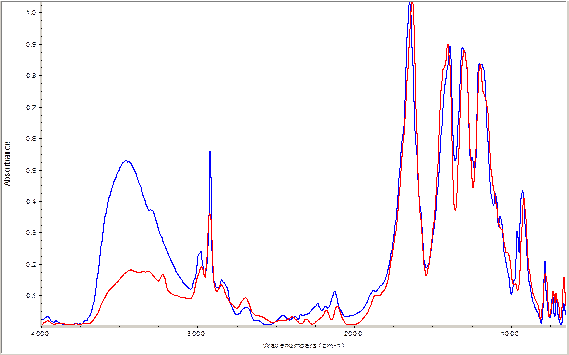
Рисунок 3.6 – График сравнения ИК-спектров калиевой и натриевой солей S-метилтио-N-нитрокарбамата
Получение соответствующих солей S-метилтио-N-нитрокарбамата также подтверждено элементным анализом.
Элементный анализ натриевой соли S-метилтио-N-нитрокарбамата:
| Найдено: | Вычислено: | |
| N, %: 17, 52 | N, %: 17, 72 | |
| C, %: 16, 99 | C, %: 15, 19 | |
| H, %: 2, 25 | H, %: 1, 91 |
Элементный анализ калиевой соли S-метилтио-N-нитрокарбамата:
| Найдено: | Вычислено: | |
| N, %: 15, 67 | N, %: 16, 08 | |
| C, %: 14, 50 | C, %: 13, 79 | |
| H, %: 2, 02 | H, %: 1, 74 |
|
|