
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Антибиотики, действующие на уровне трансляции
|
|
На рис. I.21 приведены некоторые широко распространенные антибиотики, являющиеся ингибиторами биосинтеза белка у бактерий. Многие из них находят применение не только как лекарственные средства, но и как превосходные инструменты исследования механизма различных этапов биосинтеза белка. Биохимический анализ мутантов бактерий, устойчивых к действию конкретных антибиотиков, позволяет обнаруживать сайты действия антибиотиков на рибосомах и идентифицировать изменения компонентов системы белкового синтеза под влиянием этих мутаций. Как правило, для возникновения устойчивости к антибиотику достаточно замены одного аминокислотного остатка из ~7500 остатков белков, составляющих бактериальную рибосому. То же самое относится и к ~4500 основаниям рибосомных РНК. В этом случае не только замены одиночных оснований в рРНК, но и модификация (метилирование) единственного основания могут приводить к подобным эффектам. Рассмотрим механизм действия некоторых антибиотиков более подробно.
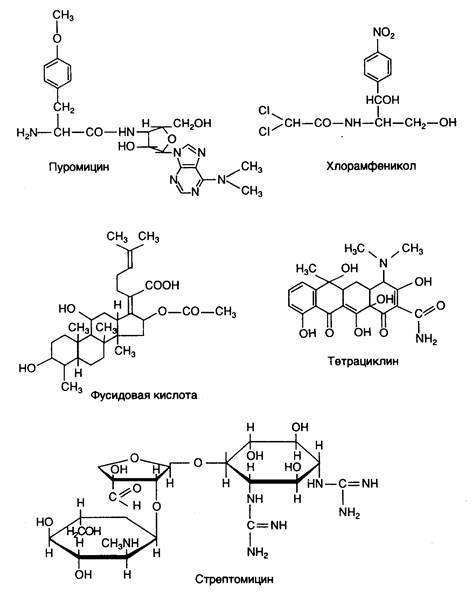
Рис. I.21. Антибиотики – ингибиторы биосинтеза белка у бактерий
Пуромицин. Этот антибиотик представляет собой производное нуклеозидов и является структурным аналогом 3’-концевой аминоацилированной группировки тРНК. Прямыми экспериментами было показано, что пуромицин конкурентным образом замещает очередную аминоацил-тРНК в A-сайте рибосом в процессе трансляции. Он участвует в акте образования пептидной связи в рибосоме, подменяя при этом очередную аминоацил-тРНК. В ходе реакции транспептидации происходит переброска C-конца растущего пептида от пептидил-тРНК на свободную аминогруппу его аминоацильного остатка, что приводит к освобождению пептидил-пуромицина из рибосом и прекращению биосинтеза белка. Пуромицин одинаково хорошо подавляет биосинтез белка как прокариотическими, так и эукариотическими рибосомами.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Хлорамфеникол. Участок лабильного связывания этого антибиотика локализован на 50S субчастице рибосом. Хлорамфеникол полностью ингибирует реакцию пуромицина с пептидил-тРНК, выступая его конкурентным ингибитором. При этом синтез пептида полностью прекращается, и он остается связанным с рибосомами. Предполагают, что хлорамфеникол имитирует аминоацильный конец молекулы аминоацил-тРНК, а его дихлорацетамидная группировка соответствует аминоацилу. Местом действия хлорамфеникола является A-участок 50S субчастицы рибосом, где антибиотик конкурирует с аминоацильным концом молекулы аминоацил-тРНК, препятствуя ее вхождению в A-участок, что сопровождается подавлением биосинтеза белка. В отличие от пуромицина хлорамфеникол ингибирует только бактериальные рибосомы. Сходным механизмом действия обладают антибиотики линкомицин и спарсомицин. Последний делает ассоциацию пептидил-тРНК с P-участком рибосом более прочной. При этом хлорамфеникол и линкомицин способны вытеснять спарсомицин из его комплекса с рибосомами.
Фусидовая кислота – антибиотик стероидной природы, блокирует биосинтез белка на стадии транслокации. Его мишенью является не столько сама рибосома, сколько белковый фактор EF2(EF-G), который, как указывалось выше, необходим для GTP-зависимой транслокации. Фусидовая кислота не влияет на взаимодействие фактора EF2(EF-G) и GTP с пре-транслоцированной рибосомой и последующее расщепление GTP. По-видимому, антибиотик препятствует диссоциации указанного комплекса и сопряженной с ней транслокации. По тому же механизму фусидовая кислота подавляет трансляцию эукариотическими рибосомами.
Тетрациклины. Антибиотики тетрациклинового ряда специфически связываются с 30S субчастицей рибосом, подавляя реакцию аминоацил-тРНК с рибосомами и свободными 30S субчастицами в присутствии матрицы, но не нарушая связывание самого матричного полинуклеотида. Предполагают, что тетрациклины взаимодействуют с акцепторным тРНК-связывающим участком 30S субчастицы рибосом.
Стрептомицин и другие аминогликозидные антибиотики. Стрептомицин (антибиотик углеводной природы) специфически взаимодействует с определенным структурным белком 30S субчастицы рибосом, блокируя стадию инициации трансляции. В присутствии стрептомицина наблюдается стимуляция связывания аминоацил-тРНК, не соответствующих кодонам мРНК, находящимся в данный момент в акцепторном A-участке рибосом. В итоге происходит ошибочное включение аминокислот в полипептидные цепи синтезируемых белков. Это может проявляться в фенотипической супрессии нонсенс-мутаций у мутантных бактерий. Аминогликозидные антибиотики также вызывают неспецифическое связывание матричных полинуклеотидов рибосомами. Следствием является, например трансляция одноцепочечных ДНК рибосомами в бесклеточных системах в присутствии аминогликозидов.
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
|
|
