
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Мышечное сокращение
|
|
Сокращение мышцы происходит при поступлении по аксонам двигательных нейронов к нервно-мышечным синапсам волны возбуждения в виде нервных импульсов (ПД нервных волокон). Это непрямое сокращение (опосредованное нервно-мышечной синаптической передачей). Возможно и прямое сокращение мышцы. Под ним понимают сокращение групп МВ (мышечные подёргивания, фибрилляции), происходящее при возбуждении любого звена последовательности событий после секреции нейромедиатора из терминалей аксона в нервно-мышечном синапсе. Последовательность этих событий такова: (1) деполяризация постсинаптической мембраны и генерация ПД (2) распространение ПД по плазмолемме МВ (3) передача сигнала в триадах на саркоплазматический ретикулум (4) выброс Ca2+ из саркоплазматического ретикулума (5) связывание Ca2+ тропонином С тонких нитей (6) взаимодействие тонких и толстых нитей (формирование мостиков), появление тянущего усилия и скольжение нитей относительно друг друга (7) Цикл взаимодействия нитей (8) укорочение саркомеров и сокращение МВ (9) расслабление. Позиции 1–4 рассмотрены выше (см. рис. 7–4 и 7–5 в книге и сопровождающий их текст), а этапы 2–4 представлены на рис. 7–10.
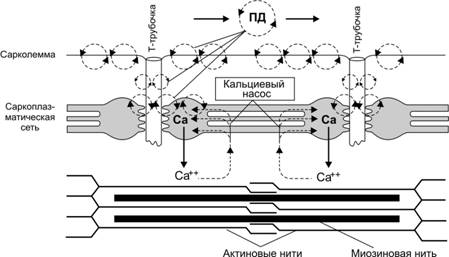
Рис. 7–10. Распространение потенциала действия по сарколемме мышечного волокна и выброс ионов кальция из цистерн саркоплазматического ретикулума
Деполяризация постсинаптической мембраны и генерация ПД рассмотрены выше и в главе 6.
Плазмолемма и потенциал действия. Локальная деполяризация постсинаптической мембраны приводит к генерации потенциала действия, быстро распространяющегося по всей плазмолемме мышечного волокна (включая Т-трубочки).
Электромиография — важный диагностический метод — позволяет регистрировать характеристики потенциалов действия.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Миотония. Уменьшение Cl—-проводимости плазмолеммы ведёт к электрической нестабильности мембраны МВ и к развитию миотонии (например, болезни Томсена).
Триады и передача сигнала на саркоплазматическую сеть. Волна деполяризации по Т-трубочкам проникает до триад. В области триад мембрана Т–трубочек в составе потенциалозависимого кальциевого канала содержит рецепторы дигидропиридина. Деполяризация мембраны Т–трубочек вызывает в структуре рецепторов дигидропиридина конформационные изменения, передающиеся на рецепторы рианодина терминальных цистерн саркоплазматического ретикулума.
Злокачественная гипертермия при наркозе (особенно при использовании тиопентала и галотана) — редкое осложнение (смертность до 70%) при хирургическом вмешательстве. Температура тела быстро поднимается до 43 °С и выше, происходит генерализованный распад мышц (рабдомиолиз). В части случаев найдена мутация гена рианодинового рецептора скелетномышечного типа.
4. Саркоплазматический ретикулум и выброс Ca2+. Активация рецепторов рианодина (Ca2+‑ канал) приводит к открытию Ca2+‑ каналов, Ca2+ из кальциевых депо поступает в саркоплазму; концентрация Ca2+ в саркоплазме достигает значений, достаточных для связывания этого двухвалентного катиона с тропонином С тонких нитей.
5. Связывание Ca2+ тонкими нитями. В покое взаимодействие тонких и толстых нитей невозможно, т.к. миозин-связывающие участки F‑ актина заблокированы тропомиозином. При высокой концентрации Ca2+ эти ионы связываются с тропонином C и вызывают конформационные изменения тропомиозина, приводящие к разблокированию миозин-связывающих участков (рис. 7–11).

Рис. 7–11. Ca2+–зависимый механизм регуляции взаимодействия актина с миозином [11]. В покое миозин-связывающие участки тонкой нити заняты тропомиозином. При сокращении ионы Ca2+ связываются с тропонином С, а тропомиозин открывает миозин-связывающие участки. Головки миозина присоединяются к тонкой нити и вызывают её смещение относительно толстой нити.
6. Взаимодействие тонких и толстых нитей. В результате разблокирования миозин-связывающих участков молекул актина головки миозина, несущие продукты гидролиза АТФ (АДФ + Фн), присоединяются к тонкой нити и изменяют свою конформацию, создавая тянущее усилие: — тонкие нити начинают скользить между толстыми (рис. 7–12). За счёт шарнирного участка в области шейки миозина происходит гребковое движение, продвигающее тонкую нить к центру сaркомера. В результате происходит скольжение тонких нитей относительно толстых. Затем головка миозина связывается с молекулой АТФ, что приводит к отделению миозина от актина. Последующий гидролиз АТФ восстанавливает конформированную молекулу миозина, готовую вступить в новый цикл. Такая модель скользящих нитей была предложена Хью Хаксли.
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
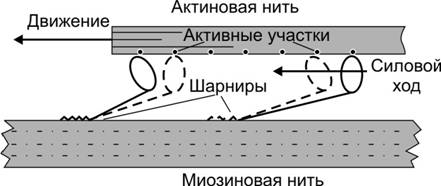
Рис. 7–12. Взаимодействие головки миозина с тонкой нитью и появление тянущего усилия
7. Рабочий цикл. Каждый цикл взаимодействия тонких и толстых нитей имеет несколько стадий (рис. 7–13).
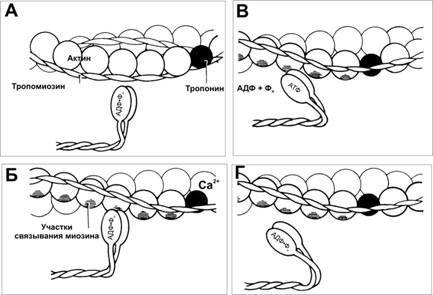
Рис. 7–13. Цикл взаимодействия тонких и толстых нитей [5]. (А) Исходное положение: головка миозина выстоит над толстой нитью (не показана). (Б) Благодаря наличию шарнира между тяжёлым и лёгким меромиозинами, несущая АДФ и Pi головка миозина прикрепляется к актину, происходит поворот головки миозина с одновременным растягиванием эластического компонента S2. (В). Из головки освобождаются АДФ и Фн, а последующая ретракция эластического компонента S2 вызывает тянущее усилие. Затем к головке миозина присоединяется новая молекула АТФ, что приводит к отделению головки миозина от молекулы актина (Г). Гидролиз АТФ возвращает молекулу миозина в исходное положение (А).
Укорочение саркомера и сокращение мышечного волокна. Головка миозина совершает около пяти циклов в секунду. Когда одни головки миозина толстой нити производят тянущее усилие, другие в это время свободны и готовы вступить в очередной цикл. Следующие друг за другом гребковые движения подтягивают тонкие нити к центру сaркомера. Скользящие тонкие нити тянут за собой Z-линии, вызывая сокращение сaркомера. Поскольку в процесс сокращения практически одномоментно вовлечены все саркомеры МВ, происходит его укорочение.
9. Расслабление. Ca2+‑ АТФаза сaркоплазматического ретикулума закачивает Ca2+ из сaркоплазмы в цистерны ретикулума, где Ca2+ связывается с кальсеквестрином. В условиях понижения концентрации Ca2+ в саркоплазме тропомиозин закрывает миозин-связывающие участки и препятствует их взаимодействию с миозином. После смерти, когда содержание АТФ в мышечных волокнах снижается вследствие прекращения её синтеза, головки миозина оказываются устойчиво прикреплёнными к тонкой нити. Это состояние трупного окоченения (rigor mortis) продолжается, пока не наступит аутолиз, после чего мышцы можно растянуть.
Ca2+‑ насос — основа активного процесса расслабления. Ионы кальция, высвобожденные из саркоплазматического ретикулума и диффундировавшие к миофибриллам, вызывают сокращение, которое будет продолжаться столь долго, сколь долго высокая концентрация ионов Ca2+ будет сохраняться в саркоплазме. Этому препятствует постоянная активность Ca2+ насоса, расположенного в стенках саркоплазматического ретикулума и откачивающего с затратой энергии ионы Ca2+ обратно в просвет саркоплазматического ретикулума. Ca2+ насос повышает концентрацию Ca2+ внутри трубочек в 10 000 раз. Дополнительно работе насоса способствует специальный белок кальсеквестрин, связывающий в 40 раз больше ионов Ca2+, чем их находится в ионизированном состоянии. Таким образом, обеспечивается 40-кратное увеличение запасов кальция. Массивное перемещение ионов Ca2+ внутрь саркоплазматического ретикулума уменьшает концентрацию Ca2+ в саркоплазме до величины 10-7 М и менее. Поэтому, за исключением периода ПД и немедленно сразу после его окончания, концентрация ионов Ca2+- в саркоплазме поддерживается на исключительно низком уровне, и мышца остаётся расслабленной.
Таким образом, при сокращении МВ практически одновременно регистрируются следующие важные характеристики: генерация ПД, выброс ионов кальция в саркоплазму и собственно сокращение (рис. 7–15)
Энергетические потребности. Мышечное сокращение требует значительных энергетических затрат. Основной источник энергии — гидролиз макроэрга АТФ. В митохондриях в процессе цикла трикарбоновых кислот и окислительного фосфорилирования генерируется АТФ. Гликоген запасaется в сaркоплазме в виде включений. Анаэробный гликолиз сопряжён с синтезом АТФ. Креатинфосфокиназа, связанная в области М-линии, катализирует перенос фосфата от фосфокреатина на АДФ с образованием креатина и АТФ. Миоглобин, как и Hb, обратимо связывает кислород. Запасы кислорода необходимы для синтеза АТФ при длительной непрерывной работе мышцы. На один рабочий цикл затрачивается 1 молекула АТФ. В МВ концентрация АТФ равна 4 ммоль/л. Такого запаса энергии достаточно для поддержания сокращения не более 1–2 сек.
Затраты АТФ. Энергия АТФ расходуется на:
образование поперечных мостиков, осуществляющих продольное скольжение актиновых филаментов (основная часть энергии гидролиза АТФ);
Ca2+-насос: выкачивание Ca2+ из саркоплазмы в саркоплазматический ретикулум после окончания сокращения;
Na+/K+-насос: перемещение ионов натрия и калия через мембрану МВ для обеспечения соответствующего ионного состава вне- и внутриклеточной среды.
|
|
