
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
⚡️ Для новых пользователей первый месяц бесплатно. А далее 290 руб/мес, это в 3 раза дешевле аналогов. За эту цену доступен весь функционал: напоминание о визитах, чаевые, предоплаты, общение с клиентами, переносы записей и так далее.
✅ Уйма гибких настроек, которые помогут вам зарабатывать больше и забыть про чувство «что-то мне нужно было сделать».
Сомневаетесь? нажмите на текст, запустите чат-бота и убедитесь во всем сами!
Основные понятия радиационной безопасности. 3. 1. Явление радиоактивности и естественная радиоактивность были открыты в мае 1896 г
|
|
 А. Беккерель
(1852-1908) А. Беккерель
(1852-1908)
|  В. К. Рентген
(1845 - 1923)
В. К. Рентген
(1845 - 1923)
|
3.1. Явление радиоактивности и естественная радиоактивность были открыты в мае 1896 г. французским ученым физиком Анри Беккерелем. За пол года до этого открытия (8 ноября 1895 г.) вюрцбургский (немецкий) физик Вильгельм Конрад Рентген открыл излучение (Х-лучи), обладающее большой энергией и проникающей способностью. Оно известно сегодня как рентгеновские лучи, которые возникают тогда, когда катодные лучи (электроны), испускаемые отрицательным электродом (катодом) электронно-вакуумной лампы, ударяют в другую часть лампы во время высоковольтного разряда. Анри Беккерель провел опыты с чистым ураном и обнаружил, почернение фотографической пластинки. Загадочное излучение, которое совершенно очевидно являлось присущим урану свойством, стало известно как лучи Беккереля.
В 1898 г. этим явлением заинтересовались ученица Беккереля Мария Складовская-Кюри и ее муж Пьер Кюри. Они обнаружили, что торий также испускает лучи Беккереля, и переименовала их в радиоактивность. После тщательных исследований они открыли
 Мария Складовская-Кюри
(1867 – 1934)
Мария Складовская-Кюри
(1867 – 1934)
|  Пьер Кюри (1859 - 1906)
Пьер Кюри (1859 - 1906)
|
два новых радиоактивных элемента - полоний (названный так в честь родины Мари Складовской-Кюри - Польши) и радий («радий» в переводе с латинского – испускающий лучи, «излучающий»).
В 1911 г. английский ученый Эрнест Резерфорд, исследуя рассеяние α -частиц тонкой металлической фольгой, предположил, что внутри атома имеется ядро шарообразной формы размером около 10-12 см. Позже (1919 г.), исследуя реакцию 714N+24He®817O+11H (протон) он высказал гипотеза о существовании нейтрона 01n.
Используя эту модель, великий датский физик-теоретик Нильс Бор в 1913 г. разработал первую теорию строения атома: атом имеет положительно заряженное ядро и окружающие его электроны (рис.

| 
|
| Э. Резерфорд (1871 – 1937) | Н. Бор (1885-1962) |
1.1). В ядре сосредоточена почти вся масса атома (более 99, 95%). Размеры ядер составляют 10-10 - 10-15 м.
В 1932 г. английский физик Дж. Чедвик открыл нейтрон в реакции 49Be+24He® 126C+ 01n. В этом же году немецкий ученый В. Гейзенберг и независимо от него отечественный физик Д.Д. Иваненко предложили протонно-нейтронную модель строения атомного ядра. Согласно этой модели ядра атомов включают в себя два вида элементарных частиц протоны (р) и нейтроны (n). Связанное состояние в n-р –системе называется дейтроном. Сколько в ядре протонов, столько и электронов вращается вокруг ядра (рис. 1.1).
Количеству протонов в ядре соответствует номеру элемента в таблице Д.И. Менделеева. Ядро любого элемента называется нукли 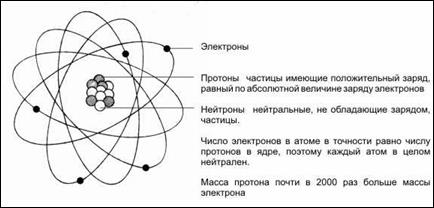
дом. Нуклид обозначается символом химического элемента с указанием атомного номера и массового числа в качестве нижнего и
Рис. 1.1. Схематическое изображение атома.
верхнего индекса соответственно (например, 24Не). В дальнейшем в ряде случаев для краткости изложения будет указываться только массовое число химического элемента.
Ядра с одним и тем же зарядом, но с разными массовыми числами (одинаковым количеством протонов и разным – нейтронов) называют изотопами. Изотопы имеют одинаковое строение электронных оболочек и, следовательно, близкие химические свойства. Они занимают одно и то же место в периодической системе химических элементов. Например, у первого элемента таблицы Менделеева - водорода существуют следующие изотопы:
- водород - 1Н (стабильный),
- дейтерий - 2Н (стабильный),
- тритий - 3Н (радиоактивный элемент, период полураспада - 12 лет).
У цезия имеются 20, у йода – 19, у стронция – 12, у плутония – 7 изотопов и т.д.
В таблице Менделеева (см. приложение) более 100 химических элементов. Почти каждый из них представлен смесью стабильных и радиоактивных атомов - изотопами данного элемента. Известно почти 2000 изотопов, из которых почти 300 – природные, т. е. естественные (столько же и стабильных изотопов), остальные – получены искусственным путём. Продукты ядерного взрыва содержат более 100 нестабильных изотопов. Большое количество радиоактивных изотопов содержится в продуктах деления ядерного горючего в ядерных реакторах АЭС и др. Но среди них количество изотопов, имеющих практическое значение и играющих заметную роль в природе невелико - не более десятка.
Радиоактивность - свойство некоторых нестабильных атомов к самопроизвольным превращениям (распаду) и к изменению своего нуклонного состава (количество протонов и нейтронов в ядре) и (или) энергетического состояния с образованием новых атомов (стабильные или радиоактивные) и испусканием ИОНИЗИРУЮЩИХ ИЗЛУЧЕНИЙ с большей или меньшей ПРОНИКАЮЩЕЙ СПОСОБНОСТЬЮ. Эти излучения и называются в обиходе радиацией («Radiation» в переводе с английского - " излучение"). Термин «радиоактивность» предложен Марией Склодовской Кюри в 1898 г. Позже был предложен знак: «Радиоактивность» для предупреждения работающих об опасности облучения.
 Знак: «Радиоактивность» Знак: «Радиоактивность»
|
Нестабильные изотопы, наряду с тяжелыми элементами с атомным номером выше 83, составляют многочисленное семейство нестабильных ядер нуклидов, претерпевающих радиоактивный распад и объединяемых единым понятием радионуклидов. Соотношение числа протонов и нейтронов в их ядрах превышает 1 и достигает 1, 6.
Число ядер радионуклидов постоянно уменьшается во времени благодаря распаду. Скорость распада этих ядер принято характеризовать периодом полураспада (Т½ ) - временем, за которое число радиоактивных ядер уменьшается в 2 раза. У каждого радионуклида свой период полураспада, он может составлять как доли секунды, так и миллиарды лет. Период полураспада любого радионуклида постоянен, и изменить его невозможно. Чем больше период полураспада и массовое число радиоактивного элемента, тем большее его количество соответствует одному кюри (1 Ки). Например, 1 Ки соответствует: 1 мг 60Со (Т½ = 5 лет), 1 г 226Rа (Т½ = 1590 лет), 16 г 239Рu (Т½ = 2400 лет), 570 кг 235U (Т½ = 880 млн. лет).
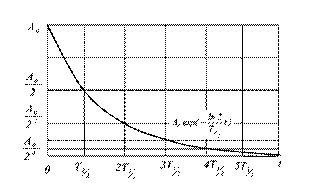
Рис. 1.2. Распад радионуклидов.
Убывание количества распадающихся ядер радионуклида происходит по экспоненте (рис. 1.2). Поэтому полностью радионуклид не исчезнет никогда. Так, например, для радионуклида с периодом полураспада 1 час количество его станет меньше первоначального в 2 раза через 1 ч, через 2 ч - в 4, через 3 ч - в 8 раз и т.д. Динамика распада описывается законом радиоактивного распада, устанавливающим, что за единицу времени распадается всегда одна и та же доля ядер данного радионуклида. Эта доля атомов, распадающихся в 1 секунду, называется радиоактивной постоянной распада (постоянная или константа распада) и обозначается λ. Величины λ и T1/2 связаны между собой обратно пропорциональной зависимостью: λ = ln 2 / T1/2. Учитывая, что ln 2 = 0, 693, данная формула может приобрести следующий вид: λ = 0, 693 / Т1/2 (сек-1).
Из закона радиоактивного распада следует, что Nt = N0•e-λ t, где N0 - число радиоактивных атомов в начальный (нулевой) момент времени, Nt число атомов, оставшихся к моменту t (время в секундах), e – основание натурального логарифма (е - 2, 718). Так как за время, равное одному периоду полураспада, число радиоактивных атомов уменьшается в два раза, то при t = T1/2 имеем: Nt = N0/2: e-λ t = 1/2; e-λ t = 2 (где t = T1/2) и, в итоге, ln 2 = λ •Т1/2.
Из указанного закона следует, что количество ядер, распадающихся за промежуток времени dt, прямо пропорционально количеству нераспавшихся ядер: dN/dt = λ N. При этом N = N0 e-λ t, или
| N = N0е - 0, 693t/T, |
где N0 – количество ядер радионуклида в момент начала отсчёта времени (t = 0); λ – постоянная распада; N – количество ядер радионуклида спустя время t; e – основание натурального логарифма = 2, 718.
Следует различать радиоактивность и радиацию. Радиоактивность – способность некоторых нестабильных атомов к самопроизвольному распаду или изменению своего нуклонного состава с испускание ионизирующих излучений. Источники ионизирующих излучений - радиоактивные вещества или ядерно-технические установки (реакторы, ускорители, рентгеновское оборудование и т.п.). Они могут существовать долгое время, а радиация существует лишь до момента своего поглощения в каком-либо веществе. Радиацию нельзя вызвать с помощью химических реакций.
3.2. Ионизирующее излучение – любое излучение, взаимодействие которого со средой приводит к образованию электрических зарядов разных знаков. Это частицы или γ -кванты, энергия которых достаточно велика, чтобы при воздействии на вещество создавать ионы разных знаков. Энергии ионизирующей радиации вполне хватает, чтобы выбить хотя бы один электрон из встречного атома По-

Рис. 1.3. Образование ионов, заряжённых положительно и отрицательно.
добные атомы без электрона называются ионами (рис. 1.3).
|
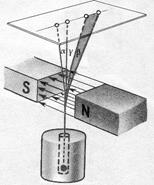
| Рис. 1.4. Неоднородность проника- ющей радиации. |
Самым известным видом ионизирующей радиации является рентгеновское излучение. При ядерном взрыве, авариях на АЭС, ядерных превращениях появляются и действуют другие невидимые и не ощущаемые человеком излучения. По своей природе они могут быть электромагнитными, как, например, гамма(γ)- и рентгеновское излучения (так называемое фотонное излучение), или представлять поток быстро движущихся элементарных частиц – нейтронов, протонов, бета (β)- и альфа (α)-частиц (это корпускулярное излучение). Любые ядерные излучения, взаимодействуя с различными материалами, ионизируют их атомы и молекулы. ИОНИЗАЦИЯ среды тем сильнее, чем больше мощность дозы радиоактивного излучения и длительнее их воздействие.
На рис. 1.4 представлен классический опыт, позволивший обнаружить сложный состав радиоактивного излучения. Препарат радия помещали на дно узкого канала в куске свинца. Против канала находилась фотопластинка. На выходившее из канала излучение действовало сильное магнитное поле, линии индукции которого перпендикулярны лучу ионизирующего излучения. Вся установка размещалась в вакууме. Под действием магнитного поля пучок распадался на три потока.
Две составляющие потока отклонялись в противоположные стороны. Это указывало на наличие у излучений электрических зарядов противоположных знаков. При этом отрицательный компонент излучения отклонялся магнитным полем гораздо сильнее, чем положительный. Э. Резерфорд, обнаруживший в 1899 г. эти две составляющие излучения, назвал менее проникающую α -излучением и более проникающую - β -излучением. Третья составляющая урановой радиации, не отклонявшаяся магнитным полем и самая проникающая из всех, была открыта через год (1900 г.) Полем Виллардом и названа по аналогии с резерфордовским рядом (α и β) третьей буквой греческого алфавита - γ -излучением. Следовательно, положительно заряженный компонент получил название α -лучей, отрицательно заряженный – β -лучей и нейтральный – γ -лучей.
Каждому виду излучения присущи свои ионизирующая и проникающая способности. Именно эти свойства лежат в основе повреждающего действия ионизирующих излучений на живые клетки человека или животного, что приводит к развитию заболевания, различной степени тяжести, а в некоторых случаях и к смерти. Рассмотрим эти две способности для различных излучений.
Альфа-излучение (α -излучение) представляет собой поток α -частиц, испускаемых при радиоактивном распаде элементов тяжелее свинца, элементов с № > 83 (например, урана, тория, радия, плутония, табл. 1.1), или образующихся в ходе ядерных реакций. α -частица фактически являются ядрами гелия (24Не), состоящими из двух протонов и двух нейтронов (статический электрический заряд равен +2, массовое число - 4). q = 2е. Скорость α -частицы при вылете из ядра - от 12 до 20 тыс. км/сек. В вакууме α -частица могла бы обогнуть земной шар по экватору за 2 с. Ионизирующая способность α -излучения в воздухе характеризуется образованием в сред-
Таблица 1.1.
|
|
