
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
ЛЕКЦИЯ 9. 1.Оптические свойства дисперсных систем
|
|
1.Оптические свойства дисперсных систем. Уравнение Рэлея и его анализ.
Абсорбция света.. Нефелометрия, турбидиметрия.
2. Отдельные классы коллоидных систем.Суспензии, порошки, пены.
3.Эмульсии. Классификация эмульсий. Стабилизация. Методы разрушения эмульсий.
4. Полуколлоиды. Мицеллообразование в коллоидных системах. С олюбилизация
5. Аэрозоли.
Прохождение света через дисперсную систему сопровождается такими явлениями, как преломление, поглощение, рассеяние и отражение. Все эти оптические явления обусловлены дисперсностью и гетерогенностью системы. Неоднородность системы определяет неоднородность оптических свойств. На эти свойства влияет структура, размер и форма частиц.
Преобладание какого-то из перечисленных оптических явлений зависит главным образом от соотношения длины волны падающего света и размера частиц дисперсной фазы.
В грубодисперсных системах размер частиц превышает длину волны видимой части спектра (40 – 70 нм), и поэтому грубодисперсные системы свет отражают.
В высокодисперсных системах частицы соизмеримы по размерам с длиной волны, в результате чего преобладает светорассеяние.
Впервые явления светорассеяния (опалесценции) описал М.В. Ломоносов, а более подробно изучил Фарадэй и его ученик Тиндаль. Они открыли эффект светорассеяния при пропускании пучка света через коллоидный раствор золота, отметив, что только коллоидные системы дают светящийся конус, узкий со стороны вхождения света в раствор и постепенно расширяющийся, особенно четко видимый на черном фоне (свет луча кинопроектора в кинотеатре – пример такого эффекта, поскольку частицы пыли являются частицами дисперсной системы Т/Г).
Молекулярные растворы и чистые вещества не дают такого эффекта, т.е. при пропускании пучка света через гомогенную среду такого явления не наблюдается. Это один из основных методов визуального определения, является ли система истинным раствором или коллоидным.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Теорию рассеяния света через коллоидный раствор создал Рэлей (1871г), определив, что интенсивность светорассеяния зависит от концентрации, длины волны и разности оптических свойств среды и фазы, а именно:
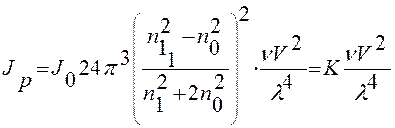 где
где
V – объем одной частицы, n -частичная (численная) концентрация.
Анализируя у равнение Рэлея, можно сделать следующие выводы:
1. При равенстве показателей преломления частиц и среды в гетерогенной системе может отсутствовать рассеяние света.
2. светорассеяние прямо пропорционально концентрации частиц, квадрату объема частицы (или 6-ой степени их радиуса)
3. Рассеяние света обратно пропорционально длине волны падающего света. отсюда можно заключить, что наиболее интенсивно происходит рассеяниесвета малых длин волн, а именно- фиолетовой части спектра, поэтому наиболее подвержены рассеянию голубые лучи, чем желто-красные.
4.
Максимальное светорассеяние происходит в системах с размером частиц < 0.1 l (2-4 10-8 м), при более крупных частицах в растворах появляется мутность и возрастает роль отражения света. Область применения уравнения Рэлея – разбавленные коллоидные растворы со сферическими частицами, в случае более крупных частиц другой формы Геллер определил другой показатель степени при длине волны – от4- 2, 8.
5. С другой стороны видно, что при более мелких частицах интенсивность рассеяни ослабевает пропоционально V2. Ту область размеров частиц, для которой интенсивность максимальна, называют Рэлеевской областью.
Для золей металлов это уравнение неприменомо, ввиду сильного поглощения ими света.
Уравнение Рэлея позволяет определить по экспериментальным данным радиус частиц, а отсюда и их объем, если известна концентрация частиц.
Может быть решена и обратная задача – при известных радиусе иобъеме –находят частичную концентрацию.
Интенсивность светорассеяния определяют методами нефелометрии и турбидиметрии, в основе которых лежит экспериментальное определение мутности (t =Ip/J 0)раствора или светопропускания и расчет радиуса частицы и ее объема.. (самостоятельно) Интенсивность света, прошедшего через какую-то однородную среду, всегда меньше, чем интенсивность падающего света, это объясняется явлением поглощения света, или абсорбцией света.
Для золей небольшой концентрации применим закон Ламберта-Бугера-Бера:
Jп = J0 e-ecl
где Jп – интенсивность прошедшего света, а J0 падающего.
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
e - молярный коэффициент поглощения. с – молярная концентрация, l – толщина слоя.
Отношение Jп/J0 носит название светопропускания раствора илиотносительной прозрачности раствора.
Если это уравнение привести к виду прямой, то его логарифмируя, получим:
ln(J0/Jп)=D= ecl
где величина ln(J0/Jп) – оптическая плотность раствора, или экстинкция D, которая прямо пропорциональна концентрации
Из уравнения Рэлея следует, что его можно применить для расчета молекулярной массы высокомолекулярного вещества (ВМВ:
Jp = J0 K Mc/NA r
Особое место среди оптических методов исследования дисперсных систем занимает ультрамикроскопия. Она позволяет видеть частицы с диаметром 2 – 4 нм, может быть использована для определения их численной концентрации путем простого подсчета, наблюдать смещение частиц под действием броуновского движения. (Самостоятельно).
2. Отдельные классы коллоидных систем.Суспензии, порошки, пены.
Отдельные классы коллоидных систем представляют собой большой практический интерес, поскольку человек постоянно сталкивается с ними в процессе своей жизненнной практики.
Такими системамми являются порошки, суспензии, пены, эмульсии, ПАВ и ВМС.
Порошки – это свободно-дисперсные системы с газообразной дисперсионной средой и твердой дисперсной фазой.
Размеры частиц порошков изменяются в широком диапазоне и в зависимости от этого им дают следующие названия: при диаметре
20*10-3 –10-5 м – песок,
2*10-5 –10-6 м –пыль
менее 2*10-6 м – пудра.
Порошки характеризуют следующими свойствами:
насыпная плотность, (масса единицы объема порошка, свободно насыпанного в какую-то емкость)
слипаемость – склонность порошка к образованию анрегатов, свойство обусловлено когезионностью частиц,
сыпучесть – подвижность частиц перемещаться относительно лруг друга (зависит от влажности, степени уплотнения)
гигроскопичность – способность порошка поглощать влагу, ее можно уменьшить добавлением ПАВ (дифильное вещество создает на его поверхности гидрофобный монослой,
абразивность – твердость частиц дисперсной фазы, имеет значение при расчете износа оборудования и разработке мер по предотвращению истирания стенок аппарата,
электрическая проводимость 1|R, зависит от влажности и плотности упаковки частиц, температуры
горючесть и взрываемость – порошка и пыли характеризуется: температурой самовоспламенения, температурой вспышки, максимальным давлением взрыва, минимальное взрывоопасное содержание кислорода в пыли.
Очень важным свойством порошков является способность к гранулированию. Этот процесс самопроизвольного слипания частиц порошка в конгломераты – гранулы шаробразной или цилиндрической формы. Процесс гранултрования широко применим в пищевой технологии, так как повышает стойкость пищевых продуктов при хранении, а также в производстве лекарств, удобрений.
Суспензиями называют микрогетерогенные системы с жидкой дисперсионной средой и твердой дисперсной фазой Т/Ж
Размер частиц суспензии – 10 –4 –10-6 м. наиболее грубодисперсные суспензии называют взвесями.
Седиментационнонеустойчивые системы. Повысить их устойчивость можно добавками полимера, что повышает вязкость раствора.
Если концентрацию дисперсной фазы в суспензии повысить до предельно возможной, то можно получить пасты.
Пены – дисперсные системы, у которых дисперная фаза состоит из пузырьков газа, а дисперсилонная среда (жидкая или твердая) образует тонкие пленки между пузырьками газа.
Образование пены происходит при прохождении газа через жидкость. Сущность его состоит в том, что пузырьки газа, окруженные адсорбционным слоем ПАВ, встречая у поверхности пленку, не могут пройти сквозь нее и создают на поверхности пену.
Пенообразование может быть как нежелательным процессом, так и необходимым.
Пенообразование – процесс необходимый в бродильном производстве, при обогащении руд методом флотации, при производстве косметических и фармацевтических средств, при тушении пожаров т.д.
Когда процесс пенообразования нежелателен, в этом случае используют пеногасители (жиры, масла, воски, высшие спирты, эфиры).
Эмульсии – это свободно-дисперсные системы, в которых и фаза и среда являются жидкостями, несмешивающимися или ограниченно смешивающимися.
одна из жидкостей полярна, другая неполярна и называется условно " маслом".
Эмульсии классифицируют по:
1). полярности фазы и среды В/М или М/В, прямые и обратные
2). по концен трации: 0, 1% - разбавленные, до 75% - концентрированные, свше 75% - высококонцентрированные.
От концентрации дисперсной фазы зависят все свойства эмульсий, и в первую очередь, их устойчивость.
В разбавленных и концентрированных эмульсиях капли фазы имеют сферическую форму, в эмульсиях при 75% они еще шарообразны, но уже упакованы вплотную друг к другу, А дальнейшее добавление фазы (при 90%) превращает капли в плоскости и эмульсия теряет свою текучесть, становится желатинизированной, приобретая свойства гелей.
Поскольку эмульсии являются высокогетерогенными системами с большой поверхностью раздела, их устойчивость невелика капли коалесцируют со временем или образуют агрегаты капель - флокулы а процесс носит название флокуляции. Поэтому эмульсии приходится стабилизировать, вводя в них специальные добавки – эмульгаторы.
Эмульгаторы – это растворимые ПАВ и ВМВ или нерастворимые порошкообразные вещества, добавление которых делает эмульсии устойчивыми.
механизм стабилизирующего действия эмульгаторов различен, но имеются некоторые закономерности, которые характеризуются правилом БАНКРОФТА:
гидрофильные эмульгаторы стабилизируют эмульсии прямого типа (В/М)
гидрофобные – обратного (М/В).
К первым относятся ПАВ, порошки, смачивающиеся водой. Лиофильные порошки (мел, гипс, глины) стабилизируют эмульсии прямого типа,
Лиофобные (сажа, уголь, канифоль, графит) – эмульсии обратного типа. таким образом, эмульгатор согласно правилу Банкрофта, должны располагаться со стороны дисперсионной среды, т.е. главным образом, на поверхности частиц дисперсной фазы.
Механизм действия порошковых эмульгаторов основан на усилении структурно-механического фактора системы, ПАВ на усилениии электростатического фактора в сочетании со структурно-механическим и энтропийным, молекулы ПАВ образуют благодаря длине своих углеводородных цепей не только защитные адсорбционные слои, но и участвуют в тепловом движении молекул, оттталкиваясь друг от друга своими радикалами.
Эмульсии могут обращаться, т. е. переходить из прямого типа в обратный и наоборот. Это вызвано, согласно геометрической теории, тем, что молекулы ПАВ как бы расклинивают своими хвостами – радикалами межфазную поверхность и изгибают ее так, что поверхность раздела становится по отношению к одной фазе выпуклой, эта жидкость является дисперсной средой, а другая сторона вогнута - эта жидкость становится дисперсной фазой.
Практически обращение фаз можно вызвать разными способами: изменением соотношения объемов фаз, перенесением эмульсии в сосуд из другого материала, перемешиванием. Но самым простым является изменение природы эмульгатора путем химического воздействия. Обращение фаз в эмульсиях наряду с другими методами применяют при деэмульгировании.
Эмульгирование является процессом совершенно необходимым в производстве многих пишевых и непищевых продуктов, но иногда образование эмульсий мешает проведению каких-то технологических операций.
Поэтому важно знать как можно разрушить эмульсию: седиментация – путем центрифугирования эмульсии
коагуляция - может быть вызвана действием поливалентногоиона электролита, вызывающего сжатие ДЭС.
Эмульсию можно разрушить, повысив температуру.
Полуколлоиды
Существуют такие системы, в которых вещества только частично находятся в коллоидном состоянии. Примером такой системы может быть обычное мыло.
Действительно, в растворе мыла имеются как отдельные молекулы, так и коллоионые образования. В зависимости от внешних условий молекулы могут оставаться в растворе, а при изменении концентрации фазы – снова образовывать мицеелы. Т.е, процесс мицеллобразования в таких ситемах обратим.
Мицеллообразование в молекулах ПАВ связано с дифильностью их молекул и наблюдается начиная с 4-5 атомов углерода в цепи. Процее мицеллообразования идет самопроизвольно, и мицеллярные образования ПАВ термодинавмически устойчивые, равновесные обратимые системы.
В водных растворах ПАВ мицеллообразование идет за счет сродства углеводороных радикалов, они объединяются друг с другом, чтобы контактировать с водой как можно меньше. В таком случае в водных растворах образуются прямые мицеллы – в которых углеводородные радикалы образуют ядро мицеллы, а полярные группы обращены к воде.
в неводных растворах (неполярных) средах идет образование мицеллы обратного типа –в которых гидрофобные группировки обращены в дисперсионную среду.
Важным свойством водных растворов ПАВ является их способность растворять нерастворимые в воде углеводородытипа бензола, гептана, различных масел, молекулы котрых внедряются внутрь мицелл.
Процесс растворения в мицеллярных системах нерастворимых в чистых жидкостях соединений называют солюбилизацией.
Мицеллярные системы обладают сильным моющим действием, а при сухой химчмстке происходит солюбилизация обратнми мицеллами полярных загразений с тканей, прямыми мицеллами солюбиоизируются жировые загрязнения, на чем основано применение ПАВ.
Велика роль процесса солюбилизации в протекании биологически важных процессов усваивания нерастворимых в воде жиров и многих витаминов, мицеллярные ПАВ являются для них способом транспортирования их в живой организм
Аэрозоли. Т/Г, Ж/Г. Самостоятельно
|
|
