
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Цикл Кребса, характеристика основных реакций.Энергетика цикла и физиологическая роль.
|
|
Произошедшие в цитоплазме реакции гликолиза приводят к образованию пирувата (ПВК). Последующие превращения пирувата протекают в митохондриальном пространстве- матриксе митохондрии. В матрикс молекулы ПВК проникают через внутреннюю митохондриальную мембрану в результате обмена с ионами гидроксила (НО-). Уже в матриксе, при участии NAD-зависимой пируватдекарбоксилазы ПВК превращается в ацетил-КоА: Образующийся NADH генерирует в дыхательной цепи 6 молекул АТФ (в пересчете на 1 молекулу глюкозы).
Ацетил-КоА вступает в цикл трикарбоновых кислот (ЦТК, цитратный цикл, цикл Кребса) при взаимодействии с молекулой оксалоацетата:
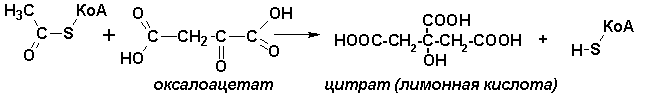
Реакция катализируется цитратсинтетазой. Другие реакции цикла и катализаторы показаны на рисунке выше.
Энергетический баланс окисления ацетил-КоА в ЦТК составляет 24 молекулы АТФ. Полное окисление глюкозы (гликолиз (8 АТФ)+ ЦТК (24 АТФ), включая окислительное декарбоксилирование пирувата в ацетил-КоА (6 АТФ)), дает 38 молекул АТФ на молекулу глюкозы.
Реакции цикла превращений Ацетил-КоА впервые были установлены Гансом Кребсом (университет Шеффилда, Великобритания), за что в 1953 году он был удостоен Нобелевской премии.
Активность ЦТК повышается с ростом концентрации АДФ (аллостерический активатор изоцитрат-дегидрогеназы) и снижается с ростом АТФ. За один оборот в ЦТК молекула ПВК окисляется полностью в 3 Н2О и СО2.

32.Структурно-функциональная организация электрон-транспортной цепи дыхания.
ЭТЦ- дыхания расположена на внутренней мембране митохондрий и включает 4 интегральных комплекса(которые пронизывают мембрану насквозь), а также липофильный переносчик убихинон. В состав митохондриальной мембраны входит интеграт\льный полипептид АТФ-синтаза, осуществляющий сопряжение транспорта протонов с синтезом АТФ.
Комплекс I (НАДН-дегидрогеназный комплекс)― он переносит электроны от восстановленной НАД к убихинону. Работа данного комплекса сопровождается трансмембранным переносом протона из матрикса в межмембранное пр-во. НАД(Ф)-зависимые дегидрогеназы, катализирующие отрыв водорода от молекул различных субстратов и передающие его на стартовый переносчик дыхательной цепи – НАД(Ф)-H2-дегидрогеназу – растворимые ферменты. Дегидрогеназы флавопротеиновой природы, выполняющие аналогичную функцию, могут быть локализованными в мембране (например, сукцинатдегидрогеназа) или существовать в растворимой форме (ацетил-КоА-дегидрогеназы жирных кислот). Водород с них поступает в дыхательную цепь на уровне хинонов.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Комплекс II― (Сукцинатдегидрогеназа) не перекачивает протоны, но обеспечивает вход в цепь дополнительных электронов за счёт окисления сукцината.
Комплекс III (Цитохром-bc1-комплекс) ― переносит электроны с убихинона на два водорастворимых цитохрома с, расположенных на внутренней мембране митохондрии. Убихинон передаёт 2 электрона, а цитохромы за один цикл переносят по одному электрону. При этом туда также переходят 2 протона убихинона и перекачиваются комплексом.
Хиноны — жирорастворимые соединения, имеющие длинный терпеноидный " хвост", связанный с хиноидным ядром, способным к обратимому окислению — восстановлению путем присоединения 2 атомов водорода. Наиболее распространен убихинон, функционирующий в дыхательной цепи на участке между флавопротеинами и цитохромами. В отличие от остальных электронных переносчиков хиноны не связаны со специфическими белками. Небольшой фонд убихинона растворен в липидной фазе мембран
Цитохромы, принимающие участие на заключительном этапе цепи переноса электронов, представляют собой группу белков, содержащих железопорфириновые простетические группы (гемы). С помощью цитохромов осуществляется перенос электронов, в процессе которого меняется валентность железа:
Fe2+ → Fe3+ + e –
В митохондриях обнаружено пять цитохромов (b, c, c1, a, a3), различающихся между собой спектрами поглощения и окислительно-восстановительными потенциалами.
Комплекс IV (Цитохром c оксидаза) катализирует перенос 4 электронов с 4 молекул цитохрома на O2 и перекачивает при этом 4 протона в межмембранное пространство.
V комплекс― АТФ-синтаза ― см вопрос 21
В результате работы ЭТЦ митохондрий происходит окисление НАДФН или ФАДН, перенос электрона на конечный акцептор О2 и образование Н2О, а также формирование транс мембранного градиента протонов, служит движущей силой АТФ.
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
При окислении 1 молекулы НАД― 3 АТФ.
При окислении 1 молекулы ФАД― 2 АТФ
Окислительное фосфорилирование. Строение и механизм работы АТФ-синтазы. см вопросы 21-22.
В соответствии с теорией Митчелла протоны проходят из митохондриального матрикса во внешнее митохондриальное пространство, тогда как электроны от НАДН идут на ЭТЦ, встроенную в митохондриальную мембрану. Каждая пара электронов пересекает мембрану три раза, когда передается с одного переносчика к другому и в конечном счете к О2. Перенос каждой пары ē по цепи от НАДН до О2 приводит к переходу через митохондриальную мембрану шести протонов. В результате возникает электрохимический потенциал Н+ на внутренней мембране. Запасенная таким образом энергия используется для синтеза АТФ при обратном транспорте протонов через АТФ-азный комплекс. Мембрана выполняет сопрягающую функцию: связывает два процесса – транспорт электронов и синтез АТФ.
Таким образом, физиологический смысл транспорта электронов заключается в образовании электрохимического потенциала, который приводит к синтезу АТФ.
Процесс фосфорилирования АДФ с образованием АТФ, сопряженный с транспортом электронов от дыхательного субстрата к кислороду воздуха, получил название окислительного фосфорилирования.
Суммарное уравнение этого процесса можно записать так:
НАДН + Н+ + 3АДФ + 3Ф + 1/2О2 → НАД+ + 3АТФ + 4Н2О.
34.Основные показатели дыхания, их характеристики. Влияние факторов среды на интенсивность дыхания растений.
Температура.
Как всякая ферментативная реакция с повышением температуры интенсивность дыхания возрастает. Однако это происходит до определенного предела, выше которого начинается инактивация ферментов и интенсивность дыхания снижается. При этом надо учитывать длительность выдерживания растения при данной температуре. При кратковременной экспозиции интенсивность дыхания возрастает при повышении температуры до 35°С и даже 40°С. При длительном выдерживании в такой температуре интенсивность дыхания уменьшается. Для суждения о влиянии температуры на какой-либо процесс обычно используют такой показатель как температурный коэффициент. Температурный коэффициент (Q10) процесса дыхания зависит от типа растений и от градаций температуры. Так, при повышении температуры от 5 до 15°С Q10 может возрастать до 3, тогда как повышение температуры от 30 до 40°С увеличивает интенсивность дыхания менее значительно (Q10 около 1, 5). Это может быть связано с тем, что повышение температуры в большей степени ускоряет ферментативные процессы по сравнению с поступлением кислорода в клетки. Изменение оптимальных температур при дыхании растений в зависимости от фазы их развития связано с тем, что в процессе онтогенеза меняются пути дыхательного обмена. Между тем для разных ферментных систем наиболее благоприятными являются различные температуры. Так, температурный минимум работы цитохромов лежит выше по сравнению с флавиновыми дегидрогеназами. В этой связи интересно, что в более поздние фазы развития растений наблюдаются случаи, когда флавиновые дегидрогеназы выступают в роли конечных оксидаз, передавая водород непосредственно кислороду воздуха.
Снабжение кислородом.
Увеличение содержания кислорода до 5—8% сопровождается повышением интенсивности дыхания. Дальнейшее возрастание концентрации 02 обычно уже не сказывается на интенсивности дыхания. Однако из этого общего положения имеются исключения. Снабжение растительных тканей и клеток кислородом зависит не только от его содержания во внешней среде, но и от скорости его поступления. Между тем часто проникновение кислорода к тем или иным тканям затруднено. Это обстоятельство может проявляться на семенах и на плодах с плотной оболочкой. В этом случае увеличение концентрации кислорода в среде до 20% и более повышает интенсивность дыхания. Большое значение в снабжении кислородом отдельных органов и тканей имеет система межклетников, способствующая циркуляции воздуха. Воздух, проникая через устьица листа, достигает по межклетному пространству других органов, что и позволяет им осуществлять аэробное дыханиеИзвестно, что приспособление корневых систем к росту в анаэробных условиях связано с развитием особенно большого объема межклетников.. В отсутствие кислорода дыхание уступает место брожению. При содержании кислорода ниже 5% брожение усиливается, и выделение углекислого газа начинает превышать поглощение кислорода. Это приводит к тому, что дыхательный коэффициент, как правило, становится больше единицы. При повышении содержания кислорода процесс брожения полностью ингибируется (эффект Пастера) и дыхательный коэффициент становится равным единице. Необходимо также отметить, что кислород оказывает стимулирующее влияние на процесс фотодыхания.
Содержание углекислого газа
. СО2 является конечным продуктом как брожения, так и аэробного дыхания. При довольно высоких концентрациях СО2, значительно превышающих те, которые обычно окружают растительный организм (выше 40%), процесс дыхания тормозится. Торможение вызывается несколькими причинами: 1) высокая концентрация СО2 может оказывать общее анестезирующее влияние на растительный организм; 2) СО2 тормозит активность ряда дыхательных ферментов; 3) повышение содержания СО2 вызывает закрытие устьиц, что затрудняет доступ кислорода и косвенно тормозит процесс дыхания.
Содержание воды
. Небольшой водный дефицит растущих тканей увеличивает интенсивность дыхания. Это связано с тем, что водный дефицит и даже подвядание листьев усиливают процессы распада сложных углеводов (крахмала) на более простые (сахара). Увеличение содержания Сахаров (основного субстрата дыхания) усиливает сам процесс. Вместе с тем при водном дефиците нарушается сопряжение окисления и фосфорилирования. Дыхание в этих условиях представляет в основном бесполезную трату сухого вещества. При длительном завядании растение расходует сахара, и интенсивность дыхания падает. Иная закономерность характерна для органов, находящихся в состоянии покоя. Увеличение содержания воды в семенах с 12 до 18% уже увеличивает интенсивность дыхания в 4 раза. Дальнейшее повышение содержания воды до 33% приводит к увеличению интенсивности дыхания примерно в 100 раз. При перемещении растения или ткани из воды в раствор солей дыхание усиливается — это так называемое солевое дыхание.
Свет.
Так, в процессе фотосинтеза образуются основные субстраты дыхания — углеводы. Вместе с тем промежуточные продукты, образовавшиеся при дыхании, могут вовлекаться в фотосинтетический цикл. Установлено, что свет стимулирует процесс фотодыхания. В настоящее время полагают, что влияние света на процесс дыхания многообразно. Под влиянием света, особенно коротковолновых сине-фиолетовых лучей, интенсивность обычного темнового дыхания возрастает. Активация дыхания светом показана на бесхлорофилльных растениях. Возможно также, что свет активирует дыхательные ферменты (оксидазы).
Питательные соли
 . Интенсивность дыхания сильно зависит от снабжения растения элементами минерального питания. Такие элементы, как фосфор, сера, железо, медь, марганец, принимают непосредственное участие в процессе дыхания, входя в промежуточные продукты (фосфор) или являясь составной частью дыхательных ферментов.
. Интенсивность дыхания сильно зависит от снабжения растения элементами минерального питания. Такие элементы, как фосфор, сера, железо, медь, марганец, принимают непосредственное участие в процессе дыхания, входя в промежуточные продукты (фосфор) или являясь составной частью дыхательных ферментов.
Поранение.
Поранение органов и тканей растения усиливает интенсивность дыхания. Это связано с разрушением клеток, из-за чего повышается соприкосновение дыхательных субстратов и ферментов. Частично поранение может вызывать переход клеток в меристематическую фазу роста. Интенсивность дыхания делящихся клеток всегда выше по сравнению с клетками, закончившими рост.
35.Физико-химические свойства воды. Роль воды в жизнедеятельности растений.
Свойства воды довольно необычны и связаны главным образом с малыми размерами молекул воды и их полярностью.
Полярность молекул воды.
Под полярностью подразумевают неравномерное распределение зарядов в молекуле воды. В целом молекула нейтральна, но атомы в ней распределены так, что на одном конце образуется частичный положительный заряд (δ +), а на другом частичный отрицательный заряд (δ -). Такую молекулу называют диполем. Более электроотрицательный атом кислорода притягивает электроны водородных атомов, в результате между молекулами возникает электростатическое взаимодействие. Эти взаимодействия более слабые, чем обычные ионные связи называются водородными связями
Вода как растворитель.
Вода хороший растворитель для полярных веществ. К ним относятся ионные соединения – соли, которые диссоциируют на ионы при растворении в воде, а так же некоторые неионные соединения.
Неполярные вещества, например липиды, не смешиваются с водой и потому могут разделять растворы на отдельные компартменты, подобно биологическим мембранам. Неполярные части молекул отталкиваются водой и притягиваются друг к другу. Наличие свойств растворителя у воды, обуславливает так же ее роль в транспорте веществ.
Большая теплоемкость.
Вода обладает большой теплоемкостью. Это значит, что существенное увеличение тепловой энергии вызывает лишь относительно небольшое повышение температуры. Это связано с тем, что большая часть энергии тратится на разрыв водородных связей, ограничивающих подвижность молекул воды.
Большая теплоемкость сводит к минимуму температурные изменения в водной среде, благодаря этому биохимические реакции идут в относительно узком температурном диапазоне и опасность нарушения от резкого скачка температуры им грозит не так сильно.
Большая теплота испарения.
Скрытая теплота испарения – это мера тепловой энергии, которую нужно сообщить жидкости для ее превращения в пар, т.е. для преодоления сил молекулярного сцепления.
Испарение воды требует значительного количества энергии, что объяснимо наличием водородных связей между молекулами. Именно из-за этого температура кипения воды – вещества, обладающего настолько маленькими молекулами – необычно высока.
Энергия, требуемая молекулами воды для испарения, черпается ими из своего окружения. Таким образом, испарение воды сопровождается охлаждением. Это явление играет существенную роль при охлаждении транспирирующих листьев растений.
Большая теплота плавления.
Скрытая теплота плавления – мера тепловой энергии, необходимая для расплавления твердого вещества (в случае воды – льда).
Воде для плавления требуется довольно большое количество энергии. Справедливо и обратное – при замерзании вода должна отдать большое количество тепловой энергии. Это уменьшает вероятность замерзания содержимого клеток и окружающей их жидкости. Кристаллы льда губительны для живого, когда образуются внутри клеток.
Большое поверхностное натяжение и когезия.
Когезия – сцепления молекул физического тела друг с другом при действии сил притяжения. На поверхности жидкости существует поверхностное натяжение – результат действия между молекулами сил когезии, направленных внутрь. Значительная когезия играет важную роль в движении воды по сосудам ксилемы.
Вода как реагент.
Биологическое значение воды определяется тем, что она является одним из необходимых метаболитов, то есть участвует в биохимических реакциях.
И так, обобщим физиологические функции воды:
· Обеспечивает поддержание структуры (высокое содержание воды в протоплазме).
· Служит растворителем и средой для диффузии.
· Вода участвует в реакциях гидролиза.
· Участвует в фотосинтезе: 6CO2+6H2O→ C6H12O6+6O2
· Обуславливает осмос и тургесцентность клеток.
· Обеспечивает транспирацию и транспорт веществ.
· Обеспечивает прорастание семян – набухание, разрыв семенной оболочки, дальнейшее развитие.
· Служит средой в которой происходит оплодотворение.
· Обеспечивает распространение семян и гамет.
36. Термодинамические показатели водного обмена растений: активность воды, химический и водный потенциалы, осмотический потенциал.
Энергетический уровень молекул данного вещества, который выражается в скорости их диффузии наз-ют химическим потенциалом этого вещества(ψ). Хим потенциал чистой воды называют водным потенциалом. (ψ h2o) Он характеризует способность воды диффундировать, испаряться или поглощаться и выражается в Паскалях. Наивысшая величина водного потенциала – у хим. Чистой воды, эта величина принята за нуль. Поэтому водный потенциал любого раствора и биологической жидкости имеет отрицательное значение. Водный потенциал складывается из осмотического потенциала ψ s, потенциала давления ψ p, гравитационного потенциала ψ g, потенциала набухания биоколлоидов.
Для оценки степени участия воды в различных химических, биохимических и микробиологических реакциях широко применяют показатель активность воды aw, определяемый как отношение парциального давления паров воды над продуктом к парциальному давлению пара над чистой водой. Показатель «активность воды» был предложен У. Скоттом в 1953 г. и в настоящее время широко применяется на практике.
Вода имеет маленькие размеры, поэтому вода может проходить через дефекты липидного бислоя. Транспорт воды осуществляется через аквапорины ― специальные трансмембранные белки. Вода так же может транспортироваться по ионным каналам вместе с ионами. Транспорт осуществляется по градиенту концентрации(против градиента водного потенциала).
Осмотический потенциал― обусловлен наличием в клетках осмотически активных веществ и оражает их влияние на активность воды.
|
|
