
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Лабораторна робота № 18. Кількісний колориметричний аналіз. Визначення концентрації домішок в газах і рідинах
|
|
Мета роботи – вивчити закони поглинання світла, визначити концентрації домішок деяких речовин у розчині та газі.
Вказівки до виконання лабораторної роботи
Для виконання лабораторної роботи необхідно вивчити такий теоретичний матеріал: закон поглинання світла – закон Бугера та Бугера – Бера.
[1, т.3, §§ 6.5; 2, §§ 187; 4. т.2, §§ 345]
За допомогою абсорбційного аналізу, заснованого на законах поглинання світла, проводять кількісний аналіз при дослідженні складу речовини: кількісне визначення його компонентів, визначення ступеня його чистоти та ін. Яке б не було завдання дослідження, в цих методах завжди використовується фізична властивість речовини – її здатність поглинати світлове випромінювання з певною довжиною хвилі.
Закони поглинання і випромінювання, що з ними зустрічається аналітик у випадку розчину, дають співвідношення між величиною поглинання і кількістю речовини, яка поглинає. Завдяки дослідному визначенню поглинання в однорідних прозорих твердих тілах, рідинах та газах встановлено два закони, які дають найбільш важливі для абсорбційного аналізу співвідношення.
Перший з цих законів дає зв’язок між поглинаючою здатністю та товщиною шару поглинаючої речовини. Нехай І 1 – величина енергії випромінювання, що падає на першу поверхню зразка, І 0 – величина енергії, що входить у зразок, І – величина енергії, яка падає на другу поверхню, І 2 – величина енергії, що виходить із зразка. Тоді Т – пропускання зразка: 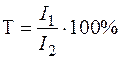 .
.
Внутрішнє пропускання зразка: 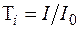 .
.
За рахунок втрат на відбивання світла при переході з одного середовища в інше й абсорбційної здатності самої кювети завжди І 1 > I 0, a I > I 2, однак ці втрати енергії приладу завжди компенсуються. Тоді зменшення інтенсивності на dІ при проходженні шару товщиною dx пропорційне інтенсивності І світла на глибині х:
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
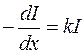 , або
, або 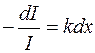 ;
;
інтегруючи від І 0 до І, та від 0 до d, одержуємо закон Бугера:
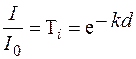 , (18.1)
, (18.1)
де k – коефіцієнт поглинання, який змінюється в залежності від довжини хвилі падаючого світла.
Крім того, вводять поняття оптичної густини речовини D, яка пропорційна коефіцієнту поглинання:
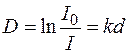 .
.
Закон Бера пов’язує між собою пропускання речовини й концентрацію поглинаючої речовини в розчині. Якщо с – концентрація, то пропускання Т і для даної товщини шару буде дорівнювати:
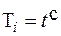 ,
,
де t – пропускання шару розчину тієї ж товщини з концентрацією, що дорівнює 1.
Внаслідок того, що Т і = I / I 0, об’єднаний закон Бугера–Бера можна записати так:
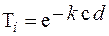 або
або 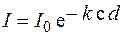 .
.
У логарифмічній формі концентрацію знаходимо як
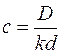 , де
, де 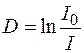 .
.
Закон Бугера – це рідкісний приклад узагальнення, що завжди має силу. Відхилень від цього закону у випадку однорідних систем не знайдено.
Внаслідок цього відхилення від об’єднаного закону Бугера–Бера в будь–якій системі потрібно віднести за рахунок невиконання закону Бера. Встановлено, що відхилення від закону Бера можна приписати хімічним процесам, що протікають у розчинах. Такі уявні відхилення мають місце, коли поглинаюча речовина дисоціює у розчині або ж утворює сполуку з розчинником. Відхилення від закону Бера спостерігають тоді, коли поглинаючі частинки (атоми, іони, молекули) впливають одна на одну. Із зміною концентрації може змінюватись і взаємодія між молекулами розчинника та поглинаючої речовини.
Для визначення концентрації домішок у розчині та газі використовують фотометр TWO GELL. Принципова схема такого фотометра зображена на рисунку 18.1:
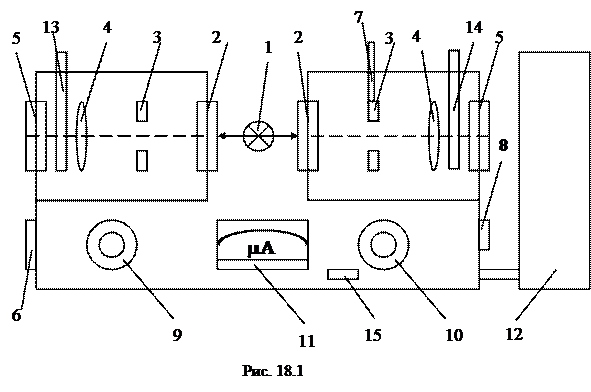 |
1 – освітлювальна лампочка; 2 – світлофільтри; 3 – діафрагми; 4 – лінзи; 5 – фотоелементи; 6 – регулятор лівої діафрагми; 7 – регулятор правої діафрагми; 8 – затвор правого плеча; 9 – потенціометр точного регулювання лівого плеча; 10 – потенціометр точного регулювання правого плеча; 11 – мікроамперметр; 12 – стабілізатор напруги; 13 – ліва кювета; 14 – права кювета; 15 – вмикач фотометра.
Принцип роботи фотометра TWO GELL полягає в порівнянні світлових потоків лівого і правого плеча. Світловий потік від лампи 1 розділяється на два потоки, лівий і правий. Проходячи в кожному плечі через системи: світлофільтрів, діафрагм та лінз світловий потік попадає на фотоелемент. Фотострум кожного плеча реєструється мікроамперметром, де відбувається їх порівняння. Якщо ці струми рівні, то мікроамперметр показує нуль. Однакового фотоструму від правого і лівого плеча досягають регулюванням світлових потоків за допомогою діафрагм 3 регуляторами 6 і 7. Більш точне регулювання досягається потенціометрами 9 та 10. Якщо в лівому плечі поставити кювету з розчином, а в правому тільки кювети з розчинником, то фотострум буде не скомпенсованим: мікроамперметр покаже різницю струмів у плечах. Мікроамперметр має два типи шкал: перша в мікроамперах, друга – відсотках поглинання світлового потоку.
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
Для визначення концентрації домішок у розчину необхідно визначити покази мікроамперметра в (mА) для відомих концентрацій для кювет однакової товщини d і побудувати графік I = f (c). Потім знайти покази мікроамперметра для невідомої концентрації і за графіком знайти невідому концентрацію домішки.
Хід роботи
1. Вставити в ліве і праве плече фотометра жовті світлофільтри.
2. Ввімкнути стабілізатор у мережу, а потім ввімкнути освітлювальну лампу. Після цього ввімкнути фотометр (вмикач 15).
3. Регуляторами діафрагм 6 і 7 встановити стрілку мікроамперметра на нуль. Вимкнути фотометр.
4. Поставити в праве плече кювету з розчинником, а в ліве – кювету з відомою концентрацією розчину. Ввімкнути фотометр. Зробити відлік і записати в таблицю 18.1. Повторити це для всіх відомих концентрацій.
5. Побудувати графік I = f (c).
6. Визначити покази мікроамперметра для невідомої концентрації домішки. За графіком I = f (c). визначити невідому концентрацію домішки.
Таблиця 18.1
| № пор. | І, (mА) | с, % | с х, % |
Контрольні запитання
1. Закони поглинання світла.
2. Який принцип будови та роботи фотометра?
3. Яка роль світлофільтрів у калориметричному аналізі?
4. Поняття про оптичну густину речовини.
|
|
