
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
⚡️ Для новых пользователей первый месяц бесплатно. А далее 290 руб/мес, это в 3 раза дешевле аналогов. За эту цену доступен весь функционал: напоминание о визитах, чаевые, предоплаты, общение с клиентами, переносы записей и так далее.
✅ Уйма гибких настроек, которые помогут вам зарабатывать больше и забыть про чувство «что-то мне нужно было сделать».
Сомневаетесь? нажмите на текст, запустите чат-бота и убедитесь во всем сами!
Хімічні властивості.
|
|
Лекція № 10
Багатоатомні спирти та феноли. Номенклатура, фізичні та хімічні властивості.
Спирти, молекули яких містять декілька гідроксильних груп відносять до багатоатомних спиртів.
Спирти, які містять дві гідроксильні групи біля одного атома Карбону нестабільні, вони розкладаються з виділенням молекули води та утворенням альдегідів чи кетонів. Тому найпростішим представником двоатомних спиртів є етиленгліколь або гліколь, триатомних спиртів – гліцерин.

Двоатомні спирти називають також діолами або гліколями (від гр. glykys – солодкий), через солодкий смак найпростіших представників цих спиртів; триатомні – триолами або гліцеринами, за назвою першого представника.
За замісниковою номенклатурою ІЮПАК назви дво- та триатомних спиртів утворюють від назви відповідного вуглеводню, додаючи суфікс – діол чи -тріол, позначаючи цифрами положення гідроксильних груп.
Фізичні властивості.
Етиленгліколь та гліцерин – безбарвні в’язкі рідини, з високою температурою кипіння, солодкі на смак. Змішуються у всіх співвідношеннях з водою та етиловим спиртом.
Хімічні властивості.
Багатоатомні спирти вступають в ті ж реакції, що й одноатомні; реакції відбувають за участю однієї або декількох гідроксильних груп. Наявність різної кількості гідроксильних груп в спиртах визначає і деякі їх особливості.
1. Кислотні властивості. Порівняно з одноатомними спиртами, багатоатомні спирти виявляють сильніші кислотні властивості. Це зумовлено електроноакцепторним впливом гідроксильних груп одна на одну і, як наслідок, більшою поляризацією зв’язку О–Н. Так, багатоатомні спирти утворюють алкоголяти не лише при взаємодії з лужними металами, але і з гідроксидами, в тому числі, важких металів.
Етиленгліколь при взаємодії з натрієм, залежно від співвідношення реагентів, утворює як повні так і неповні гліколяти:
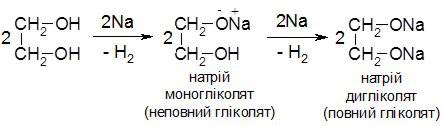
Утворення гліколятів спостерігається і при взаємодії з натрій гідроксидом:
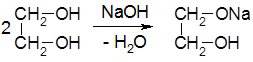
Особливістю багатоатомних спиртів є їх здатність розчиняти купрум (ІІ) гідроксид, при цьому з’являється характерне синє забарвлення розчину. При взаємодії багатоатомних спиртів з Cu(OH)2утворюються комплексні сполуки, у яких поряд з ковалентними зв’язками Cu–O є і донорно-акцепторні зв’язки Cu← O:
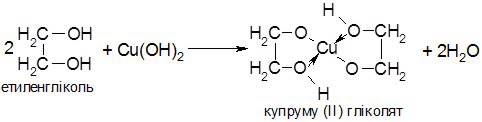
Такі внутрішньомолекулярні сполуки називають хелатними комплексами (гр. chelae – клешні); молекули етиленгліколю захоплюють атом металу, як клешнями. Взаємодія з Cu(OH)2– якісна реакція на багатоатомні спирти.
2. Утворення естерів. Етиленгліколі та гліцерин, як і одноатомні спирти, здатні утворювати естери з мінеральними та карбоновими кислотами.
Найбільше значення має повний естер гліцерину з нітратною кислотою:
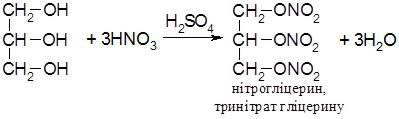
Тринітрат гліцерину або тринітрогліцерин – важка масляниста рідина, яку застосовують у виробництві ліків та вибухових речовин.
Естери гліцерину та вищих карбонових кислот – жири, тваринного та рослинного походження. Насичені кислоти входять до складу твердих жирів, а ненасичені – до складу олій.
Феноли – гідроксильні похідні ароматичних вуглеводнів, у яких гідроксильна група безпосередньо зв’язана з бензольним ядром.
Сполуки, що містять гідроксил в боковому ланцюзі, відносять до ароматичних спиртів.
Як і спирти, феноли можуть містити одну, дві, три або більше гідроксильних груп. При наявності в молекулі кількох ароматичних ядер з відповідними оксигрупами виникають поліфеноли. Найпростішим фенолом є власне фенол, або карболова кислота, могутній дезинфекційний засіб.
Найпростішими представниками фенолів є гідроксибензен або фенол; найближчі його гомологи о-, м-, п- крезоли:
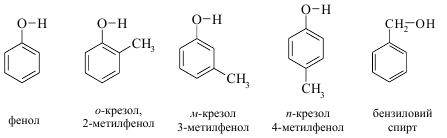
Бензиловий спирт (ароматичний) – ізомер крезолів. Це – міжкласова ізомерія.
Якісна реакція на феноли. Якісною реакцією на фенол є його кольорова реакція із ферум (ІІІ) хлоридом: безбарвний розчин фенолу реагує зі світло-жовтим ферум (ІІІ) хлоридом з утворенням темносинього ферум феноляту: 3С6Н5ОН + FeCl3 = (C6H5O)3 + 3HCl
До дифенолів відносять пірокатехін, резорцин і гідрохінон:
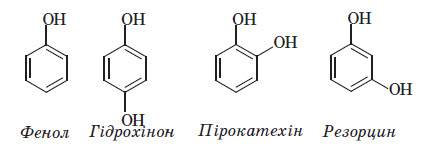
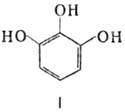
Найбільше значення мають трьохатомні феноли з рядовим і симетричним розташуванням гидрок-силов — пірогалол і флороглюцин. Пірогалол, або 1, 2, 3-тригідроксибензол або пірогалова к-та.
| |
З FeCl3 пірогалол дає червоне забарвлення. Для якісного визначення пірогалолу використовують реакцію з Fe2(SO4)3(синьо-фіолетове забарвлення) або з гліцерином в сернокислотной середовищі (червоно-фіолетове забарвлення, посилення при нагр.). Пірогалол дуже легко окислюється. Наприклад, лужні розчини його на повітрі швидко буріють внаслідок окислення. З солей срібла пірогалол негайно виділяє металеве срібло.
Флороглюцин існує у вигляді двох таутомерних форм: форми з трьома гідроксигрупами і форми з трьома карбонильними групами: 1, 3, 5-тригідроксибензен, 1, 3, 5-бензенетриол або циклогексан-1, 3, 5-трион:
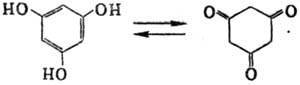
Флороглюцин досить легко окислюється, але набагато більш стійкий до окислення, ніж пірогалол.
Триоксибензени виявляють по кольоровим р-ціям: 1, 3, 5-триоксибензен з FeCl3 дає синьо-фіолетове забарвлення.
Завдання для самоконтролю:
1. Напишіть структурні формули (не менш як чотири) ізомерних двохатомних спиртів складу С5Н12О2. Врахуйте, що сполука, у молекулі якої біля одного атома Карбону знаходяться дві гідроксильні групи, нестійка й у вільному стані не існує.
2. У пробірках без етикеток знаходяться гліцерин і фенол. Як хімічним способом виявити кожну з цих речовин? Напишіть рівняння відповідних хімічних реакцій.
3. Зобразіть структурні формули за наведеними нижче назвами спиртів:
а) 2, 2 – дибром – 3, 4, 5 – трихлоргептан – 3, 5 – диол; б) 2 – хлор – 3 – гептан – 2, 5 – диол;
4. Гліцерин реагуватиме з: а) водою; б) натрієм; в) купрум (ІІ) гідроксидом.
5. Структурним формулам відповідають:

|
|
