
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Рибозимы как лекарственные средства
|
|
На основании результатов рассмотренных опытов, а также других накопленных знаний о рибозимах складывалось мнение о принципиальной возможности использования рибозимов для регуляции активности конкретных генов человека. Область применения рибозимов как лекарственных средств может быть весьма широкой. В качестве возможных сфер их использования в клиниках в настоящее время рассматривают лечение вирусных инфекций, онкологических заболеваний, для которых известны продукты онкогенов, а также патологических состояний организма, вызываемых сверхэкспрессией конкретных генов.
Лечение вирусных заболеваний. Большие усилия предпринимаются для использования рибозимов в лечении СПИДа, вызываемого вирусами иммунодефицита человека (ВИЧ). Уже в 1990 г. Н. Сарвер и соавторы продемонстрировали возможность расщепления геномной ВИЧ-РНК с помощью рибозима in vitro в бесклеточной системе, что сопровождалось снижением уровня р24-антигена на 98%. Длительные эксперименты на культурах клеток показали, что клетки, экспрессирующие такие рибозимы, не изменяли своего обычного фенотипа на протяжении, по крайней мере, 9 месяцев. Одновременно с этим было показано, что клетки линии MT4, стабильно трансфецированные вектором, экспрессирующим рибозим под контролем промотора гена тимидинкиназы вируса простого герпеса, были частично устойчивы к ВИЧ-инфекции. Полностью устойчивыми к заражению ВИЧ оказались клетки, содержащие рибозим под контролем вирусного регуляторного элемента tar, в которых вирус не обнаруживали даже через 22 дня после заражения. В этих клетках высокий уровень индукции синтеза рибозима происходит как раз во время ВИЧ-инфекции. Та же самая стратегия была применена и к рибозимам, образующим структуру типа шпильки. Экспрессия гена рибозима под контролем промотора гена b-актина подавляла ВИЧ-инфекцию в культивируемых клетках. При этом продукты расщепления ВИЧ-РНК в таких клетках специфически и быстро деградировали.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
Еще одним подходом к преодолению ВИЧ-инфекции является отщепление 5’-концевой кэп-структуры ВИЧ-РНК с помощью рибозимов. Известно, что у большинства изолятов ВИЧ 5’-концевая лидерная последовательность их геномной РНК высококонсервативна. Из всех известных изолятов только штамм MN содержит замену одного нуклеотида в лидерной области РНК, расщепляемой рибозимом. В то же время исследованные штаммы ВИЧ различаются по другим участкам 5’-концевой лидерной последовательности. Эндонуклеазное удаление в составе олигонуклеотида 5’-концевой кэп-группы РНК ВИЧ подавляет трансляцию РНК и делает ее более доступной мишенью для внутриклеточных нуклеаз. Все имеющиеся экспериментальные данные позволяют сегодня сделать вывод о перспективности использования 5’-концевой лидерной последовательности ВИЧ-РНК в качестве мишени для рибозимов.
Основной сложностью, которую приходится преодолевать при конструировании рибозимов, расщепляющих геномную ВИЧ-РНК, является высокая мутабильность этих РНК. Из-за мутационных замен отдельных нуклеотидов в сайтах, по которым происходит расщепление РНК рибозимами, последние утрачивают свою активность по отношению к этим РНК и соответственно противовирусную активность. Новейшая стратегия в решении данной проблемы заключается в создании нескольких рибозимов, действие которых направлено против разных консервативных участков генома ВИЧ, причем отдельные рибозимы должны входить в одну молекулу рекомбинантной РНК (" метод дробовика"). Помимо последовательностей антивирусных рибозимов такие рекомбинантные РНК содержат в себе дополнительные cis -действующие рибозимы, которые осуществляют аутокаталитический процессинг предшественников антивирусных рибозимов с освобождением зрелых рибозимов, действующих на разные участки вирусного генома. Этот метод не позволяет вирусу ВИЧ избежать инактивирующего действия рибозимов путем мутационных преобразований своего генома.

Рис. II.26. Использование сайтов рестрикции для конструирования рибозима, интегрированного в антисмысловую РНК
Недавно была получена кассета из девяти идентичных генов рибозимов, расположенных друг за другом в одном экспрессирующем векторе. Рибозимы такой " полицистронной" РНК, направленные против разных частей ВИЧ-генома, сохраняли внутри клетки свою специфичность, но были более эффективными в пересчете на одну копию РНК полирибозима и не утрачивали своей активности даже в частично деградировавших молекулах РНК.
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе

Рис. II.27. Взаимодействие рибозима с РНК-субстратом
В заключение этого раздела рассмотрим пример использования рибозимов против вирусов растений в сельском хозяйстве. Как упоминалось выше, рибозимы, образующие структуру типа " головки молотка", распознают в сайте расщепления РНК-мишени последовательности из трех нуклеотидов, рядом с которой происходит гидролиз цепи РНК. Подобными тринуклеотидами могут быть последовательности AUC, CUA, CUC, GUA, GUC, GUU и UUC. В предложенном подходе РНК-связывающий домен рибозима конструируют таким образом, что распознаваемый тринуклеотид входит в состав последовательности нуклеотидов, которая в двухцепочечной ДНК образует сайт рестрикции. Подобный подход дает возможность встраивать последовательность каталитического домена рибозима по этому сайту рестрикции в кДНК, полученную путем обратной транскрипции РНК-мишени. Следовательно, каталитический домен рибозима оказывается фланкированным последовательностями антисмысловой РНК, комплементарной РНК-мишени, которые автоматически выполняют роль РНК-связывающего домена. При таком подходе отпадает необходимость в синтезе большого числа олигонуклеотидов, и в любом необходимом случае рибозим собирается из готовых блоков. В качестве конкретного примера рассмотрим создание рекомбинантного рибозима, специфически расщепляющего РНК, содержащую последовательность сайта рестрикции Sal I (рис. II.26). После расщепления кДНК рестриктазой Sal I (этап 1) образовавшиеся " липкие" концы гидролизуют нуклеазой S1 (этап 2) и по образовавшимся " тупым" концам встраивают каталитический домен рибозима, заключенный в двухцепочечном фрагменте ДНК (этап 3). В результате транскрибирования такой конструкции синтезируется антисмысловая РНК, в состав которой включен каталитический домен рибозима. После гибридизации с РНК-мишенью образуется двухцепочечная молекула РНК, на одной из цепей которой формируется структура рибозима типа " головки молотка" (рис. II.27), расщепляющего РНК-мишень в строго определенном месте. Описанный подход был реализован при конструировании рибозима, направленного против геномной РНК одного из вирусов сливы. При этом были получены последовательности нуклеотидов рибозима, пригодные для использования с другими 25 сайтами рестрикции.
Подавление функционирования онкогенов. Одними из основных различий, обнаруживаемых между нормальными и раковыми клетками, являются генетические различия ряда генов, контролирующих пролиферацию. В геноме опухолевых клеток часто обнаруживают мутации в генах двух типов: онкогенах и генах-супрессорах опухолевого роста, или антионкогенах. Онкогены эволюционно консервативны и вызывают неопластическую трансформацию клеток как при ретровирусной инфекции в природных условиях (поскольку они часто бывают включены в состав генома ретровирусов), так и после введения ДНК онкогенов в культивируемые клетки с помощью трансфекции. Большинство онкогенов вначале было обнаружено именно в составе генома онкогенных вирусов, и они являются мутантными производными протоонкогенов, присутствующих в здоровых клетках многоклеточных организмов и активирующихся во время эмбриогенеза, роста клеток или регенерации тканей. Поскольку активированные онкогены в опухолевых клетках, как правило, сверхэкспрессируются и кодируемая ими РНК по своей первичной структуре отличается от РНК протоонкогенов, РНК онкогенов являются хорошей потенциальной мишенью для рибозимов.
Онкоген H-ras. Мутация в кодоне 12 гена H -ras, приводящая к замене GGC®GUC, создает консенсусный сайт, по которому HH-рибозим может расщеплять мутантную мРНК. In vitro было продемонстрировано пятикратное различие в эффективности действия рибозима на мутантную H -ras -РНК и соответствующую РНК дикого типа. Получены H -ras -зависимые линии клеток, стабильно трансформированные экспрессирующим вектором, который направлял синтез HH-рибозима под контролем промотора b-актинового гена. Для таких клеток характерна пониженная скорость пролиферации, сопряженная с уменьшением внутриклеточных уровней H -ras -РНК и белка р21, кодируемого этим геном. Далее рибозим экспрессировали в клетках линии EJ карциномы мочевого пузыря человека. Введение исходных клеток мышам сопровождалось их быстрой гибелью на фоне развития высокоинвазивных опухолей. В отличие от этого клоны EJ-клеток, экспрессирующих рибозим, в организме мышей обладали резко сниженным опухолевым фенотипом. Образующиеся опухоли были малоинвазивны, и наблюдалось приблизительно двукратное повышение уровня выживаемости мышей с трансплантатами. Гистологические исследования подтверждали слабую способность опухолей к метастазированию. Рибозимы в опухолях обнаруживались методом ПЦР на протяжении 86–90 дней. Таким образом, эти и ряд других экспериментов показали способность рибозимов нормализовать экспрессию активированного H -ras как in vitro, так и in vivo.
Онкоген c-fos. Как уже упоминалось в первой части книги, белковый продукт гена c-fos участвует в передаче сигнала эукариотическими клетками, вовлечен в синтез ДНК и может придавать клеткам устойчивость к противоопухолевым препаратам. Последние два свойства этого белка находят подтверждение, в частности в том факте, что при проведении лечения часто используемым противоопухолевым лекарством цисплатином (цис- диаминодихлорплатина) происходит индукция гена c-fos вслед за генами dTMP-синтазы и ДНК-полимеразы. Рибозим, разрушающий c-fos -мРНК, снижал конечный уровень экспрессии гена c-fos, приводил к повышению чувствительности опухолевых клеток к химиотерапевтическим агентам (включая цис- платину) и значительно подавлял экспрессию генов dTMP-синтазы, ДНК-полимеразы b и гена металлотионеина человека hMTII-A.
Онкогены bcr/abl. Аберрантная филадельфийская хромосома образуется в результате транслокации (9; 22)(q34; q11) в стволовых клетках костного мозга, что сопровождается слиянием генов bcr и abl с образованием химерного онкогена bcr/abl и развитием хронических миелоидных лейкозов (ХМЛ). Транскрипт химерного гена кодирует белок р210bcr/abl, который обладает повышенной активностью тирозинкиназы. Такие РНК и белок обнаруживаются почти у всех больных с синдромом ХМЛ, а также у 50% пациентов с острым лимфобластоидным лейкозом, у которых имеется филадельфийская хромосома. С помощью рибозимов, специфически расщепляющих последовательность химерной мРНК в месте стыковки последовательностей двух генов, удалось подавить экспрессию химерного гена bcr/abl в культивируемых клетках. Экспрессия рибозимов в культивируемых клетках вызывала снижение уровня bcr/abl -мРНК, полностью блокировала образование химерного белка р210bcr/abl и ингибировала рост клеток на 84%. Эти результаты были значительно лучше эффектов, вызываемых антисмысловыми олигонуклеотидами.
В работах других исследователей был получен рибозим, расщепляющий вышеупомянутую химерную РНК по кодону GUU, расположенному по соседству с местом стыковки последовательностей двух генов. Этот рибозим разрушал соответствующую РНК in vitroиin vivo, а также подавлял тирозинкиназную активность белка р210.
9.2.4. Репарация мутантных РНК с помощью рибозимов, осуществляющих транс- сплайсинг
Просто устроенные HH- и HP-рибозимы принято рассматривать как рибозимы первого поколения. Во всех примерах, рассмотренных выше, в прикладных целях использовалась их способность осуществлять специфическое эндонуклеазное расщепление молекул РНК. Недавно (Дж. Т. Джонс и др., 1996 г.) удалось приспособить рибозимы для восстановления генетической информации на уровне молекул РНК, структура которых нарушена мутациями. Рибозим интрона группы I Tetrahymena после незначительных генно-инженерных модификаций оказался способным выполнять такие репарирующие функции.
Как уже обсуждалось в первой части книги (см. раздел 2.2.3), аутосплайсинг транскриптов, содержащих интроны группы I, начинается с расщепления фосфодиэфирной связи между 5’-концевым экзоном и прилегающим к нему интроном, сопровождаемого полным удалением интрона и лигированием фланкирующих его экзонов, приводящим к восстановлению непрерывной структуры РНК. Идея, лежащая в основе использования рибозимов для репарации РНК, проста. Достаточно лишь с помощью генно-инженерных методов к 3’-концу рибозима присоединить вместо 3’-концевого экзона любую другую последовательность, чтобы она соединялась с последовательностью 5’-концевого экзона в строго определенной точке с образованием гибридной молекулы РНК. Поскольку сайт взаимодействия рибозима с РНК во время транс- сплайсинга и положение точки разрыва РНК целиком определяются внутренней направляющей последовательностью рибозима (internal guide sequence – IGS), присоединение новой 3’-концевой последовательности можно осуществлять практически в любом месте РНК-мишени (рис. II.28). Таким образом, для репарации мутационного повреждения в экзоне 2 на уровне РНК IGS делают комплементарной участку РНК-мишени, локализованному выше точки повреждения (в рассматриваемом примере – А) на стыке экзонов 1 и 2. Экзон 2 дикого типа соединяют с рибозимом, который после взаимодействия с РНК-мишенью вырезает из нее мутантную последовательность экзона 2 и заменяет на эквивалентную последовательность дикого типа. В результате комплекс рибозима и репарированной РНК распадается и обновленная РНК вовлекается в трансляцию.
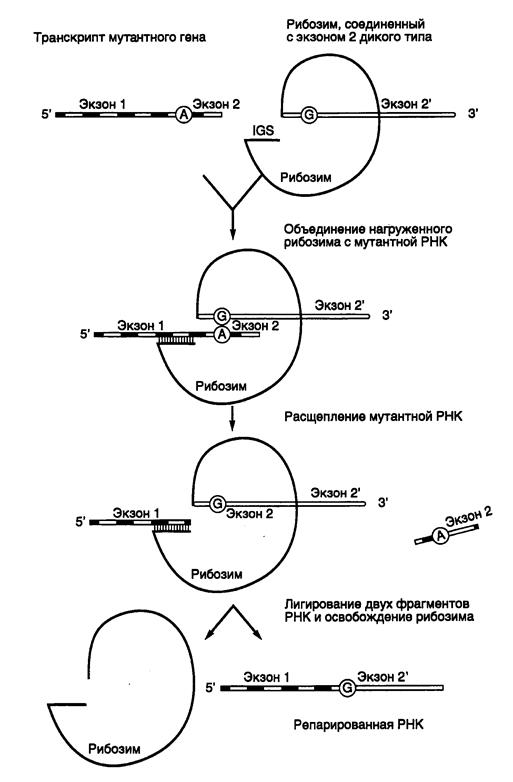
Рис. II.28. Схема репарации мутантной мРНК рибозимом, осуществляющим транс- сплайсинг
Молекула рибозима, соединенная 3’-концом с последовательностью экзона 2 дикого типа, взаимодействует с мутантной РНК выше мутантного нуклеотида и замещает мутантную часть репарируемой РНК в реакции аутосплайсинга
Такой подход был успешно использован для репарации мРНК гена lacZ как в клетках E. coli, так и в культивируемых клетках животных. Точность транс- сплайсинга, направляемого рибозимом, оказалась абсолютной – в образующихся восстановленных молекулах РНК не наблюдали сдвига рамки считывания. Однако в этих опытах на первый план вышла другая проблема. Длина IGS-последовательности, определяющей специфичность взаимодействия рибозима с РНК, составляет всего шесть нуклеотидов. Такая последовательность из шести нуклеотидов в молекулах РНК встречается достаточно часто (каждые 4096 оснований). Следствием этого было объединение репарирующего фрагмента РНК не только с РНК-мишенью, но и другими РНК, не имеющими отношения к первой. Выход из сложившейся ситуации ищут в увеличении специфичности действия рибозима путем удлинения IGS. Однако с увеличением длины области комплементарного взаимодействия между рибозимом и РНК будут возрастать прочность этого взаимодействия и, как следствие, затруднение последующего распада каталитического комплекса, что должно сопровождаться ингибированием реакции.
Применение рибозимов в реакциях транс- сплайсинга для корректировки экспрессии мутантных генов на посттранскрипционном уровне рассматривается как весьма перспективное направление в генотерапии. И хотя более логичной все-таки кажется необходимость репарации мутаций на уровне самих генов, такой подход, возможно, получит право на жизнь и в клиниках. По сути дела он является прототипом реакции редактирования РНК (см. раздел 2.2.2), который эффективно используется клетками при экспрессии ряда генов в природных условиях.
Благодаря генной инженерии введение в молекулярную генетику антисмысловых РНК и рибозимов привело к появлению высокоспецифичного инструмента для изучения функциональной роли и регуляции экспрессии индивидуальных генов in vivo. Использование этих методов представляется особенно перспективным в исследованиях по биологии и генетике развития, так как именно здесь инактивация отдельных генов соматических клеток представляется особенно сложной задачей. Плодотворным подходом является объединение последовательностей антисмысловых РНК с рибозимами, поскольку в результате получаются каталитически действующие, высокоспецифические супрессоры генов, а также конструкции, корректирующие экспрессию генов на посттранскрипционном уровне. Полагают, что дальнейшее развитие техники адресной доставки генов антисмысловых РНК, направленных против патогенных вирусов, в клетки зародышевой линии животных и растений может привести к созданию сортов растений и пород животных, устойчивых к действию патогенных вирусов, и дать большой экономический эффект в сельском хозяйстве. Однако хорошо известно, что на любое лекарство у возбудителя заболевания всегда находится адекватный защитный ответ. Поэтому до тех пор, пока генотерапия не будет опираться на самонастраивающиеся генетические системы, что имеет место, например в случае иммунной системы, победа, в конечном счете, будет оставаться за возбудителем. Нельзя не учитывать и возможное использование антисмысловых РНК в будущем для генотерапии как инструмента воздействия на онкогены и другие генные локусы, повышенный уровень экспрессии которых вредно сказывается на жизнедеятельности соматических клеток многоклеточных организмов. Первые результаты, полученные при разработке некоторых из этих направлений молекулярной генетики, кратко изложены в главе 11.
|
|
