
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
⚡️ Для новых пользователей первый месяц бесплатно. А далее 290 руб/мес, это в 3 раза дешевле аналогов. За эту цену доступен весь функционал: напоминание о визитах, чаевые, предоплаты, общение с клиентами, переносы записей и так далее.
✅ Уйма гибких настроек, которые помогут вам зарабатывать больше и забыть про чувство «что-то мне нужно было сделать».
Сомневаетесь? нажмите на текст, запустите чат-бота и убедитесь во всем сами!
Повышение информационной стабильности генома избыточными последовательностями
|
|
Анализ структуры генома современных эукариот показывает, что эволюционные преобразования генома-предшественника, приведшие к включению в него избыточных последовательностей нуклеотидов, сопровождались важными генетическими изменениями в отношении стабилизации генетической информации. В частности, многократное превышение содержания избыточных последовательностей нуклеотидов над кодирующими неизбежно должно приводить к соответствующему уменьшению вероятности возникновения мутаций в кодирующих и других функционально значимых частях под действием внутриядерных мутагенов эндогенного и экзогенного происхождения. Поскольку в разных частях интерфазного ядра (микрокомпартментах, заключающих в себе хромомеры интерфазных хромосом) наблюдается гетерогенность в уровнях конденсации хроматина, индивидуальные локусы могут быть по-разному защищены от мутационных изменений, вызываемых мутагенами. Рассмотрим более подробно влияние избыточных последовательностей ДНК генома эукариот на стабильность их генома.
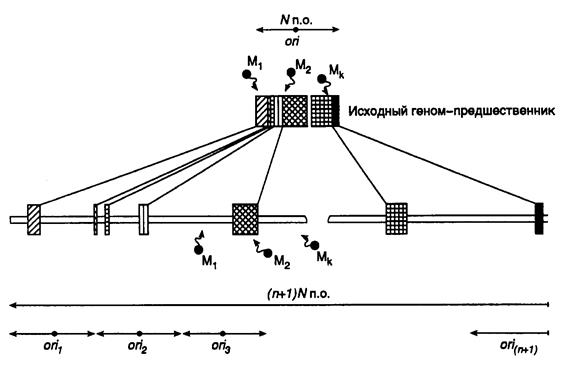
Рис. I.63. Гипотетическое эволюционное преобразование генома-предшественника путем включения в него некодирующих избыточных последовательностей нуклеотидов
Влияние избыточных последовательностей нуклеотидов на число мутаций, возникающих в результате ошибок репликации в кодирующих последовательностях генома. Предположим, что длина исходного генома, не содержащего избыточных последовательностей нуклеотидов, составляет N п.о. (см. рис. I.63). При этом в результате ошибок репликации в нем, в среднем, возникает a мутаций независимо одна от другой и случайным образом. Допустим, что в ходе эволюционных преобразований в него включаются избыточные последовательности нуклеотидов, суммарная длина которых составляет nN п.о. и, соответственно, общая длина преобразованного генома становится равной (n+ 1) N п.о. Поскольку число мутаций, возникающих в результате ошибок репликации, прямо пропорционально длине реплицирующейся ДНК, общее количество мутаций, в среднем, возникающих в преобразованном геноме при участии этого механизма, должно возрасти в n+ 1 раз и составить a (n+ 1). Вероятность возникновения одной независимой и случайной мутации в некодирующей части генома P(1) будет пропорциональна его длине:
P(1) =  =
=  . (1)
. (1)
В то же время вероятность возникновения в избыточных частях генома всех a (n+ 1) мутаций будет равна:
P[a(n+1)] = 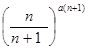 (2),
(2),
поскольку вероятность одновременного наступления a (n+ 1) независимых событий равна произведению вероятностей наступления каждого из них в отдельности.При a = 1 (т.е. в том случае, если в процессе репликации исходного генома в нем, в среднем, возникала одна мутация) и достаточно больших значениях n это выражение стремится к e-1, т.е. к ~0, 36. Таким образом, в данном случае при n = 100 (что, приблизительно, соответствует соотношению некодирующих и кодирующих последовательностей нуклеотидов в геноме человека и других млекопитающих) вероятность того, что ни одна из мутаций, возникающих в гипотетическом преобразованном геноме в результате ошибок репликации, не произойдет в его кодирующих частях, будет довольно высокой и составит ~ 0, 37. Это означает, что, в среднем, каждая третья дочерняя соматическая или половая клетка, возникшая в результате редупликации гипотетического генома с достаточным количеством некодирующих избыточных последовательностей нуклеотидов, будет полностью свободна от мутаций, образующихся по такому механизму в кодирующих частях своего генома.
С увеличением числа мутаций в исходном геноме-предшественнике (a > > 1) вероятность возникновения всех мутаций в некодирующих частях генома быстро уменьшается. Однако поскольку эти мутации будут распределяться между кодирующими и некодирующими частями генома пропорционально длине каждой из этих частей, общее их количество в кодирующих частях генома останется неизменным. Следовательно, эволюционное включение в геном-предшественник большого количества некодирующих последовательностей нуклеотидов не увеличивает число мутаций, возникающих в кодирующих частях генома в результате ошибок репликации. Более того, в ряде случаев такое эволюционное преобразование генома может заметно стабилизировать его генетическую информацию.
Влияние избыточных последовательностей нуклеотидов на число мутаций, возникающих в кодирующих частях генома под действием мутагенов. Ситуация, связанная с возникновением мутаций в гипотетическом геноме под действием мутагенов экзогенного и эндогенного происхождения, принципиально отличается от только что рассмотренной (см. рис. I.63). Если предположить, что эволюционное преобразование генома, приведшее к включению в него n некодирующих последовательностей нуклеотидов, не сопровождается увеличением числа внутриядерных мутагенов, то генетические последствия такого преобразования будут гораздо более значительными.
Так же как и в предыдущем случае, вероятность попадания одного мутагена Mk в некодирующую область гипотетического генома равна  . Вероятность же того, что все k мутагенов попадут в некодирующие области нового генома P(k), равна:
. Вероятность же того, что все k мутагенов попадут в некодирующие области нового генома P(k), равна:
P(k) = 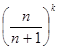 (3).
(3).
При больших значениях n и малых k величина P(k) стремится к 1, 0, т.е. имеет место событие, близкое к достоверному. Иными словами, чем больше доля некодирующих последовательностей нуклеотидов в геномной ДНК, тем вероятнее, что все внутриядерные мутагены попадут в некодирующие последовательности. В случае гипотетического генома с n = 100 вероятность попадания одного мутагена в кодирующую область становится равной 0, 01, т.е. весьма малой. При этом общее число мутагенов, которые будут взаимодействовать с кодирующими последовательностями нуклеотидов, уменьшится в 100 раз и будет иметь место 100-кратная защита кодирующих функционально значимых участков эволюционно преобразованного генома от мутаций, вызываемых внутриядерными мутагенами, по сравнению с исходным геномом-предшественником. При k = n+ 1 с ростом n уравнение (3) будет стремиться к e-1, т.е. к ~0, 36, и быстро уменьшаться при дальнейшем увеличении k. Но это относится к вероятности полной защиты кодирующих последовательностей нуклеотидов. Относительная же защита, равная доле химических мутагенов из всего их пула, взаимодействующих с кодирующими последовательностями нуклеотидов, будет обратно пропорциональна общей длине избыточных последовательностей в преобразованном геноме, т.е. обратно пропорциональна n. Относительная защита генома от химических мутагенов может быть особенно актуальной в условиях экологического стресса.
Насколько соответствует действительности предположение о том, что эволюционное преобразование генома-предшественника путем включения в него большого количества избыточных последовательностей нуклеотидов не будет сопровождаться пропорциональным возрастанием количества внутриядерных мутагенов? Очевидно, что такое предположение является упрощением. Увеличение внутриядерного содержания ДНК, например в результате эндорепликации при политении, по-видимому, всегда приводит к пропорциональному увеличению объема соответствующих ядер, следствием чего, казалось бы, должно быть пропорциональное возрастание количества молекул внутриядерных мутагенов. Однако это не совсем так. Данный вывод относится лишь к мутагенам, непосредственно образующимся в ядре, например в результате взаимодействия ионизирующего излучения с веществом ядер. Большая же часть мутагенов, по-видимому, должна поступать в ядра из цитоплазмы путем радиальной диффузии через ядерные мембраны. При этом одним из факторов, ограничивающих попадание мутагенов из цитоплазмы в ядра, является их поверхность, поскольку вероятность контакта мутагенов цитоплазмы с ядром прямо пропорциональна площади его поверхности. При увеличении объема поверхность ядра-шара возрастает пропорционально квадрату его радиуса, тогда как объем – пропорционально кубу радиуса ядра. Следовательно, объем ядер будет увеличиваться быстрее площади их поверхности и количество молекул внутриядерных химических мутагенов, приходящихся на нуклеотид ядерной ДНК, должен уменьшаться при возрастании ядерного объема за счет увеличения содержания ядерной ДНК. Такое эволюционное преобразование генома в целом будет сопровождаться повышением его информационной стабильности.
Включение в геномную ДНК некодирующих последовательностей может приводить и к более специфической защите жизненно важных локусов генома от химических мутагенов. В частности, глобальная защита кодирующих последовательностей от химических мутагенов, поступающих из цитоплазмы в ядро путем радиальной диффузии, могла бы происходить в том случае, если бы некодирующие последовательности были преимущественно локализованы вблизи поверхности ядер и экранировали последовательности, расположенные ближе к их центральной части. В настоящее время имеются многочисленные экспериментальные данные, указывающие на высокоупорядоченное расположение последовательностей нуклеотидов ДНК в интерфазных ядрах. Значение пространственного расположения отдельных последовательностей ДНК интерфазных хромосом для избирательной, специфической защиты кодирующих последовательностей будет подробнее рассмотрено ниже.
|
|
