
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
⚡️ Для новых пользователей первый месяц бесплатно. А далее 290 руб/мес, это в 3 раза дешевле аналогов. За эту цену доступен весь функционал: напоминание о визитах, чаевые, предоплаты, общение с клиентами, переносы записей и так далее.
✅ Уйма гибких настроек, которые помогут вам зарабатывать больше и забыть про чувство «что-то мне нужно было сделать».
Сомневаетесь? нажмите на текст, запустите чат-бота и убедитесь во всем сами!
Специфические свойства аминокислот
|
|
Отношение к нагреванию. В этом они напоминают оксикислоты. α -Аминокнслоты образуют дикетопиперазин (межмолекулягныи циклический диамид):
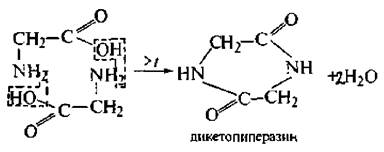
β -Аминокислоты при нагревании отщепляют аммиак и образуют непредельные кислоты:
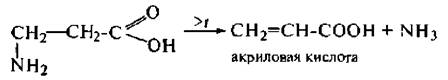
γ -Аминокислоты претерпевают внутримолекулярную дегидратацию с образованием циклических амидов – лактамов:
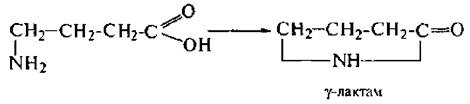
2. Для α -аминокислот характерно образование комплексных соединений с ионами меди (I).
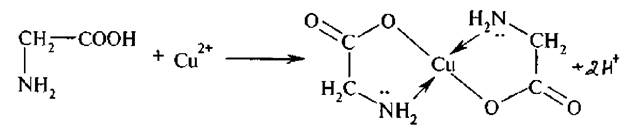
При этом образуется растворимый в воде устойчивый комплекс интенсивно синего цвета. Только α -аминокислоты дают подобную синюю окраску.
Значение аминокислот заключается в том, что они являются исходными веществами при построении белковых тел.
В состав белка входит 31 аминокислота, из них 30 а-аминокислот и одна р-аминокислота.
Отметим некоторые из аминокислот.
гликокол (глицин, аминоуксусная кислота)
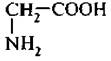
Относится к α -аминокислотам.
АЛАНИН (α -аминопропиововая кислота)
Различают α - и β -аланины, которые входят в состав белка.
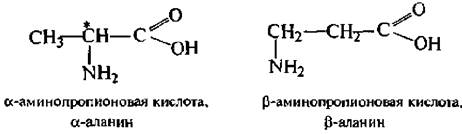
Молекула α -аланина содержит асимметричный атом углерода и существует в виде пары энантиомеров.
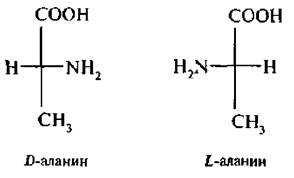
В построении молекулы белка принимает участие только L-аланин.
γ -АМИНОМАСЛЯНАЯ КИСЛОТА (ГАМК)
ГАМК содержится в клетках мозга и участвует в процессах торможения.
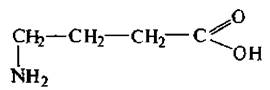
|
|
