
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
HCl H2 H2SO4
|
|
H2(г) + CI2(г) «2HCI(г) реакцияныњ тепе-тењдік константасын жазыњыз. NO
H2(г) + I2(к) Û 2HI(г) реакциясының тепе-тең дік константасының ө рнегін кө рсет: 125.95
H2O – H2S – H2Se – H2Te - қ атарда байланыс тұ рақ тылығ ы қ алай ө згередi? тө мендейді
H2S+H2SO3®S+H2O тотығ у – тотық сыздану реакциясын тең естiрiп тү зiлген кү кiрттiң моль санын анық таң ыз. 3
H2SO4 қ айсы затпен ә рекеттеседi? CuO
H2SO4-кү кiрт қ ышқ ылының молярлық массасы қ андай? 98
HCI-дың стандартты тү зілу жылуы 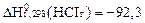 кДж/моль. Тө мендегі реакцияның стандартты жылу эффектісін есептең із: 2HCI(г) = H2 + CI2 NO
кДж/моль. Тө мендегі реакцияның стандартты жылу эффектісін есептең із: 2HCI(г) = H2 + CI2 NO
HCl ерітіндісі диссоциацияланғ анда қ анша ион тү зіледі? 2
HCl молекуласындағ ы химиялық байланыс тү рiн кө рсетініз:
КОВАЛЕНТТІ, ПОЛЮСТІ
Н+ ионының концентрациясын ең аз беретін қ ышқ ылды кө рсет:
HClO K(a)= 2.95*10^-8
Н2(г) + CI2(г) = 2HCI(г) реакциясыныњ тепе-тењдiк константалары (КР мен КС) ө зара ќандай байланыста болады? NO
KCl
KCl сулы ерітіндісін толық электролиздегенде анодта 2, 8 л газ бө лінді. Катодта бө лінген қ андай газ қ анша кө лемде бө лінді? 48
K2Cr2O7 тотық тырғ ыш болса, онда оның эквиваленті неге тең? 4
KMnO4+H2S+H2SO4®MnSO4+K2SO4+S¯ +H2O. Осы реакциядағ ы тотық тырғ ыштың моль санын табың ыз. 2
KMnO4+NaNO2+H2SO4®MnSO4+NaNO3+K2SO4+H2O тотығ у-тотық сыздану реакциясына қ атысатын электрондар санын анық таң ыз. 10
KMnO4+NaNO2+КОН®К2MnO4+NaNO3+H2O тотығ у-тотық сыздану ряакциясындағ ы тотық тырғ ыштың моль санын табың ыз. 2
Mg
MgCl2 ерiтiндiсiн электролиздегенде катодта бө лiнетiн зат: H2
Mg0+HNO3®Mg(NO3)2+NH4NO3+H2O реакция тең деуiн аяқ тап, тотық сыздандырғ ыш алдындағ ы коэффициентiн анық таң ыз: 4
Мg + HNO3 ® Мg (NO3)2 +NH4 NO3 +H2O реакциясындағ ы тотық тырғ ыштың реакцияғ а дейінгі жә не реакциядан кейінгі тотығ у дә режелерін кө рсет: NO
Mg(NO3)2 тұ зы ерiтiндiсi электролизiнде анодта бө лiнетiн затты кө рсетiң iз. O2
(MnOH)2SO3 тұ зы қ алай аталады? Марганец гидро сульфит
MgCO3(қ) Û MgO(қ) + CO2 (г) реакциясының тепе-тең дік константасының ө рнегін жазың ыз: -130
N
1 2 3 4
N2 ® NH3 ® NH4Cl ® NH3 ® N2
Қ айсы реакцияда температураны арттыру қ ажет. 1.3.4
N2 + 3H2 «2NH3 реакциясында тепе-тењдік орнаѓандаѓы заттар концентрация-лары: [N2] = 0, 03 моль/л, [H2] = 0, 10 моль/л, [NH3] = 0, 4 моль/л. Тепе-тењдік константасын есептењіз. 0.5
N2-молекуласында қ анша p-байланысы бар? БАРЛЫҒ Ы π, 2π БАР
Na2O2+CO2®Na2CO3+O2 реакцияның қ ай типiне жатады: ДИСПРОПОРЦИЯЛАНУ
NaNO3 ерiтiндiсiн электролиздегенде катод пен анодта бө лiнетiн заттар: H2, O2
NaCrO2 + Br2 + NaOH® NaCrO4 + NaBr + H2O реакциясының сол жақ бө лігінің қ осындысын кө рсет: 2
NaCl балқ ымасының электролизi кезiнде катодта қ андай процесс жү редi? Егер I=10 A, t=1сағ, F=96500 Кл. болса, онда катодта тү зiлетiн заттың массасы: 8.85
NaNO3 и K2SO4 тұ здары ерiтiндiлерiнiң қ оспаларын электролиздегенде электродта бө лiнетiн заттарды кө рсетiң дер. H2, O2
NO2(г)Û N2O(г) реакциясының температура 298К кезiндегi стандартты жылу эффектiсiн табың ыз, егер DH0298 N2O(г)=+9, 4 кДж/моль, DH0 298 NO2(г) =+33, 9 кДж/моль болса. 58, 4
NH3(г)+HCl(г)=NH4Cl(к) реакциясы DG0298NH3=-16, 48 кДж/моль,
DG0298HCl(г)=-95, 3 кДж/моль, DG0298NH4Сl=-203, 22 кДж/моль болғ анда стандартты жағ дайда ө з бетiнше жү ре ала ма? -91, 44
NH4+ ионы тү зiлуi кезiнде қ айсы атом немесе ионның электрон жұ бы донор қ ызметiн атқ арады? N
NaBr+NaBrO3+H2SO4®Br2+Na2SO4+H2O тотығ у-тотық сыздану реакциясындағ ы тотық тырғ ыштың моль санын анық таң ыз. 2
NaCrO2+PbO2+2NaOH®Na2PbO2+NaCrO4+2H2O тотығ у-тотық сыздану реакция-сындағ ы тотық тырғ ыштың моль санын анық таң ыз. 2
NaOH-пен ә рекеттесетiн затты кө рсетiң iз? HCl
Na3PO4 толық диссоциаланғ анда тү зiлетiн ион саны: 4
S
S2- -ионына сә йкес келетiн электрондық формула: 3S2 3P6
S2- ионына қ андай электрондық формула сә йкес келедi? 3s2 3p6
Sn2+ ионының электрондық формуласын кө рсет: +50 2 8 18 18 3
SO2 + 0, 5O2 «SO3; 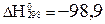 кДж/моль, реакциясы бойынша SO3-њ шыѓымын арттыру ү шін ќандай параметрлерді ќалай ө згерту керек? NO
кДж/моль, реакциясы бойынша SO3-њ шыѓымын арттыру ү шін ќандай параметрлерді ќалай ө згерту керек? NO
Zn
Zn/Zn+2 j0=-0, 76 B мен сутектiк электрод j0=0, 00 жартылай элементтен тұ ратын гальваникалық элементтiң Э.Қ.К. неге тең? +0.76
Zn2+ ионының электрондық конфигурациясын жазың ыз. 1S2 2S2 2P6 3S2 3P6 3D10
Zn/Zn2+ (0, 01 моль/л) // Cd2+ (0, 01 моль/л)/Cd гальваникалық элементiнiң E0Cd2+/Cd=-0, 43 B; E0Zn2+/Zn=-0, 76 B болса, онда ЭҚ К неге тең? +0, 33B
Zn/Zn2+ (0, 01 моль/л) // Ag+ (0, 01 моль/л)/Ag гальваникалық элементiнiң E0Zn2+/Zn=-0, 76 В; E0Ag+/Ag=+0, 80 B болса, онда ЭҚ К неге тең? +1, 56B
САНДАР
0, 01М HNO3 ерiтiндiсiнiң рОН мә нiн есептең iз. 12
0, 01М КОН ерiтiндiсiнiң рН мә нiн есептең iз. 12
0, 01М ZnSO4 тұ зы ерiтiндiсiндегi мырыштың электрод потенциалын есептең iз:
E0Zn2+/Zn = - 0, 76B. -0.28
0, 01М CuSO4 ерiтiндiсiндегi мыстың электродтық потенциалын (В) анық таң ыз: E0Cu2+/Cu=+0.34B. 0.28
0, 25М NaOH ерiтiндiсiнiң титрiн анық таныз. 0.01
0, 25 моль молекулалық хлордағ ы хлордың атомдық саны: 1
0, 5 моль кү кiрт қ ышқ ылының массасы (г) қ андай? M(H2SO4)=98 г/моль 49
0, 5 моль сутегiнiң (қ.ж.) кө лемiн анық таң ыз. 11, 2
0, 5 л 1Н Na2SO4 ерiтiндiсiн дайындау ү шiн қ анша грамм Na2SO4 ө лшеп алу керек?
1 л натрий сульфатында 0, 5 моль сульфат бар. Осы ерітіндінің 1л қ анша натрий ионы болуы мү мкін? 6.02*10^23
1 литр қ ұ рамында 49 г H2SO4 бар. Осы ерiтiндiнiң нормальдық концентрациясы неге тең? Mr(H2SO4)=98 г/моль. 1
1 л ерiтiндiде 6, 3 г HNO3 (М.м.=63 г/моль) ерiтiлген. Осы ерiтiндiнiң молярлық концентрациясын анық таң ыз. 0.1
1 мл 40%-тiк ерiтiндiде 0, 45 г ерiген зат бар. Ерiтiндiнiң тығ ыздығ ын табың ыз.
1.125 г/мл 0.1
1 литр ерiтiндiде 98 г H2SO4 болса (MH2SO4=98 г/моль) осы ерiтiндiнiң молярлық концентрациясы қ андай? 1М
1 сағ бойы AlCl3 балқ ымасынан 13, 4 А. ток жiбергенде бө лiнетiн алюминийдiң массасы: 4.5
11, 2 л кө мiртегi (IV) оксидiнiң қ алыпты жағ дайдағ ы мө лшерi нешеге тең? 0, 5
100 мл ерiтiндiде 49 г H2SO4 бар болса, осы ерiтiндiнiң нормалдығ ы қ андай? 10
100 г ерітіндіде 5 г Ca(OH)2Бар. Гидроксид кальцийдің массалық ү лесін w, % табың дар .5%
100 мл 0, 25 н K2Cr2O4 ерітіндісінің кө мегімен кү кірт қ ышқ ылы қ атысында қ анша грамм FeSO4 тотық тыра алады? 28.4
100 мл ерiтiндiде 3, 4 г AgNO3 болса, осы ерiтiндiнiң нормалдығ ы қ андай?
M(AgNO3) =170 г/моль 0, 2
100 мл ерiтiндiде 3, 4 г AgNO3 ерiтiлген. Ерiтiндiнiң нормалдығ ы қ андай?
M(AgNO3 )=170 г/моль). 0, 2
100 г Н2О да 10 г глицеринді С3Н8О3 ерiткенде глицерин ерiтiндiсiнiң қ ату температурасы қ анша градусқ а тө мендейдi? (МС3Н8O3=92 г/моль). КН2О=1, 860С. 2.02
15 минут 5 А. токты кү мiс нитраты ерiтiндiсiнен ө ткiзгенде 5, 04 г кү мiс бө лiндi. Ток шығ ымы қ андай? 85% 100
160 г суда 40 г тұ з ерiтiлген. Ерiтiндiдегi заттың массалық ү лесi қ андай (w, %)? 20
180С температурада Mg(OH)2 –магний гидроксидiнiң суда ерiгiштiгi 1, 7*10-4 моль/л. Осы температурадағ ы Mg(OH)2-ерiгiштiк кө бейтiндiсiн анық та (молл/л). 1.96*10^-11
2NO+O2®2NO2+Q-реакция тепе-тең дiгi солғ а қ арай қ ай жағ дайда ығ ысады?
Темп. кө терсе
2N2 О5 = 2N2О4 + О2 реакциясында бастапќы заттыњ концентрациясын 2 есеге кемiткенде, оныњ жылдамдыѓы ќалай ө згередi? NO
2NO + O2 = 2NO2 реакциясыныњ стандартты Гиббс энергиясыныњ ө згерiсiн 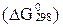 жә не реакцияныњ еркiн жү ру баѓытын аныќтањыз, егер заттардыњ 298 К температурадаѓы еркiн тү зiлу энергиялары тө мендегiдей болса:
жә не реакцияныњ еркiн жү ру баѓытын аныќтањыз, егер заттардыњ 298 К температурадаѓы еркiн тү зiлу энергиялары тө мендегiдей болса: 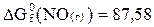 Дж/моль;
Дж/моль; 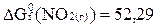 Дж/моль.NO
Дж/моль.NO
2А+В®А2В –реакция жылдамдығ ы қ алай ө згередi, егер А–заты концентрациясын 2 есе арттырып, ал B заты концентрациясын 2 есе азайтса? 2 есе ө седі
2NO(г)+O2(г)Û 2NO2(г) жү йесiндегi қ ысымды 4 есе ө сiрсе реакция жылдамдығ ы қ анша есе ө седi? 64
2SO2(г)+O2(г)Û 2SO3(г) жү йесiнiң қ ысысымын 2 есе азайтқ анда реакция жылдамдығ ы қ алай ө згередi? 8 есе кемиді
2РН3(г)+4О2(г)=р2О5(г)+3Н2О(с) реакция тең деуiн пайдаланып фосфиннiң (DН0298 РН3, кДж/моль) тү зiлуiнiң стандартты. жылуын табың ыз егер DНх.р.=-2360 кДж;
DН0298 Р2О5(г)=-1492 кДж/моль;
DН0298 Н2О(с)=-285, 8 кДж/моль болса. +5, 3
2CO(г) +O2 (г) Û 2CO(г)+Q жү йесiндегi тепе-тең дiктi солғ а, яғ ни бастапқ ы заттар жағ ына ығ ыстыру ү шiн:. 0, 33
2А2(г)+В2(г)=2А2В(г)-реакциядағ ы А-заты концентрациясын 4 есе тө мендету нә тижесiнде тура жә не керi реакция жылдамдығ ы ө згермеуi ү шiн B2 заты концентрациясын неше есе арттыру қ ажет? 16 ece
2SO2 + O2 «2SO3 системасында заттардыњ тепе-тењдiк кү йдегi концентрациялар: [SO2] = 0, 04 моль/л, [O2] = 0, 06 моль/л, [SO3] = 0, 02 моль/л. Тепе-тењдік констан-тасын есептењіз.NO
200 г Н2О да 40 г қ антты С12Н22О11 ерiткенде қ ант ерiтiндiсiнiң қ айнау температурасы қ анша градусқ а ө седi? (МС12H22O11=342 г/моль). ЕН2О=0, 520. 0.3
2 моль су мө лшерiн 2А ток кү шiмен ыдыратуғ а қ анша уақ ыт (сағ -мө лшерiмен) қ ажет? 53.6
2 моль хлордың (Cl2) қ алыпты жағ дайдағ ы кө лемi қ андай? 44, 8
2 моль темiр сульфидiнiң (FeS) массасын кө рсетiң iз. 176
2, 5 А токты қ алайы хлоридiнен SnCl2 30 мин ө ткiзгенде 2, 77 г қ алайы бө лiндi. Қ алайының эквивалентiн тап. 29, 7
200 г суда 5, 4 г зат ерiтiлген жә не ерiтiндiнiњ ќайнау температурасы 100, 0780С. Ерiген заттыњ молекулалыќ массасын есептењiз. Судыњ эбуллиоскопиялыќ константасы 0, 520 160;
298 К-де PbO2-нi цинкпен PbO(к)+2Zn(к)®Pb(к)+2ZnO(к) реакциясы бойынша тотық сыздандыруғ а бола ма? -99, 2
250 г суғ а 54 г глюкоза (C6H12O6) ерiтiлген. Осы ерiтiндi қ андай температурада (0С) кристалданады? -2.23
250 мл сулы ерiтiндiде 10, 5 г натрий фторидi ерiтiлген. (Мr(NaF)=42). Ерiтiндiнiң нормальдық концентрациясын анық таң ыз. 1
250С температурада 0, 5М глюкоза (С6Н12О6) ерiтiндiсiнiң осмос қ ысымы неге тең? 2.41
250 мл ерiтiндiдегi 10, 5 г натрий фторидiнiң нормалдық концентрациясы неге тең? MNaF=42 г/моль. 1
20 %-тiк ерiтiндi дайындау ү шiн 400 г суда NaNO3-тiң қ андай мө лшерiн ерiту керек?
Г
3H2(г)+N2(г)®2NH3(г) реакциясының жылдамдығ ы сутегi концентрациясын 2 есе ө сiргенде қ анша есе ө седi? 8
3H2(г)+N2(г) Û 2NH3(г) жү йесiндегi тепе-тең дiктi оң ғ а, яғ ни аммиак тү зiлу жағ ына ығ ыстыру ү шiн: 2, 68
34 г аммиак (NH3) қ алыпты жағ дайда қ андай кө лем (л) алады? 44, 8
30 г бейэлектролит (электролит емес) 500 г суда ерiтiлген. КН2О=1, 860С. Ерiтiндi –1, 860С-та қ атады. Ерiтiлген заттың молекулалық массасын анық таң ыз (г/моль). 60
4 энергетикалық дең гейде қ анша дең гейше бар? 4
400 мл 0, 1 н кү кірт қ ышқ ылының ерітіндісін дайындау ү шін 2 М H2SO4 –тен қ анша мл қ ажет? 3.56
400 г 50 % H2SO4 ерiтiндiсiнен (массасы бойынша) буландырып 100 г суды бө лiп алдық. Қ алғ ан ерiтiндiдегi H2SO4 массалық ү лесi (%) неге тең? 66.7
4NН3(г)+5NO2(г)=4NO(г)+6H2O(Бу) жү йесiнiң қ ысымын 2 есе ө сiрсе реакция жылдамдығ ы қ анша есе ө седi? 512
44, 5 г AlCl3 –гі хлор атомының саны неге тең? 23.5
4HCl(г)+O2(г)®2H2O(г)+2Cl2(г) реакциясының жылдамдығ ы HCl концентрациясын 2 есе ө сiргенде қ анша есе ө седi? 16
500 мл 0, 25Н Na2CO3 ерiтiндiсiнде қ анша Na2CO3 (г) ерiтiлген? 6.63
5, 6 г кү кiрт темiрмен қ осылғ анда 17, 59 кДж жылу бө лiнген. Мына реакция бойынша: Fe+S=FeS темiр сульфидiнiң тү зiлу жылуын есептең iз, 56 kDj /mol
5, 6 л азот оксидiнiң (NO) қ.ж. мө лшерiн (n) табың ыз? 0, 25
56 г азоттың (N2) қ.ж. моль санын кө рсетiң iз. 2
5 л газдың қ алыпты жағ дайдағ ы массасы 7, 15 г. Осы газдың азотпен салыстырғ андағ ы тығ ыздығ ын табың ыз. 1, 14
80 г электролит емес зат 2 кг суда (Н2О) ерiтiлген. Бұ л заттың молярлық массасы 80 г/моль. KH2O=1, 860. Ерiтiндiнiң қ ату температурасын анық таң ыз (Dt). -3, 720
“f”-электрон бұ лты дең гейiндегi орбиталь санын кө рсет: 14
 Sb сурьманың ең кіші жә не ең ү лкен тотығ у дә режесiн кө рсетiң iз. (-3) - (+5)
Sb сурьманың ең кіші жә не ең ү лкен тотығ у дә режесiн кө рсетiң iз. (-3) - (+5)
235U реттік нө мірі 92, нейтрон саны неге тең? 0
|
|