
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
⚡️ Для новых пользователей первый месяц бесплатно. А далее 290 руб/мес, это в 3 раза дешевле аналогов. За эту цену доступен весь функционал: напоминание о визитах, чаевые, предоплаты, общение с клиентами, переносы записей и так далее.
✅ Уйма гибких настроек, которые помогут вам зарабатывать больше и забыть про чувство «что-то мне нужно было сделать».
Сомневаетесь? нажмите на текст, запустите чат-бота и убедитесь во всем сами!
Металлические защитные покрытия
|
|
По характеру поведения при электрохимической коррозии их подразделяют на катодные и анодные.
Металлы катодных или коррозионно – стойких покрытий в данной среде имеют более положительные значения электродных потенциалов по сравнению с потенциалом металла, на который они наносились. Это, например  на железе
на железе 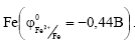
Они защищают изделия лишь механически. изолируя их поверхность от окружающей среды. Основным требованием, предъявляемым к этому виду покрытий является их герметичность (сплошность и беспористость). При повреждении покрытия или наличия пор, электролитная коррозионная среда, попадая в них, вызывает разрушение основного (защищаемого) металла вследствие возникновения микрокоррозионных гальванических пар, в которых металл покрытия выступает в качестве катода и на котором выделяется водород или поглощается кислород.
Металлы анодных или протекторных покрытий имеют более отрицательные потенциалы, чем потенциал основного (защищаемого) металла. Поэтому цинк 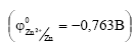 и алюминий
и алюминий 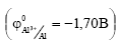 на железе
на железе 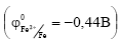 являются анодными покрытиями.
являются анодными покрытиями.
Анодные покрытия защищают изделия не только механически, но и электрохимически. При их повреждении или наличии в них пор, в коррозионной среде также образуются микрокоррозионные гальванические пары, в которых защищаемый металл выступает в роли катода и не корродирует. Разрушению в этои случае подвергается само покрытие. Поэтому, требования герметичности (сплошности и беспористости) для анодных покрытий не существенно.
Потенциалы металлов зависят от вида и состава растворов, поэтому при их изменении может меняться и характер покрытия. Так, олово на железе в растворах неорганических кислот и солей ведет себя как катодное покрытие, а в растворах ряда органических кислот как анодное покрытие. Для повышения защитных свойств катодных покрытий их часто пропитывают органическими лаками, которые заполняют имеющиеся в них поры. Методов нанесения металлических покрытий много. Об ионной имплантации говорилось в легировании, так же можно наносить электрохимическим методом (электролизом). Рассмотрим еще некоторые.
|
|
