
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Векторы на основе фага l
|
|
Основным недостатком плазмидных векторов для клонирования является их малая емкость в отношении клонируемых фрагментов ДНК. Размер вставок клонируемой ДНК в плазмидных векторах, которые способны стабильно в них существовать, как правило, не превышает нескольких тысяч пар оснований. Большие вставки ДНК в векторных плазмидах нестабильны, и их размеры постепенно уменьшаются по мере увеличения числа раундов репликации таких рекомбинантных плазмид in vivo. Преимущественное делетирование чужеродной ДНК в плазмидах большого размера связано с тем, что в бактериальных клетках селективное преимущество получают те плазмиды, время репликации которых минимально. Поэтому нуклеотидные последовательности ДНК, не участвующие в репликации векторных плазмид, постепенно элиминируются посредством делеций при длительном культивировании рекомбинантных бактерий.
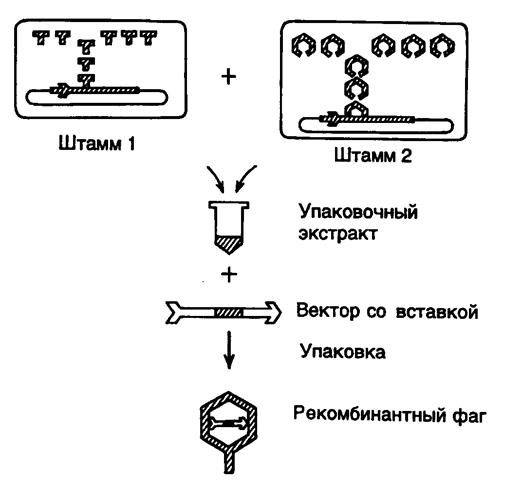
Рис. II.6. Упаковка рекомбинантной фаговой ДНК в фаговые частицы in vitro
Емкость клонирующих векторов была значительно повышена с появлением векторов, сконструированных на основе хромосомы бактериофага l. Получившие широкое распространение векторы серий Charon, lgt11 и EMBL обладают, по крайней мере, двумя существенными преимуществами перед плазмидными векторами. Во-первых, векторы на основе ДНК фага l обладают значительно большей емкостью, в них можно клонировать фрагменты ДНК длиной от 5 до 25 т.п.о. Во-вторых, фаговые частицы, содержащие упакованную ДНК, способны проходить литический цикл развития внутри бактериальных клеток и, следовательно, образовывать стерильные пятна (бляшки) на газоне бактерий. Такие бляшки содержат в концентрированном виде как сами фаговые частицы с упакованными в них рекомбинантными молекулами ДНК, так и все продукты метаболизма зараженных бактериальных клеток, включая белки и ферменты, которые появляются в результате экспрессии клонированных бактериальных генов. Каждая бляшка возникает вследствие развития индивидуальной фаговой частицы, содержащей рекомбинантную ДНК только одного типа, а, следовательно, все фаговые частицы одной бляшки (~1010) представляют собой, как правило, клон идентичных фаговых частиц (они могут различаться в редких случаях за счет мутационных изменений их генома, произошедших в процессе жизненного цикла фага, либо в том случае, если одна бактериальная клетка заражается несколькими фаговыми частицами одновременно). Все это позволяет легко обнаруживать в фаговых бляшках искомые ферментативные активности или последовательности нуклеотидов и идентифицировать клонированные последовательности ДНК. В основе конструирования фаговых векторов лежит несколько простых принципов (рис.II.6). В середине молекулы l-ДНК длиной ~45 т.п.о. расположен участок хромосомы (~15 т.п.о.), который не является необходимым для литического развития бактериофага. Поэтому, в принципе, его можно заменить на любой фрагмент ДНК аналогичного размера и осуществить клонирование фрагмента путем размножения рекомбинантного бактериофага. Поскольку механизм упаковки хромосомной ДНК в фаговые частицы основан на включении ДНК строго определенного размера, рекомбинантные ДНК, содержащие фрагменты клонируемой ДНК, которые не соответствуют оптимальному размеру, не упаковываются и не клонируются. Это позволяет легко освобождаться от фаговых частиц, не содержащих вставки клонируемой ДНК, и оптимизировать процесс клонирования путем снижения в упаковочных экстрактах доли нежизнеспособных фаговых частиц. Процесс упаковки фаговой ДНК в зрелые фаговые частицы осуществляется в смеси бесклеточных экстрактов двух штаммов E. coli, лизогенных по дефектным бактериофагам l. В одном штамме амбер-мутацией инактивирован один из белков фагового капсида (продукт гена E), а в другом – ген A, продукт которого необходим для включения фаговой ДНК в головку бактериофага. Имеются и другие пары лизогенных штаммов E. coli, позволяющие производить упаковку ДНК в фаговые частицы с использованием тех же общих принципов. Объединение бесклеточных лизатов обоих штаммов E. coli приводит к взаимной комплементации недостающих функций с помощью соответствующих белков дикого типа. Таким образом, в объединенных экстрактах имеются все компоненты, необходимые для сборки зрелых инфекционных фаговых частиц, в них происходит упаковка рекомбинантной ДНК с эффективностью образования 104–105 фаговых частиц на 1 мкг упаковываемой ДНК. Помимо вышеупомянутых мутаций ДНК l-лизогенов содержат температурно-чувствительную мутацию в репрессоре cI, который инактивируется после переноса лизогенных клеток E. coli на непермиссивную температуру (42o), что сопровождается индукцией профага l и накоплением внутри бактериальных клеток белковых продуктов, необходимых для упаковки ДНК. ДНК профагов также содержит делецию b2, элиминирующую сайт att, необходимый для интеграции фаговой ДНК в бактериальную хромосому. Это предотвращает выход ДНК профага из бактериальной хромосомы, а следовательно, и ее упаковку in vitro. Кроме того, в хромосоме профага имеется мутация, инактивирующая ген S, кодирующий лизоцим, что препятствует преждевременному лизису бактериальных клеток после индукции профага и позволяет сконцентрировать бактериальные клетки перед получением упаковочных экстрактов. И, наконец, бактериальные лизогенные клетки содержат мутацию recA, которая предотвращает гомологичную рекомбинацию между ДНК профага и рекомбинантными ДНК, упаковываемыми в фаговые частицы.
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение

Рис. II.7. Генетическая карта хромосомы бактериофага l-EMBL3
а – расположение генов на хромосоме; б – шкала длины хромосомной ДНК в процентах от длины l-ДНК и т.п.о.; в – участок генома, замещаемый на клонируемый фрагмент ДНК соответствующего размера. S, B и R – сайты рестрикции SalG I, BamH I и EcoR I соответственно
В качестве примера рассмотрим генетическую карту векторной ДНК бактериофага l-EMBL и кратко обсудим возможности этого вектора (рис. II.7). Векторы серии EMBL являются производными ДНК бактериофага l1059. Их хромосомная ДНК длиной в 42364 п.о. содержит центральный сегмент ДНК длиной ~15 т.п.о., который замещается на клонируемый фрагмент ДНК соответствующего размера. При этом в фаговые частицы может быть упакована рекомбинантная ДНК общей длиной в 9–23 т.п.о. Замещаемый фрагмент фаговой хромосомы фланкирован с обоих концов последовательностями полилинкера, содержащего рестриктазные сайты EcoR I, BamH I и SalG I, по которым встраивают клонируемые фрагменты ДНК. При этом во время подготовки вектора к работе нет необходимости отделять " плечи" вектора от центрального фрагмента. Сначала центральный фрагмент ДНК выщепляется рестриктазой по одному из сайтов полилинкера, а затем смесь образовавшихся фрагментов обрабатывается другой рестриктазой, сайт для которой находится в полилинкере. Образующиеся олигонуклеотидные фрагменты полилинкера удаляются при переосаждении ДНК спиртом, а " липкие" концы " плеч" вектора и центральной последовательности получаются некомплементарными друг другу и не могут объединяться в процессе лигирования с образованием исходной формы ДНК вектора.
|
|
