
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
III. Стадия длительного поддержания жизни. Согласно данным Национального регистра по сердечно-легочной реанимации США (National Registry of Cardiopulmonary Resuscitation — NRCPR)
|
|
Согласно данным Национального регистра по сердечно-легочной реанимации США (National Registry of Cardiopulmonary Resuscitation — NRCPR), среди 19 819 взрослых и 524 детей после восстановления спонтанного кровообращения уровень внутрибольничной летальности составил 67 и 55 % соответственно [15]. По данным эпидемиологического исследования, среди 24 132 реанимированных пациентов в Великобритании уровень летальности в постреанимационном периоде составил 71 % [16]. При этом необходимо отметить, что среди выживших только 15–20 % имеют быстрое восстановление адекватного уровня сознания, остальные 80 % пациентов проходят через постреанимационную болезнь. Причины смерти в постреанимационном периоде: 1/3 — кардиальные (наиболее высок риск в первые 24 часа постреанимационного периода), 1/3 — дисфункция различных экстрацеребральных органов и 1/3 — неврологические (причины смерти в отдаленном периоде постреанимационной болезни — ПРБ) [3].
Согласно В.А. Неговскому, «для постреанимационной болезни (ПРБ) характерна своя особая этиология — неразделимое сочетание глобальной ишемии с реоксигенацией и реперфузией. Поскольку реоксигенация и реперфузия после перенесенной остановки кровообращения не только ликвидируют последствия первичного патологического воздействия, но и вызывают каскад новых патологических изменений. Важно, что причиной этих изменений является не сама по себе глобальная ишемия, а ее сочетание с реоксигенацией и реперфузией» [17].
ПРБ представляет собой комбинацию патофизиологических процессов, включающих 4 ключевых компонента (табл. 1):
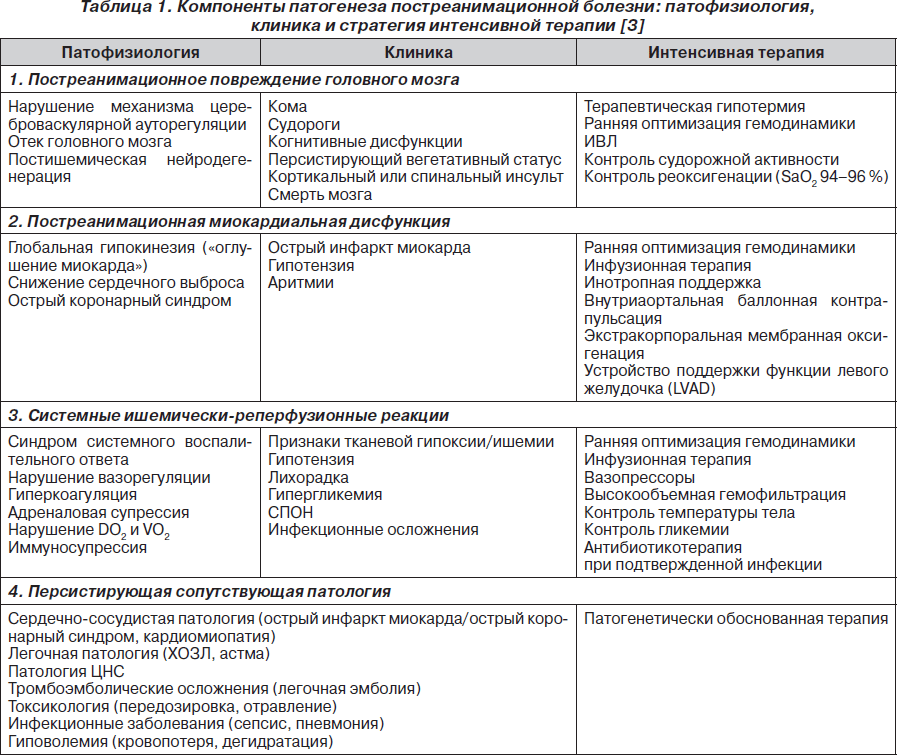
1) постреанимационное повреждение головного мозга;
2) постреанимационную миокардиальную дисфункцию;
3) системные ишемически-реперфузионные реакции;
4) персистирующую сопутствующую патологию [3].
Распространенность постреанимационного повреждения головного мозга обусловлена сложностью морфологической структуры головного мозга, выполняемых им функций, а также малой толерантностью к ишемии и гипоксии. Ни одна клетка организма не зависит от уровня кислорода и глюкозы так, как нейрон. Максимальная продолжительность клинической смерти (т.е. аноксии) в условиях нормотермии, при которой возможно выживание нейронов, составляет не более 5 минут.
Нейрональное повреждение при ПРБ носит многофакторный характер и развивается в момент остановки кровообращения, в процессе СЛР, а также в периоде восстановления самостоятельного кровообращения:
— период ишемии — аноксии в момент отсутствия кровообращения во время клинической смерти (no-flow);
— период гипоперфузии — гипоксии при искусственном поддержании кровообращения в процессе СЛР (low-flow), поскольку максимально возможный уровень сердечного выброса (СВ) достигает только 25 % от исходного;
— период реперфузии, состоящий из последовательно развивающихся фаз: no-reflow, следующей затем фазы гиперемии и последующей глобальной и мультифокальной гипоперфузии [18].
В постреанимационном периоде выделяют следующие стадии нарушения перфузии головного мозга после восстановления самостоятельного кровообращения:
1. Начальное развитие мультифокального отсутствия реперфузии (феномен no-reflow).
2. Стадия транзиторной глобальной гиперемии — развивается на 5–40-й минуте с момента восстановления спонтанного кровообращения. Механизм ее развития связан с вазодилатацией сосудов головного мозга за счет повышения внутриклеточной концентрации Na+ и аденозина, а также снижения внутриклеточного рН и уровня Са2+. Длительность ишемии головного мозга в последующем определяет длительность стадии гиперемии, которая, в свою очередь, носит гетерогенный характер в различных регионах головного мозга, приводя к снижению перфузии и набуханию астроцитов.
3. Стадия пролонгированной глобальной и мультифокальной гипоперфузии — развивается от 2 до 12 часов постреанимационного периода. Скорость церебрального метаболизма глюкозы снижается до 50 % от исходного уровня, однако глобальное потребление кислорода мозгом возвращается к нормальному (или более высокому) уровню в сравнении с исходным до момента остановки кровообращения. Церебральное венозное РО2 может находиться на критически низком уровне (менее 20 мм рт.ст.), что отражает нарушение доставки и потребления кислорода. Причина этого заключается в развитии вазоспазма, отека, сладжирования эритроцитов и чрезмерной продукции эндотелинов.
4. Данная стадия может развиваться по нескольким направлениям:
4.1. Нормализация церебрального кровотока и потребления кислорода тканью мозга с последующим восстановлением сознания.
4.2. Сохранение персистирующей комы, когда как общий мозговой кровоток, так и потребление кислорода остается на низком уровне.
4.3. Повторное развитие гиперемии головного мозга, ассоциированное со снижением потребления кислорода и развитием гибели нейронов [19].
Постреанимационная дисфункция миокарда имеет различные клинические проявления. Так, в экспериментах на свиньях было показано снижение в первые 30 мин постреанимационного периода фракции изгнания с 55 до 20 %, а также повышение конечно-диастолического давления (КДД) левого желудочка с 8–10 до 20–22 мм рт.ст. Согласно результатам других исследований, у пациентов в 49 % случаев постреанимационная дисфункция миокарда манифестирует тахикардией, повышением КДД левого желудочка, а в первые 6 часов гипотензией (САД < 75 мм рт.ст.) и низким сердечным выбросом (СИ < 2, 2 л/мин/м2) [3].
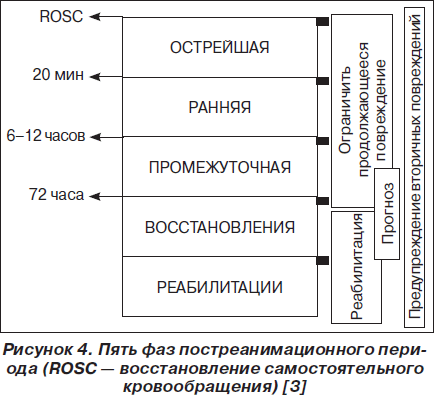
Согласно последнему международному консенсу, выделяют пять фаз постреанимационного периода, каждая из которых определяет тактику интенсивной терапии (рис. 4) [3].
Прогностическая оценка состояния в постреанимационном периоде
Коматозное состояние в течение 48 и более часов выступает предиктором плохого неврологического исхода. Если через 72 часа после остановки кровообращения неврологический дефицит составляет Ј 5 баллов по шкале ком Глазго в отсутствие двигательной реакции в ответ на болевое раздражение или зрачкового рефлекса, это является предиктором развития персистирующего вегетативного состояния у всех больных [3].
|
|