
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
⚡️ Для новых пользователей первый месяц бесплатно. А далее 290 руб/мес, это в 3 раза дешевле аналогов. За эту цену доступен весь функционал: напоминание о визитах, чаевые, предоплаты, общение с клиентами, переносы записей и так далее.
✅ Уйма гибких настроек, которые помогут вам зарабатывать больше и забыть про чувство «что-то мне нужно было сделать».
Сомневаетесь? нажмите на текст, запустите чат-бота и убедитесь во всем сами!
Ненасыщенные двухосновные kapбоhobыe кислоты
|
|
Наиболее простые ненасыщенные двухосновные кислоты – фумаровая и малеиновая – имеют одну и ту же структурную формулу, но разные пространственные конфигурации. Фумаровая кислота – транс-, а малеиновая – цис -изомер:
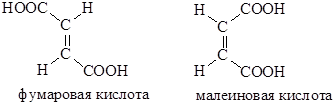
Эти кислоты отличаются по физическим свойствам. Фумаровая кислота имеет т. пл. 287-288°С, плохо растворима в воде, а малеиновая плавится при 130°С, очень хорошо растворима в воде.
Малеиновая кислота значительно сильнее фумаровой, их константы диссоциации соответственно равны 117∙ 10-2 и 9.3∙ 10-2.
Обе кислоты получаются при нагреве яблочной кислоты, образование того или иного изомера зависит от режима нагревания:
НООС-СН2-СНОН-СООН ® НООС-СН=СН-СООН + Н2О
В промышленности малеиновую кислоту получают каталитическим окислением бензола или нафталина кислородом воздуха.
Эти кислоты идентично ведут себя в реакциях присоединения по двойной связи водорода, галогенов, галогеноводородов.
Обе кислоты способны образовывать соли, сложные эфиры, амиды и другие производные кислот. В отличие от фумаровой, малеиновая кислота легко образует циклический ангидрид:
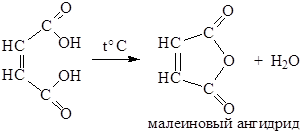
Малеиновый ангидрид служит реактивом для обнаружения 1, 3-диеновых соединений: он легко вступает в реакцию диенового синтеза. В последние годы он приобрел широкое применение в производстве полиэфирных смол, а также для получения сополимеров (со стиролом, акриловым и метакриловым эфирами).
Малеиновая кислота под действием брома, йода, азотистой кислоты легко переходит в более устойчивую фумаровую кислоту. Обратный переход осуществляется под действием ультрафиолетовых лучей.
Лекция 23. МОНОКАРБОНОВЫЕ КИСЛОТЫ АРОМАТИЧЕСКОГО РЯДА
Монокарбоновые кислоты, изомерия, номенклатура. Способы получения: из ароматических углеводородов, спиртов, альдегидов, кетонов, из тригалогенпроизводных и нитрилов, реакцией Канниццаро, по реакции ацилирования, реакцией Гриньяра. Физические свойства. Химические свойства. Уравнение Гаммета. Функциональные производные ароматических кислот. Отдельные представители.
Ароматическими карбоновыми кислотами называются производные бензола, содержащие карбоксильные группы, непосредственно связанные с ароматическим ядром. Кислоты, содержащие карбоксильные группы в боковой цепи, рассматриваются как жирноароматические. По количеству карбоксильных групп ароматические кислоты делятся на моно-, дикарбоновые и т.д. Название кислоты производится от ароматического углеводорода (бензойная кислота, п -толуиловая кислота).
|
|
