
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Железо-серный белок
|
|
¯
НАДН(Н+) ® ФМН ® железо-серный белок ® КоQ (убихинон) ® цитохром b ® железо-серный белок ® цитохром с1 ® цитохром с ® цитохром а ® цитохром а3 ® О2
Порядок расположения компонентов в дыхательной цепи зависит от величины их окислительно-восстановительного потенциала. Для каждого последующего компонента характерна более высокая окислительная способность.
В состав III и IV комплексов входят сложные белки из группы хромопротеинов - цитохромы. Их простетическая группа близка к гему и содержит железо. Однако в противоположность гемоглобину, имеющему двухвалентное железо, цитохромы содержат железо, которое может переходить из двухвалентного (восстановленного) в трехвалентное (окисленное) состояние и обратно.
Конечным акцептором электронов является О2. Восстановление кислорода до воды происходит по схеме:
2Н+ + 2 е + 1/2 О2 ® Н2О или 4 Н+ + 4 е + О2 ® 2 Н2О
Ионы Н+ для образования воды берутся из матрикса митохондрий.
Согласно хемиосмотической теории П.Митчелла сопряжение переноса электронов и синтеза АТФ обеспечивается градиентом электрохимического потенциала ионов водорода (рис. 3) Dm Н+, который состоит из двух компонентов - разности электрических потенциалов (Dj) и разности концентраций ионов водорода - D рН. Перенос электронов по дыхательной цепи приводит к выбросу протонов из матрикса на цитоплазматическую сторону внутренней митохондриальной мембраны где, таким образом возрастает концентрация ионов водорода. В результате происходит генерирование DрН (защелачивание в матриксе и закисление с внешней стороны внутренней митохондриальной мембраны) и Dj (разности электрических потенциалов, причем та часть внутренней мембраны, которая обращена к матриксу, приобретает отрицательный заряд, а та, которая обращена к межмембранному пространству – положительный). Протонный градиент используется для синтеза АТФ, который осуществляется при помощи ферментного комплекса АТФ-синтазы в ходе обратного поступления протонов в митохондриальный матрикс.
Выброс протонов происходит в 3-х пунктах потока электронов по дыхательной цепи от НАДН(Н+) к О2 – в I, III и IV комплексах; 1-й пункт - это НАДН(Н+) – КоQ - оксидоредуктазный комплекс; 2-й пункт - КоQ - цитохром с - оксидоредуктазный комплекс; 3-й - цитохромоксидазный комплекс. Протонный градиент, генерируемый в каждом из этих пунктов при переносе одной пары электронов от НАДН(Н+) к О2, используется для синтеза одной молекулы АТФ (АДФ + Н3РО4 ® АТФ). Окисление одной молекулы НАДН(Н+) дает 3 АТФ, тогда как окисление ФАДН2 - 2 АТФ (энергии, выделяющейся в процессе функционирования сукцинат-КоQ-оксидоредуктазного комплекса недостаточно для синтеза АТФ, т.е. трансформации энергии здесь не происходит).
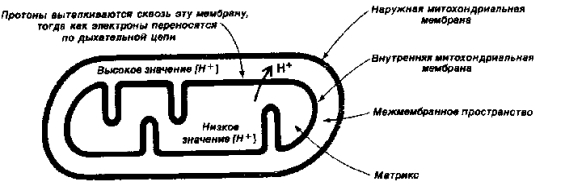 |
Рис.3. Схема переноса протонов водорода в митохондриях.
Таким образом, окислительное фосфорилирование представляет собой процесс переноса электронов от восстановленных коферментов НАДН(Н+) и ФАДН2 к молекулярному кислороду, сопряженный с синтезом АТФ. Окислительное фосфорилирование часто характеризуют отношением Р: О (число молей неорганического фосфата, использованного для синтеза АТФ в расчете на один атом потребляемого кислорода).
Скорость окислительного фосфорилирования зависит, в первую очередь, от содержания АДФ: чем быстрее расходуется АТФ для нужд организма, тем больше накапливается АДФ и тем больше потребность в энергии, а следовательно и в синтезе АТФ. Накопление АТФ, естественно, сопровождается снижением содержания АДФ, скорость образования АТФ при этом также уменьшится. При ограниченной потребности в АТФ падает и скорость окислительного распада субстратов. Регуляцию скорости окислительного фосфорилирования содержанием АТФ называют дыхательным контролем.
· СУБСТРАТНОЕ ФОСФОРИЛИРОВАНИЕ
Субстратное фосфорилирование является альтернативным механизмом образования АТФ, так как оно не требует образования DmН+. В ходе окисления субстратов образуются макроэргические соединения, разрыв макроэргической связи в которых сопряжен с фосфорилированием АДФ (т.е. с синтезом АТФ).
Пример субстратного фосфорилирования:
О О ОН
// // |
С – Н +НАД+ С - О ~ Р = О СООН
| + H3PO4 | | +АДФ |
Н – С – ОН ОН ¾ ¾ ¾ ® Н – С – ОН ОН ОН ¾ ¾ ¾ ¾ ® Н – С – ОН ОН
| | -НАДН(Н+) | | -АТФ | |
СН2О - Р = О СН2 – О - Р = О СН2 – О – Р = О
| | |
ОН ОН ОН
ГА – 3 – Ф 1, 3 – ДФГ 3 – ФОСФОГЛИЦЕРАТ (3-ФГ)
В процессе гликолиза высвобождаемая при окислении глицеральдегид-3-фосфата (ГА-3-Ф) энергия, аккумулируется в макроэргической связи 1, 3-дифосфоглицерата (1, 3-ДФГ). Расщепление этой связи в дальнейшем сопряжено с фосфорилированием АДФ, в результате чего осуществляется образование АТФ.
· МАКРОЭРГИЧЕСКИЕ СОЕДИНЕНИЯ
Энергия, прежде чем быть использованной для нужд организма, аккумулируется в макроэргических соединениях. Гидролиз таких соединений сопровождается выделением большого количества энергии (свыше 7 ккалмоль). К ним относятся нуклеозидтрифосфаты, ацилфосфаты, енолфосфаты, тиоэфиры, фосфагены.
Нуклеозидтрифосфаты (АТФ, ГТФ, ЦТФ, УТФ) содержат по 2 макроэргические связи.
АТФ (рис. 4) является главным, непосредственно используемым донором свободной энергии в биологических системах.
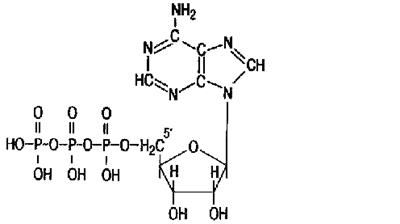
Рис.4. Строение АТФ.
Гидролиз АТФ может происходить двумя путями:
1) АТФ + Н2О ® АДФ + Н3РО4;
2) АТФ + Н2О ® АМФ + Н4Р2О7
В обоих случаях при стандартных условиях высвобождается 7, 3 ккалмоль энергии (при условиях, существующих в клетке в норме, около 12 ккалмоль).
Высвобождаемая при гидролизе АТФ энергия, используется для процессов биосинтеза сложных веществ из более простых, при мышечном сокращении, для активного транспорта молекул и ионов (рис. 5).
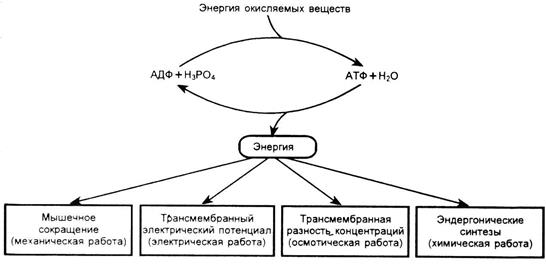
Рис.5. Основные пути использования энергии АТФ.
Примером ацилфосфата является 1, 3-дифосфоглицерат, являющийся промежуточным продуктом гликолиза (при его гидролизе выделяется 11, 8 ккалмоль энергии).
О ОН
// |
С - О ~ Р = О
| |
Н – С – ОН ОН ОН
| |
СН2 – О - Р = О
|
ОН
1, 3-дифосфоглицерат
К енолфосфатам относится фосфоенолпируват, также участвующий в процессе гликолиза (гидролиз его макроэргической связи приводит к выделению 14, 8 ккалмоль энергии).
СООН ОН
½ ½
С – О ~ Р = О
ê ê ê
СН2 ОН
фосфоенолпируват
Активная уксусная кислота (ацетил-КоА) и активная янтарная кислота (сукцинил-КоА) являются тиоэфирами.
О О
// //
СН3 – С ~ S – КоА НООС – СН2 – СН2 – С ~ S – КоА
ацетил-КоА сукцинил-КоА
Креатинфосфат (при его гидролизе выделяется 10, 3 ккалмоль энергии) относится к фосфагенам.
ОН
ê
Н – N ~ Р = О
ê ê
С=NH ОН
ê
N – CН3
ê
СН2
ê
СООН
креатинфосфат
Креатинфосфат используется в мышечной ткани для регенерации АТФ (креатинфосфат + АДФ ® креатин + АТФ).
· СВОБОДНОЕ ОКИСЛЕНИЕ
Свободное окисление не сопряжено с синтезом АТФ. Выделяющаяся при этом энергия рассеивается в виде тепла. Классическим примером разобщения окисления с образованием АТФ является действие 2, 4-динитрофенола (ДНФ). Это соединение использовалось для снижения массы тела. Оно резко увеличивает протонную проницаемость клеточных мембран, разобщает окислительное фосфорилирование и приводит к развитию тяжелых дистрофических процессов в результате недостаточного синтеза клеткой АТФ.
Частичное разобщение окисления с фосфорилированием наблюдается при многих заболеваниях, поскольку митохондрии являются наиболее чувствительными клеточными органеллами к действию неблагоприятных факторов внешней среды. Митохондриальная патология развивается при гипертиреозе. При избыточном выделении щитовидной железой гормонов происходит набухание митохондрий и их распад, что приводит к снижению образования АТФ. При этом усиливаются окислительные процессы, отмечается более высокая чем в норме температура тела, учащается сердцебиение.
Разобщение окислительного фосфорилирования может быть биологически полезным. Оно представляет собой способ генерирования тепла для поддержания температуры тела у зимнеспящих животных, у некоторых новорожденных животных и у млекопитающих, адаптированных к холоду. Для этого процесса термогенеза специализирована бурая жировая ткань, очень богатая митохондриями. В качестве разобщителей в ней выступают жирные кислоты, высвобождение которых в свою очередь регулируется норадреналином. Таким образом, степень разобщения окислительного фосфорилирования в бурой жировой ткани находится под гормональным контролем. Митохондрии в этой ткани могут выполнять функцию генераторов АТФ или миниатюрных обогревательных печей.
В микросомах печени с участием цитохрома Р-450 происходит метаболизм многих лекарственных веществ путем их гидроксилирования. Восстановителями цитохромов являются НАДН(Н+) и НАДФН(Н+):
Лек - Н + О2 + цитохром Р-450 (Fe2+) + 2Н+ ® Лек - ОН + Н2О + цитохром Р-450
(Fe3+)
Митохондриальные цитохром Р-450 - содержащие монооксигеназные системы находятся в коре надпочечников, в семенниках, яичниках, плаценте. Они участвуют в синтезе стероидных гормонов из холестерина. В печени происходит гидроксилирование холестерина по положению 26 в ходе биосинтеза желчных кислот.
· КОНТРОЛЬНЫЕ ВОПРОСЫ ПО ТЕМЕ:
«ОБМЕН ВЕЩЕСТВ И ЭНЕРГИИ. БИОЛОГИЧЕСКОЕ ОКИСЛЕНИЕ»
1. Какие особенности присущи живым организмам по сравнению с неживой приро-дой? В чем состоит сущность обмена веществ?
2. Назовите принципиальные различия между анаболическими и катаболическими процессами.
3. Какова последовательность обменных процессов в организме животных?
4. Охарактеризуйте стадии обмена веществ в зависимости от количества выделяемой
энергии.
5. Что такое биологическое окисление? Укажите основные отличия процессов биоло-
гического окисления глюкозы и ее горения.
6. Какие пути синтеза АТФ существуют в организме животных?
7. Что понимают под окислительным фосфорилированием? Каковы механизмы регу-
ляции этого процесса?
8. Назовите компоненты дыхательной цепи, сопряженной с трансформацией энергии.
От чего зависит порядок их расположения?
9. В чем состоит сущность хемиосмотической теории П.Митчелла?
10. Объясните почему при окислении НАДН(Н+) в дыхательной цепи образуется 3 молекулы АТФ, а при окислении ФАДН2 – 2?
11. В чем состоит разница между окислительным и субстратным фосфорилированием?
12. Какие соединения называют макроэргическими? Приведите примеры макроэрги-
ческих соединений и укажите в чем заключается их роль для организма животных.
13. Какое значение для организма животных имеет разобщение окисления с синтезом
АТФ?
14. В чем заключается роль микросомального окисления?
|
|