
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
⚡️ Для новых пользователей первый месяц бесплатно. А далее 290 руб/мес, это в 3 раза дешевле аналогов. За эту цену доступен весь функционал: напоминание о визитах, чаевые, предоплаты, общение с клиентами, переносы записей и так далее.
✅ Уйма гибких настроек, которые помогут вам зарабатывать больше и забыть про чувство «что-то мне нужно было сделать».
Сомневаетесь? нажмите на текст, запустите чат-бота и убедитесь во всем сами!
Схема 8. Циклы железа в организме
|
|
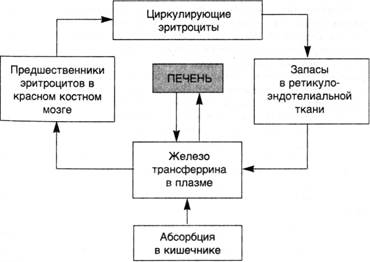
Гемоглобиногенные пигменты получили свое наименование вследствие того, что их образование связано с метаболизмом гемоглобина. При этом часть пигментов образуется в физиологических условиях. Это гемосидерин, ферритин и билирубин. Часть пигментов — гематоидин, гематины и порфирин, образуются только в условиях патологии. Некоторые из этих пигментов (ферритин, гемосидерин) синтезируются, помимо гемоглобина, из железа, всасывающегося в кишечнике (схема 8). Поэтому определение " гемоглобиногенные пигменты" является для них весьма условным.
Гемоглобин — хромопротеид, который в качестве простетической группы содержит железопорфириновый комплекс гем. Белковая часть молекулы гемоглобина состоит из двух пар полипептидных (а и Ь) цепей, содержащих по 140 аминокислот. Своим
огромным значением гемоглобин обязан содержащемуся в нем железу, с которым филогенетически связана функция дыхания. Обмен гемоглобина тесно связан с эритроцитами, в которых он содержится, с их состоянием, старением, разрушением. Физиологический гемолиз происходит в основном в костном мозге, реже — в селезенке и печени, в клетках макрогистиоцитарной системы этих органов образуются ферритин, гемосидерин и билирубин.
Ферритин — железопротеид, содержащий белок апоферритин и трехвалентный атом железа в составе фосфатного гидроксида. Ферритин неоднороден, известно до 20 изоферритинов. Это разнообразие обусловлено различием вариантов входящего в его состав апоферритина (Н-, L- и HL-субъединицы), различием способов происхождения пигмента (" анаболический" — из железа, всасывающегося в кишечнике, " катаболический" — из железа гемолизированных эритроцитов), разной локализацией (в сыворотке крови — HL-ферритин, в печени и селезенке — L-ферритин). Наконец, важное значение имеет кислород: ферритин синтезируется из двухвалентного железа в присутствии кислорода и содержит много SS-групп. При гипоксии образуется SH-ферритин, обладающий вазопаралитическим действием. Значение ферритина трудно переоценить. Он является главным участником метаболизма железа. Известно, что свободные атомы железа токсичны для организма. Именно в форме ферритина депонируется железо (до 30 %, хотя расходуется только 0, 1 %). Ферритин содержится практически во всех органах и тканях и является акцептором железа в клетках, которые в нем нуждаются (эритробласты). Он также осуществляет перенос железа в кишечнике и плаценте, т.е. является медиатором при соединении железа с трансферрином и в переносе его от матери к плоду.
Ферритин выявляют в тканях с помощью сульфата кадмия по методу Клочкова, а также иммуногистохимически с использованием специфических антисывороток. На практике чаще всего используется гистохимический метод — реакция образования берлинской лазури (железистосинеродистое железо) или реакции Перльса — реакция на выявление солей оксида железа (III) с помощью железосинеродистого калия и хлороводородной (соляной) кислоты.
Гемосидерин — это продукт полимеризации ферритина. По химической структуре он является коллоидным гидроксидом железа, соединенным с мукопротеидами клетки. В норме гемосидерин образуется в ретикулярных и эндотелиальных клетках селезенки, лимфатических узлов, печени и костного мозга. При окраске гематоксилином и эозином гемосидерин выявляется в виде зерен бурого цвета в цитоплазме этих клеток, а при реакции Перльса — в виде гранул зеленовато-синего цвета (берлинская лазурь). Гемосидерин — внутриклеточный пигмент. Синтез его происходит в клетках, которые называют сидеробластами, в специализированных органеллах — сидеросомах. Иногда в сидеробластах накапливается такое большое количество гемосидерина, что клетки разрушаются и гемосидерин оказывается свободно лежащим в строме органов. В этих случаях он обычно захватывается макрофагами, которые принято называть сидерофагами. В цитоплазме этих клеток сидеросомы не выявляются.
Билирубин — конечный продукт гемолиза. Билирубин образуется, когда от гемоглобина отщепляется гем, а затем от гема отщепляется железо и разворачивается тетрапиррольное кольцо. Этот процесс начинается в клетках ретикуломакрофагальной системы костного мозга, селезенки, лимфатических узлов и печени. Затем продукт, соединяясь с альбумином, с током крови поступает в печень. В печени синтез пигмента завершается — гепатоциты, обладая специфическими рецепторами, захватывают его и с помощью ферментов специфической глюкуронилтрансферазной системы осуществляют его конъюгацию. Конъюгаты билирубина поступают в желчные капилляры. Таким образом, билирубин становится основным пигментом желчи.
Обычно билирубин находится в виде кристаллов красновато-желтого цвета. Он легко окисляется, образуя при этом продукты различного цвета. Именно это происходит при выявлении его по методу Гмелина — при окислении его азотной кислотой образуются продукты сначала зеленого, а затем синего или пурпурного цвета.
Гематоидин — пигмент, не содержащий железа. По химической структуре близок к билирубину и также дает положительную реакцию Гмелина. Гематоидин формирует ярко-оранжевые кристаллы в виде ромбических пластинок, иголок или зерен. Образуется при распаде эритроцитов и гемоглобина, как и гемосидерин, внутриклеточно, но в клетках не остается и при их гибели оказывается свободно лежащим среди некротических масс.
Гематины образуются при гидролизе оксигемоглобина и представляют собой окисленную форму гема, содержащую трехвалентный атом железа в связанном состоянии. Имеют вид темно-коричневых кристаллов или зерен. К гематинам относят малярийный пигмент (гемомеланин), солянокислый гематин и формалиновый пигмент.
Малярийный пигмент (гемомеланин) образуется из гема в теле малярийного плазмодия, который, как известно, паразитирует в эритроцитах. Пигмент построен из буровато-черных аморфных гранул и синтезируется обычно в ретикулярных и эндотелиальных клетках печени, костного мозга, селезенки и лимфатических узлов.
Солянокислый гематин (гемин) образуется исключительно в желудке при взаимодействии гемоглобина, ферментов желудочного сока и соляной кислоты. Пигмент откладывается в виде ромбовидных или игловидных кристаллов.
Формалиновый пигмент образуется в тканях при фиксации их кислым формалином (рН< 5, 6), имеет вид бурых зерен или кристаллов, расположенных, как правило, в просвете венозных сосудов.
Порфирины — предшественники гема, которые имеют строение замкнутых тетрапиррольных колец, лишенных железа. Пигменты повышают чувствительность кожи к ультрафиолетовому облучению, являются антагонистами меланина. Обычно метаболизм порфиринов в организме человека заканчивается на стадии уропорфириногена III, который затем принимает участие в реакциях синтеза гема. При отсутствии фермента уропорфириноген Ш-косинтетазы появляются предшественники уропорфириногена III — уропорфириноген I, порфобилин, порфобилиногены. В норме они в минимальных количествах определяются в тканях, крови и моче: они дают оранжевую флюоресценцию в ультрафиолетовом свете.
|
|
