
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Вміст важких металів у воді
|
|
Одним із проявів антропогенного впливу на екосистему є присутність у воді різних типів водоймищ таких токсикантів як важкі метали, які мають значний вплив на життєдіяльність представників водного біоценозу. Особливу увагу привертають важкі метали (ВМ), зокрема плюмбум та кадмій. В екологічно несприятливих районах у воді надмірно накопичуються ВМ, що призводить до порушення оптимальних співвідношень мікроелементів і зниження біологічних властивостей рослин та тварин [2].
В процесі життєдіяльності рослини використовують макро- і мікроелементи, наприклад ферум, цинк, мідь, свинець, кадмій та інші. Надходження надлишкової кількості елементів у рослинний організм порушує рівновагу між мікро- і макроелементами, що призводить до пригнічення біохімічних процесів [3, 4]. Дослідження рівня ВМ у водному середовищі різних районів Житомирського Полісся свідчать про суттєві коливання їх вмісту. Оцінка хімічного стану природних вод і донних осадків, як правило, базується на визначенні складу і кількісної характеристики ВМ, що має важливе наукове та прикладне значення.
Мета роботи полягала у встановленні особливостей розподілу іонів ВМ у воді та донних відкладах р. Норинь. Об’єктом дослідження слугувала якісна та кількісна характеристика іонів ВМ у поверхневих водах і донних відкладах р. Норинь. Оцінювали воду р. Норинь в межах міста Овруч в чотирьох створах: створ №1 – за 1 км на околиці м. Овруч, 2-й – початок міста, 3-й – 200 м вище скиду очисних споруд та 4-й – 20 м нижче скиду очисних споруд господарсько-побутових стічних вод м. Овруча.
Встановлено, що вміст іонів кадмію у чотирьох зразків води перевищував гранично допустимі концентрації (ГДК) у 2, 6-6, 4 разів, а плюмбуму – в 2-30 разів (рис. 1). Найбільший вміст іона кадмію, відносно фону, відзначений у воді четвертого створу, найнижчий – на окраїні міста, а по місту – ближчі до середнього статистичного значення, проте вище ГДК у 4, 2 та 4, 8 разів. Максимальне значення іонів плюмбуму (0, 34 мг/дм3, ГДК=0, 01 мг/дм3) зафіксовано нижче скиду очисних споруд господарсько-побутових стічних вод м. Овруча, високі показники – в районі міста (0, 24 мг/дм3 ) та низькі – на початку та околиці міста (0, 023 та 0, 031 мг/дм3 відповідно ).
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
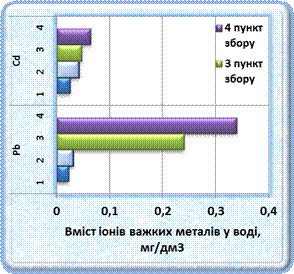

Рис.1. Вміст іонів Cd2+ та Pb2+ у воді та у донних відкладах р. Норинь
Спектральний аналіз показав міру забрудненості донних відкладів важкими металами (рис. 1). Спостерігається аналогічна тенденція накопичення іонів кадмію та плюмбуму у донних відкладах як і в воді, проте темпи акумуляції ВМ у мулі значно вище. У донних відкладеннях р. Норинь вміст кадмію (у валовій формі) варіюється в середньому в межах від 0, 15 – 0, 24 мг/кг та плюмбуму – в межах 0, 35-0, 76 мг/кг.
На даному етапі розвитку суспільства все гостріше постають питання про негативні наслідки забруднення водних екосистем як накопичувачів токсичних речовин. Водні екосистеми піддаються забрудненню важкими металами (ВМ) в результаті природних і техногенних процесів. Підвищення рівнів забруднення природного середовища важкими металами спричиняє зростання їх вмісту в рослинах [1, 2, 3]. Зважаючи на вище викладене, ми поставили за мету оцінити вплив поліметалічного забруднення водного середовища на акумуляцію іонів ВМ у вегетативному тілі Ceratophyllum demersum L., які є досить поширеними макрофітами малих річок в зоні Полісся.
Відбір проб та їх аналіз проводили за загальноприйнятими методиками в гідрохімії, гідробіології та токсикології [2]. Визначення елементарного складу ВМ виконувалося методом атомноадсорбціоної спектрофотометрії на спектрофотометрі С115–1М.
Згідно з результатами лабораторних досліджень води у пункті збору №1 (р. Тетерів) на вміст іонів важких металів (цинку, феруму, мангану), визначалися у кількостях, які не перевищують ГДК (для води господарсько-питного і культурно-побутового користування): цинк – показники нижчі у 4, 4 рази, манган – у 2, 1, окрім феруму, вміст якого перевищував ГДК в 1, 3 рази і становив 0, 329 мг/дм3 (при нормі 0, 1 мг/дм3) (рис.1).
На території глиняного кар’єру (с. Іванівка) вміст іонів феруму перевищував ГДК в 2 раза і становив 0, 591 мг/дм3 (при нормі 0, 3 мг/дм3). Показники іонів цинку не перевищують ГДК для води ГПКПК. Концентрація іонів мангану виявилися у кількостях, нижчих ГДК для води рибогосподарських водоймищ (РГВ) (рис. 1).
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе

Рис. 1. Вміст іонів Цинку, Феруму та Мангану у вегетативних органах C. demersum L.
У пункті збору №3 (р. Кам’янка, с. Тетерівка Житомирського району) показники концентрацій іонів цинку та феруму у воді були нижчими ГДК (ГПКПК) на 28 та 5 % відповідно. Концентрація іонів мангану була на рівні ГДК (РГВ).
Тому в пунктах відбору проб були відібрані не лише проби води на виявлення вмісту важких металів, а й зразки домінуючого виду вищих водних рослин – C. demersum L. З’ясовано, що за однакових умов зростання даний вид рослин накопичують іони важких металів в вегетативних органах неоднаково.
Перше місце по інтенсивності накопичення в вегетативній масі C. demersum L належить мангану. Валовий вміст мангану в рослині характеризувався значним накопичення у вегетативній масі рослин у межах 17, 99-19, 43 мг/кг. Максимальний коефіцієнт накопичення (КН) для даного елемента становить 119 (ПЗ № 2). Різкі зміни вмісту мангану у водному середовищі можуть виникати внаслідок низького ступеня комплексоутворення, а його зниження у вересні – внаслідок міграції у водне середовище і біологічного засвоєння, що корелює зі зниженням рH та зростанням концентрації у воді.
Біогенні елементи ферум та цинк мають важливе значення у фізіологічних процесах рослин, зокрема у ферментативних системах фотосинтезу. Проте восени знижується інтенсивність фотосинтезу і зменшується його концентрація іонів феруму в рослинному організмі. Щодо зростання концентрації феруму у воді восени, то тут можливе його надходження з ґрунтовими водами [2]. Близькі за значенням концентрації феруму зафіксовані у C. demersum L. зібраних на пунктах збору №1-3 (27 мг/кг). КН даного елемента становить в межах 4, 6-9, 5. Іони Цинку мають самі нижчі між іншими ВМ показники КН у межах 1, 3-6.
Таким чином, вода у пункті збору № 2 (р. глиняний кар’єр, с. Іванівка, Житомирського району) не придатна для господарсько-питного і культурно-побутового користування за наявності високої концентрації іонів феруму.
Проведений аналіз вмісту ВМ у вегетативній масі C. demersum L. з приводу видової специфіки накопичення досліджуваних елементів в системі вода-рослина показав, що вони акумулюють ВМ у наступному порядку: манган > ферум > цинк.
Отже, якість води у малій річці Норинь на території Житомирського Полісся за вмістом важких металів перевищує гранично допустиму концентрацію іонів кадмію та плюмбуму в 2, 6-6, 4 разів та в 2-30 разів відповідно. За результатами аналізів поверхневих вод та донних відкладень р. Норинь очевидно, що підвищений вміст іонів кадмію та плюмбуму спричинений в першу чергу неякісним очищенням скиду очисних споруд господарсько-побутових стічних вод м. Овруча.
3.3 Накопичення Zn2+ у тканинах роголисника темно-зеленого
Нами вперше проведено дослідження на накопичення Zn2+ в тканинах роголисника темно-зеленого та визначення кількість накопиченого металу (Zn2+) взалежності від гранично допустимої концентрації (ГДК) та вирахуване відсоткове відхилення ві норми. Результати досліджень поміщені в таблиці (Табл. 1).
Таблиця 1
Вміст Zn2+ у вегетативному тілі роголистника темно-зеленого
| ГДК | Хс ± mx | δ | CV |
| контроль | 3, 946 ± 0, 005 | 0, 01 | 0, 28 % |
| 0, 5 ГДК | 06, 71 ± 0, 004 | 0, 01 | 0, 14 % |
| 1 ГДК | 6, 232 ± 0, 023 | 0, 05 | 0, 85 % |
| 2 ГДК | 5, 81 ± 0, 004 | 0, 01 | 0, 17% |
| 5 ГДК | 5, 38 ± 0, 004 | 0, 01 | 0, 18 % |
| 10 ГДК | 7, 42 ± 0, 003 | 0, 0, 007 | 0, 09% |
Маючи подані результати, було розраховано відсоткове відхилення показників накопиченогоZn 2+ при різних ГДК від контролю.

Рис. 6. Відсоткове відхилення показників накопиченого Zn2+ при різних ГДК від контролю
З даного графіка помітно, що відбуваються помірні і різкі підйоми відсоткового відхилення. У контролі і при 0, 5 ГДК - 5 ГДК відбувається поступове підняття вгору і %-ве відхилення становить близько 110 - 137%. Від контролю до 10 ГДК відбувається різкий стрибок вгору і %-ве відхилення становить близько 384%.
Порівнюючи показники 5 ГДК і 10 ГДК, досить яскраво виражений різкий підйом накопиченого кадмію в тканині до 384%. Значення від 0, 5 ГДК - 5 ГДК майже однакові і відрізняються лише на декілька одиниць 8 - 10% відповідно.
Отже, при низьких концентраціях важкого металу роголисник має меншу протидію до накопичення його тканинами і врезультаті цього відбувається більше його накопичення, але більша частина рослини залишається живою. При вищих концентраціях відбувається більша протидія, оскільки більша частина рослини внаслідок дії металу загинула.
Після семи діб перебування роголисника у розчинах кадмію різної концентрації, було виявлено деяку закономірність. У тканинах рослини вміст важкого металу зменшувався зі збільшенням концентрації кадмію. Цей процес ґрунтується на тому, що чим вища концентрація Cd2+, тим більшу протидію чинитиме рослина, і тим менше металу накопичуватиметься у рослинному організмі.
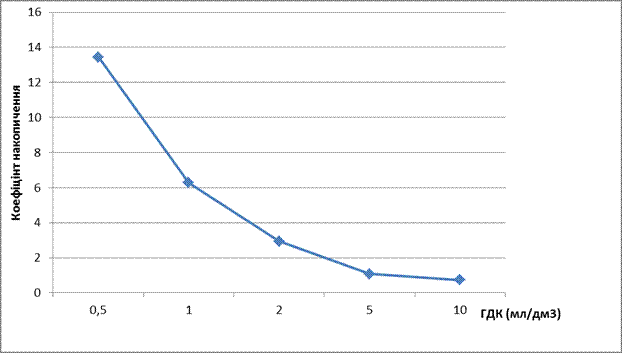
Рис.7. Порівняння коефіцієнту накопичення Zn2+ в тканинах роголистника темно-зеленого
З даного графіка помітно, що відбуваються помірні підйоми відсоткового коефіцієнту накопичення. Порівнюючи показники від 10 ГДК до 0, 5 ГДК, досить яскраво виражений підйом коефіцієнту накопичення цинку в тканині від 0, 742 до 13, 44. Значення від 10 ГДК, 5 ГДК, 2 ГДК майже однакові і відрізняються лише на декілька одиниць. Від 1 ГДК до 0, 5ГДК відбувається різкий стрибок вгору.
|
|
