
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Галогендерге жалпы сипаттама.
|
|

|
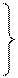
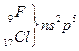 - типтік элементтер, т.э.а.
- типтік элементтер, т.э.а.
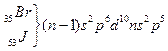
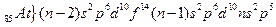
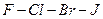 элементтерінің топтық атауы – галогендер («тұ з тү зушілер»).
элементтерінің топтық атауы – галогендер («тұ з тү зушілер»).
Фтор тек – 1, ал басқ алары – 1-ден +7-ге дейін тотығ у дә режесін кө рсетеді. 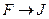 қ атарында
қ атарында 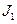 (17, 4→ 10, 5 эВ) жә не СЭТ (4, 0→ 2, 6) кемиді, бірақ ә рбір галоген ө з периодында электртерістігі жоғ ары элемент болады. Электрон тартқ ыштық
(17, 4→ 10, 5 эВ) жә не СЭТ (4, 0→ 2, 6) кемиді, бірақ ә рбір галоген ө з периодында электртерістігі жоғ ары элемент болады. Электрон тартқ ыштық 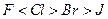 ө згерісінде бұ л қ атарда инверсия қ ұ былысы байқ алады.
ө згерісінде бұ л қ атарда инверсия қ ұ былысы байқ алады.
Фтор табиғ атта 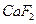 ,
, 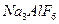 ,
, 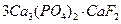 тү рінде кездеседі. Фтор – ашық -сары тү сті, ө ткір иісті газ, ө неркә сіпте
тү рінде кездеседі. Фтор – ашық -сары тү сті, ө ткір иісті газ, ө неркә сіпте 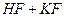 балқ ымасының электролизімен алынады. Ол
балқ ымасының электролизімен алынады. Ол 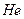 ,
, 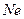 жә не
жә не 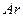 басқ а барлық жай жә не кү рделі заттармен ә рекеттеседі. Бинарлы қ осылыстарының ішінде
басқ а барлық жай жә не кү рделі заттармен ә рекеттеседі. Бинарлы қ осылыстарының ішінде 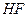 жә не оның тұ здары маң ызды орын алады. Фтор жә не оның қ осылыстары фторопластар, тоң азытқ ыш агенттер, т.б. галогендер фторидтері ракеталық отынның тотық тырғ ыштары ретінде қ олданылады.
жә не оның тұ здары маң ызды орын алады. Фтор жә не оның қ осылыстары фторопластар, тоң азытқ ыш агенттер, т.б. галогендер фторидтері ракеталық отынның тотық тырғ ыштары ретінде қ олданылады.
Хлор – сарғ ыш-жасыл ө ткір иісті газ. Хлор да фтор сияқ ты айқ ын тотық тырғ ыштық қ асиет кө рсететін бейметалл. Сондық тан хлор бинарлы жә не кү рделі қ осылыстарда анионтү зуші ролін атқ арады. Негіздік хлоридтер іс жү зінде гидролизге ұ шырамайды, қ ышқ ылдық хлоридтер қ ышқ ылдар тү зе отырып, толық жә не қ айтымсыз гидролизденеді.
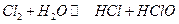
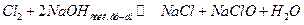
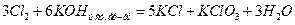
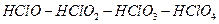 қ атарында солдан оң ғ а қ арай қ ышқ ылдық қ асиеті артады, ал тотық тырғ ыштығ ы кемиді.
қ атарында солдан оң ғ а қ арай қ ышқ ылдық қ асиеті артады, ал тотық тырғ ыштығ ы кемиді. 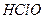 - кү шті тотық тырғ ыш, ал оның тұ здары – гипохлориттер ағ артқ ыш зат ретінде қ олданылады.
- кү шті тотық тырғ ыш, ал оның тұ здары – гипохлориттер ағ артқ ыш зат ретінде қ олданылады.
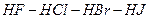 қ атарында қ ышқ ылдық жә не тотық сыздандырғ ыштық қ асиеттері солдан оң ғ а қ арай ұ лғ аяды.
қ атарында қ ышқ ылдық жә не тотық сыздандырғ ыштық қ асиеттері солдан оң ғ а қ арай ұ лғ аяды.
|
|