
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Метилтрансфераза
|
|
 Гомоцистеїн Метіонін
Гомоцистеїн Метіонін
Порушення вищенаведеної реакції призводить до акумулю-вання фолату у вигляді N5-метил-ТГФК. Метильована форма не може прямо перетворюватися на інші форми тетрагідрофолевої кислоти. Таким чином, створюється дефіцит фолату і ТГФК, які виключаються з метаболізму, у тому числі з реакцій синтезу тимідилових нуклеотидів, що призводить до інгібування утворення ДНК.
Причини гіповітамінозу В12
У зв′ язку із достатньою кількістю вітаміну у продуктах тваринного походження дефіцит його не виникає у здорових людей при змішаному харчуванні. Загалом виділяють три основні групи причин розвитку гіпо- та авітамінозівВ12:
1) недостатнє надходження з їжею;
2) порушення всмоктування у ШКТ;
3) уроджені порушення метаболізму кобаламіну.
1. Захворювання шлунка та кишечнику (гіпо- та антацидні гастрити, рак шлунка, хронічний панкреатит, інвазії гельмінтами, мальабсорбція). Оперативне видалення частини шлунка або кишечнику призводить до порушення всмоктування кобаламіну через зменшення синтезу «внутрішнього фактора Касла», у результаті чого розвивається злоякісна анемія.
2. Нефізіологічне харчування. Дієта з низьким вмістом вітаміну В12і високою концентрацією фолієвої кислоти (вегетаріанська дієта) часто викликає розвиток прихованого гіповітамінозу. Тому вегетаріанці можуть отримувати цей вітамін із бобових рослин.
3. Анемія Аддисона-Бірмера – аутоімунне захворювання, викликане утворенням аутоантитіл до компонентів водневого насоса та гастринового рецептора обкладинкових клітин слизової оболонки шлунка, або аутоантитіл до внутрішнього фактора Касла.
4. Спадкові дефекти синтезу ферментів для перетворення вітаміну В12у коферментні форми, недостатність або функціо-нальна неактивність внутрішнього фактора Касла, муковісцидоз.
5. Використання закису азоту для наркозу (при пролонгованій дії).
6. Куріння тютюну, яке викликає швидку інактивацію вітаміну.
7. Дефіцит вітаміну може виникати при підвищенні потреби в ньому при гіпертиреозі, злоякісних пухлинах тощо.
8. Утилізація вітаміну знижується при надмірному вживанні алкоголю.
Клінічні та біохімічні прояви недостатності вітаміну В12
На відміну від інших водорозчинних вітамінів кобаламінможе накопичуватися в організмі у значній кількості (4 – 5 мг) і у разі часткової чи повної гастроектомії або при дефіциті внутрішнього фактора симптоми гіповітамінозу розвиваються тільки через декілька років.
Прояви недостатності вітаміну В12
· «Печіння язика», глосит – один із ранніх симптомів недостатності вітаміну;
· розвиток перніціозної анемії – зменшення кількості еритроцитів, збільшенням їх об¢ єму та форми, зниження рівня гемоглобіну;
· збільшення печінки, селезінки, болі у животі, анорексія, запори, проноси, зниження маси тіла;
· поєднання гематологічних проявів із порушеннями перифе-ричної нервової системи. Недостатність вітаміну В12є однією з причин дисфункції мозку у людей похилого віку;
· атрофія слизової оболонки шлунка та кишечнику, розвиток глоситів, стоматитів, фарингітів, хейлітів («полірований» кінчик язика), ахлоргідрія;
· ураження задніх і бокових стовпів спинного мозку;
· безплідність та викидні, які повторюються.
Біохімічні порушення:
· накопичення і підвищене виділення з сечею метилмалонової кислоти. Метилмалонова ацидурія– чутливий показник недостатності вітаміну В12, що відрізняє цю патологію від недостатності фолієвої кислоти; г омоцистеїнурія;
· порушення перетворення рибонуклеотидів на дезоксирибо-нуклеотиди; зниження концентрації кобаламіну в крові та сечі при збільшенні його вмісту у фекаліях;
· поява аутоантитіл до внутрішнього фактора та клітин слизової оболонки шлунка;
· збільшення кількості РНК і зниження синтезу ДНК у еритроцитах через:
o припинення утворення тимідилових нуклеоти-дів шляхом метилюваннядезоксиуридилових нуклеотидів.
· порушення мітозу – подовження фази спокою;
· зниження синтезу холінучерез дефіцит метіонінуі, як наслідок, порушення утворення ацетилхоліну, фосфоліпідіві екскреції ліпопротеїнів печінкою;
· збільшення вмісту метилмалонової та пропіонової кислот призводить до утворення нефізіологічних жирних кислот з непарною кількістю атомів вуглецю, які включаються у ліпіди нейронів, викликаючи жирову дистрофію нервових клітин;
· виділення метилмалонової кислоти з сечею (метилмалонова ацидурія) є чутливим тестом для діагностики гіповіта-мінозу В12.
Застосування вітаміну В12
Кобаламін використовують для лікування В12-дефіцитної анемії, а також анемій іншої етіології, безплідність, уражень спинного мозку і переферичних нервів, захворювань шкіри, при гострих і хронічних гепатитах, променевій хворобі та ін.
4.8. Біотин (вітамін H)
(біос, коензим R, антисеборейний)
Хімічна структура та властивості
· біотин– сірковмісний водорозчинний вітамін, циклічне похідне сечовини з бічним ланцюгом, який представлений валеріановою кислотою:
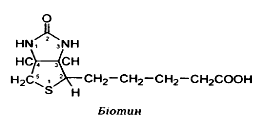
· у природі зустрічаються дві однаково активні форми вітаміну – α -біотин у жовтку яєць і β -біотину печінці, які відрізняються лише природою бічного ланцюга;
· у тканинах біотиніснує у вільній та зв’язаній формах. Останні представлені біоцитином, у якому карбонільна група біотину утворює амідний зв’язок із ε -аміногрупою лізину, дезтіобіотином, оксибіотином.
Біосинтез
Біотинпродукуютьбактерії, дріжджі, гриби. Він утворюється у зеленому листі та коренях рослин. В організмі людини не синтезується і повинен надходити з їжею, але бактеріальна мікрофлора ШКТ може синтезувати вітамін у достатній кількості.
Метаболізм
Всмоктування та накопичення. Біотин їжі потрапляє у кишечник переважно у складі біотиновмісних білків, з яких під дією протеаз ШКТ вивільняється біоцитин. Останній гідролізу-ється до біотину та лізину під дією ферменту підшлункової залози біоцитинази, потімвсмоктується у кишечнику. У крові вітамін транспортується альбумінами і відкладається у незначній кількості у печінці та нирках.
Виділення. При нормальному забезпеченні з сечею виводиться 10 – 180 мг біотину, з фекаліями – 15 – 200 мг/добу.
Поширення у природі та добова потреба
Вітамін Нпоширений у тканинах рослин і тварин переважно у зв’язаній формі.
Джерела:
· продукти рослинного походження: картопля, цибуля, горох, квасоля, томати, шпинат, соя, арахіс;
· продукти тваринного походження: печінка, нирки, молоко, жовток яєць, шоколад, гриби;
· важливим джерелом вітаміну для організму людини та тварин є його синтез мікрофлорою кишечнику. Людина виділяє з фекаліями більше біотину, ніж засвоює.
Добова потреба у біотині становить приблизно 0, 25 мг/добу. Потреба підвищується при вагітності, лактації, довготривалому пероральному вживанні антибіотиків та сульфаніламідних препаратів, які пригнічують розвиток мікрофлори кишечнику.
Біологічна роль
Біотин є простетичною групою ферментів, які каталізують два типи хімічних реакцій: карбоксилювання, або фіксації СО2, та транскарбоксилювання – перенесення СО2 між субстратами.
1. Ферменти карбоксилюванння – карбоксилази каталізують реакції засвоєння СО2 в організмі тварин. Процес охоплює дві стадії:
· На першій – СО2 «активується», утворюючи ковалентний зв’язок із біотином в активному центрі ферменту із формуванням карбоксибіотину. N5 – карбоксибіотин вважається коферментною формою вітаміну Н.
СО2 + Enz-біотин Карбоксилаза Enz-біотин- СОО-


АТФ, Н2О АДФ, Фн, 2Н+
· Карбоксибіотин– джерело «активного СО2», який переноситься на різні субстрати на другій стадії реакції. Реакцією першого типу є перетворення пірувату на оксалоацетат у піруваткарбоксилазнійреакції:
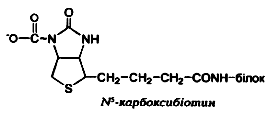
2. У реакціях транскарбоксилюваннякарбоксильна група переноситься з одного субстрату на інший, без використання АТФ. Прикладом такої реакції є метилмалоніл-оксалоацетат-транскарбоксилазна реакція:
S1-COOH + S2H↔ R1H + R2-COOH.
Реакції карбоксилюваннята транскарбоксилюваннянаявні у шляхах перетворення жирних кислот, пуринів, білків, окремих амінокислот. Приклади біотинозалежних ферментів наведені у табл. 5.
Таблиця 5 – Біотинозалежні ферменти
| Назва ферменту | Схема реакції |
| Піруваткарбоксилаза | ПВК → Оксалоацетат |
| Ацетил-КоА-карбоксилаза | Ацетил-КоА → Малоніл-КоА |
| Пропіоніл-КоА-карбоксилаза | Пропіоніл-КоА → Метилмалооніл-КоА |
| Метил-кротоніл-КоА-карбоксилаза | β – Метилкротоніл-КоА→ β –Метилглутаконіл-КоА |
| Метилмалоніл-оксалоацетат-транскарбоксилаза | Малоніл-КоА + ПВК → Пропіоніл-КоА + Оксалоацетат |
Прояви вітамінної недостатності
Гіповітамінозсупроводжується розвитком себорейного дер-матиту носогубного трикутника та волосистої частини голови, випадінням волосся (алопецією), кон′ юктивітом, підсиленим виділянням сала сальними залозами, пошкодженням нігтів, болями у м’язах, анемією, паралічем нижніх кінцівок.
Основні причини гіповітамінозу вітаміну Н
Вітамін дуже поширений у природі, тому гіповітаміноз біотину у чистому вигляді не зустрічається, але дефіцит може розвинутися при:
· уродженій недостатності ензиму синтази холокарбокслази, який бере участь в утилізації біотину. Недостатність ензиму супроводжується дерматитами, посивінням волосся, алопе-цією, дезорієнтацією у просторі. З сечею екскретується значна кількість лактату, β -гідрокси-пропіонату, β -метил-кротонату;
· хворобі Лейнера, яка розвивається у новонароджених при годуванні грудним молоком на фоні тривалої діареї. Низька концентрація біотину у грудному молоці та погана абсорбція біотину в кишечнику через діарею призводять до розвитку вітамінної недостатності;
· гіповітамінозрозвивається при мальабсорбції, споживанні великої кількості сирого яєчного білка (12 білків за добу), парентеральному харчуванні, довготривалому пероральному прийманні антибіотиків та сульфаніламідних препаратів.
Антивітаміни та застосування вітаміну Н
Авідин– антивітамін біотину.Цеглікопротеїн з основними властивостями, що міститься у білку курячого яйця і комоле-ментарно, незворотно зв′ язується з біотином у нерозчинний комплекс, що не перетравлюється у кишечнику.
У медицині біотинвикористовують для лікування дерматитів.
4.9. Вітамін С
(аскорбінова кислота, антискорбутний вітамін)
Хімічна структура та властивості
· Аскорбінова кислота– лактон дієнолгулонової кислоти, яка за своєю структурою схожа на L-глюкозу.
· Це відносно сильна кислота. Кислотний характер її зумовлений наявністю двох енольних гідроксилів біля С2 та С3, які зворотно дисоціюють.
· Аскорбінова кислотаутворює чотири оптичні ізомери за рахунок наявності двох асиметричних атомів вуглецю – С4 та С5. D-ізомери зовсім неактивні. Вітамінну активність мають тільки природні ізомери L-ряду.
· Вітамін Сдобре розчинний у воді та практично не розчин-ний в органічних розчинниках. Тверда форма та кислі розчини його стабільні, але він швидко розщеплюється у лугах. Окиснювальна деградація аскорбінової кислоти прис-корюється при підвищенні рН, за наявності іонів Ag++, Cu++.
· Відновлювальні властивості аскорбінової кислоти пов'язані з її здатністю зворотно окиснюватися до дегідроаскорбінової кислоти, утворюючи окисно-відновну систему.



 О=С О=С
О=С О=С
│ │
НО-С -2 Н+ О=С


 ║ О │ О
║ О │ О
 НО-С О=С
НО-С О=С
│ +2 Н+ │

 Н-С Н-С
Н-С Н-С
│ │
|
|