
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Гемоглобін
|
|
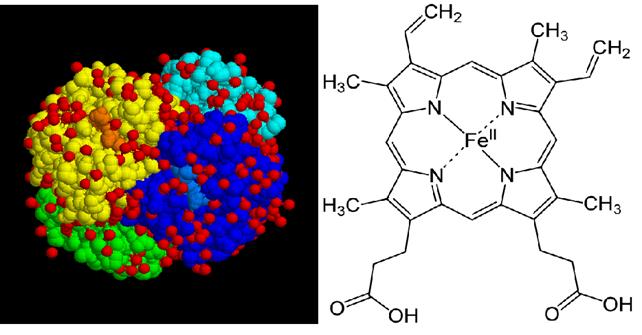 Еритроцити містять дихальний фермент — гемоглобін (Нb), що обумовлює червоний колір крові (рис. 14).
Еритроцити містять дихальний фермент — гемоглобін (Нb), що обумовлює червоний колір крові (рис. 14).
Рис. 14. Молекула гемоглобіну: 4 ланцюги глобіну забарвлено в різні кольори. Зправа структурна формула гему, що містить двовалентне залізо.
На долю гемоглобіну приходиться 34 % загальної і 90 % сухої ваги еритроцита, тобто більша частина його маси. Загальна кількість гемоглобіну в крові варіює в залежності від індивідуальних особливостей, але в середньому його кількість дорівнює: 130–160 г/л крові в чоловіків і 120–140 г/л у жінок, що в загальному для людини з масою 65 кг складає приблизно 600 г. Встановлено також, що 1 м Нb містить 3, 5 мг заліза, тобто у всіх еритроцитах організму його міститься біля 2500 мг.
Гемоглобін являє собою складну хімічну сполуку, що складається з 600 амінокислот, його молекулярна маса дорівнює 66 000 ± 2000. Гемоглобін складається з білкової і небілкової частини: білка глобіну і чотирьох молекул гему. Молекула гему, що містить атом заліза, має здатність приєднувати чи віддавати молекулу кисню. При цьому валентність заліза, до якого приєднується кисень, не змінюється, тобто залізо залишається двовалентним (Fe2+). Гем є активною, чи так званою простетичною групою, а глобін — білковим носієм гему.
Розрізняють три основних фізіологічних сполуки гемоглобіну:
Оксигемоглобін — гемоглобін, зв’язаний з киснем (Hb2 або HbО), утворюєтьсяв легеневих капілярах у зв’язку з високим парціальним тиском кисню в альвеолах.
Дезоксигемоглобін (відновлений) — гемоглобін, що віддав кисень (Hb) у тканинах у зв’язку з високим напруженням в них вуглекислого газу.
Карбгемоглобін — сполука гемоглобіну з вуглекислим газом (HbСО2).
Крім фізіологічних сполук гемоглобіну, існують патологічні:
Карбоксігемоглобін — сполука гемоглобіну з чадним газом (СО), тому що спорідненість заліза до СО перевищує його спорідненість до кисню в 300 разів.
Метгемоглобін (MetHb) — сполука гемоглобіну із сильними окислювачами (перманганат калію, аміл і пропілнітрит, фенацетин), при якому залізо гему з двовалентного перетворюється в тривалентне. При накопиченні цих сполук гемоглобіну в крові порушується транспорт кисню, що призводить до розвитку кисневого голодування.
У посмугованих м’язах, до яких належать скелетні м’язи і м’яз серця, знаходиться речовина аналогічна гемоглобіну і за місцем локалізації називається міоглобіном. Подібність між гемоглобіном і міоглобіном полягає в наявності однієї і тієї ж простетичної групи, однакової кількості заліза, у здатності вступати в зворотні сполуки з киснем і вуглекислим газом.
Корінною відмінністю міоглобіну є менша, ніж у гемоглобіну, щільність його білкової частини — глобіну, що різко підвищує його спорідненість до кисню. Тому міоглобін пристосований до депонування кисню. Міоглобін людини зв’язує до 14 % загальної кількості кисню в організмі. Це має велике значення для постачання киснем м’язів, що особливо ритмічно працюють протягом тривалого часу (м’язи кінцівок, жувальні м’язи, м’яз серця).
У фазі скорочення відбувається перетискання капілярів з фактичним припиненням кровотоку через м’яз. У цей період міоглобін служить одним з основних джерел кисню для працюючої тканини, томущо акумуляція кисню відбувається в період розслаблення м’яза, а віддача його — у період скорочення.
Період напівнасичення міоглобіну киснем відбувається швидше ніж за 0, 1 с, завдяки його високій спорідненості до кисню.
Руйнування еритроцитів з виходом гемоглобіну в плазму крові на зивається гемолізом.
У залежності від фактора впливу на еритроцити розрізняють такі види гемолізу:
— осмотичний — дія на еритроцит гіпотонічних розчинів;
— хімічний — під дією речовин, що руйнують оболонку еритроци
та — кислоти, лугу;
— механічний — інтенсивне струшування ампули з кров’ю;
— термічний — заморожування і розморожування крові;
— біологічний — переливання іншогрупної крові, бактеріально забрудненої, при укусах змій, при дії імунних гемолізинів.
9.2.3. Швидкість осідання еритроцитів (ШОЕ)
У крові еритроцити знаходяться у зваженому стані. Якщо кров помістити в пробірку з доданням антикоагулянту, то через якийсь час можна побачити, що кров розділилася на два шари. Верхня частина являє собою шар прозорої жовтуватої рідини — плазми, нижня — щільний осад, що містить формені елементи, в основному, еритроцити. Це обумовлено тим, що відносна щільність плазми крові дорівнює 1, 027 г/мл, а еритроцитів — 1, 090 г/мл.
Швидкість осідання еритроцитів виражається в міліметрах висоти стовпа плазми над шаром осілих еритроцитів за одиницю часу (1 година). У нормі швидкість осідання еритроцитів в чоловіків за 1 годину складає 1–10 мм, у жінок — 2–15 мм.
Осідання еритроцитів обумовлене кількістю еритроцитів, їхніми морфологічними особливостями, величиною заряду, здатністю до агломерації, білковим складом плазми.
Реакція осідання еритроцитів характеризує деякі фізико-хімічні особливості крові при певних фізіологічних чи патологічних станах організму. Прискорення реакції осідання відбувається при вагітності, при різних запальних процесах в організмі. Реакція осідання еритроцитів використовується як діагностичний тест в амбулаторній і клінічній практиці.
|
|