
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Сократительные белки
|
|
Безусловно, основной функцией гладкомышечной клетки является сокращение. За реализацию этой функции отвечают в первую очередь сократительные белки - актин и миозин. Взаимодействие между актином и миозином регулируется с участием целого ряда процессов, которые рассмотрены в главе «Регуляция сокращения».
Актин
Белок актин является важным компонентом цитоскелета клетки и обнаруживается почти во всех клетках животных и растений. Актин получил название благодаря своей способности активировать гидролиз АТФ. Актиновые миофиламенты – имеют длину более 1 мкм, толщину 3-8 нм, прикрепляются к плотным тельцам. Около 12 актиновых филаментов окружают миозиновые филаменты в виде розетки. Актиновые микрофиламенты состоят из глобулярных субъединиц G-актина - мономеров актина (диаметр 5, 6 нм и молекулярный вес 42000 дальтон), которые полимеризуются в фибриллярный F-актин. Актин образован спирально переплетенными цепочками F-актина [50, 299].
Процесс полимеризации глобулярных субъединиц G-актина возможен благодаря способности актина образовывать межмолекулярные контакты после гидролиза АТФ до АДФ и неорганического фосфата. Мономеры актина собираются в полимер в определенном порядке, причем полимеризацию актина инициирует активация сокращения [128]. Процесс полимеризации и деполимеризации актина регулируется с помощью особых белков. Например, имеется особый белок профилин, который, образуя комплекс с глобулярным актином, противодействует полимеризации актина. Есть специальные белки (например, цитохалазин D), которые связываются с актином и «кеппируют» его, т.е. образуют некое подобие шапочки на одном из концов полимеризующегося актина, регулируя тем самым процесс полимеризации. Существуют белки (латрункулин А), которые предотвращают полимеризацию глобулярного актина и белки, которые «разрезают» нити актина на короткие фрагменты. И наоборот, имеются белки, которые «сшивают» уже сформировавшиеся нити актина, образуя при этом упорядоченные жесткие пучки нитей актина или крупноячеистые гибкие сети (рис.3). [3, 60, 123, 190, 206, 226, 237, 266, 284, 285, 359].
В тканях позвоночных обнаружено 6 изоформ актина, которые являются производными различных генов и различаются по аминокислотной последовательности. В сосудистой гладкомышечных клетках присутствует α -изоформа, в гладких мышцах желудочно-кишечного тракта γ -изоформа актина [183, 230].
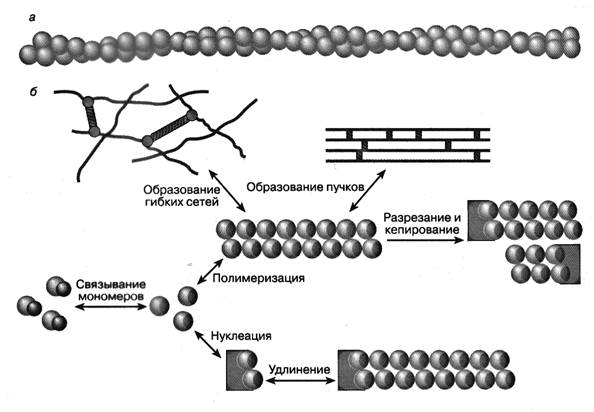
Рис.3. Фибриллярный F-актин (а). Схема процесса полимеризации и деполимеризации нитей актина (б). P – неорганический фосфат.
Миозин
В настоящее время обнаружено более десяти различных изоформ миозина. Наиболее подробно изучен миозин скелетных мышц. Гладкие мышцы имеют свои собственные изоформы миозина [91, 262].
Миозиновые филаменты – имеют длину около 0, 5мкм и толщину 12-15нм состоят из нескольких молекул мономеров миозина. Гладкомышечный миозин относится к классу миозинов II, так называемому классическому миозину, который состоит из двух тяжелых цепей (с мол. массой 200 – 250 кДа, длиной 150 нм и толщиной 1, 52 нм). Молекулу миозина составляют субъединицы-меромиозины: 1) легкий меромиозин, образующий стержень или хвост миозинового филамента; и 2) тяжелый меромиозин, состоящий из фрагмента S-1, который образует головку и фрагмента S-2 (шарнирного участка), который прилегает к стержню миозинового филамента и соединяет фрагмент S-1 с субъединицей легкого меромиозина (рис. 4). Тенденция хвостов мономеров к упорядоченному взаимодействию друг с другом лежит в основе формирования филаментов. На головке миозина располагаются две легкие цепи - регуляторная и основная, с молекулярной массой 18 – 28 кДа, которые участвуют в процессе взаимодействия миозина с актином. Существует гипотеза, что в отсутствие ионов Са2+ легкие цепи обернуты вокруг шарнирного участка тяжелой цепи миозина, что значительно ограничивает его подвижность. В таком состоянии головка миозина не способна перемещаться относительно актиновой нити. В присутствии же ионов Са2+ подвижность в области головки резко увеличивается и после гидролиза АТФ головка миозина может продвигаться вдоль актиновых нитей [8, 109, 120, 210, 261, 263, 324, 364].
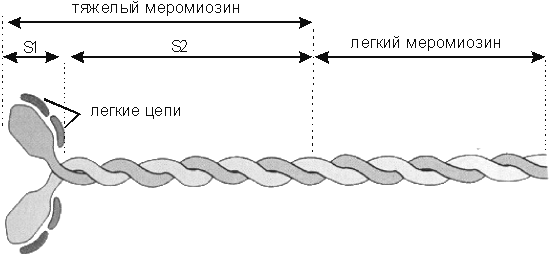
Рис.4. Строение макромолекулы миозина (объяснение в тексте).
Миозиновые филаменты в гладкомышечной клетке не всегда определяются под микроскопом, поэтому полагают, что они образуются и обратимо распадаются при каждом сокращении гладкой мышцы [157]. Гладкомышечный миозин значительно отличается от скелетного тем, что в присутствии физиологических концентраций АТФ он находится в так называемой свернутой (10S) конформации. В этой конформации участок мономера миозина приблизительно в 1/3 от конца хвоста взаимодействует с областью шейки). При этом внутримолекулярные взаимодействия в гладкомышечном миозине преобладают над межмолекулярными, не происходит ассоциации хвостов и равновесие сдвинуто в сторону мономерного миозина. В реакцию полимеризации вступают молекулы миозина в развернутой (6S) конформации (рис.5) [8]. Гладкомышечный миозин полимеризуется в филаменты при фосфорилировании его легкой цепи специальным ферментом – киназой легких цепей миозина или при взаимодействии с белком KRP (kinase-related protein).
Хорошо изученные миозиновые филаменты скелетных мышц собираются в биполярные гантелеобразные филаменты, в которых головки миозина располагаются радиально вокруг оси филамента с обеих сторон, при этом центральная часть молекулы головок не содержит. В отличие от скелетных, гладкомышечные миозиновые филаменты имеют боковую полярность, т.е. головки миозиновых молекул расположены в одной плоскости с двух сторон филамента по всей его длине и имеют противоположную ориентацию (рис.5) [8, 68].
Скорость диссоциации димеров от филамента прямо пропорциональна его длине, поэтому рост биполярных миозиновых филаментов скелетных мышц самоограничивается. Этот эффект не наблюдается в гладкомышечных миозиновых филаментах (которые обладают боковой полярностью) и поэтому они могут изменять длину в широких пределах за счет эквивалентного присоединения новых молекул миозина, что позволяет перемещать актиновые филаменты на большие расстояния. Вероятнее всего, подобная организация гладкомышечных миозиновых филаментов лежит в основе способности гладких мышц к развитию значительного укорочения [8, 143].

Рис.5. Модель гладкомышечного миозинового филамента. А – свернутая конформация, Б – развернутая конформация, В – полимеризованный миозин гладкой мышцы, Г – полимеризованный миозин скелетной мышцы.
В гладкомышечных клетках отсутствует белок тропонин, вместо него в саркоплазме присутствует структурно близкий белок кальмодулин. Ca2+ реализует большинство из своих физиологических функций, взаимодействуя со специфическими Ca2+ связывающими белками, которые выполняют и Ca2+ сенсорную и регуляторную функции. Таким белком в гладкомышечной клетке является кальмодулин. В сущности, кальмодулин вовлекается во все Ca2+-завиcимые процессы в клетке. Общая внутриклеточная концентрация кальмодулина в клетке значительно ниже, чем общая концентрация его внутриклеточных мишеней, что позволяет ему являться своеобразным лимитирующим регуляторным фактором. Комплекс Ca2+/кальмодулин необходим для активации киназы легкой цепи миозина и инициации сокращения. С другой стороны, Ca2+/кальмодулин-зависимый белок фосфатаза инициирует дефосфорилирование легких цепей миозина, что приводит к расслаблению. Присутствующая в гладкомышечной клетке Ca2+/кальмодулин-зависимая протеинкиназа II является медиатором многих Ca2+-зависимых внутриклеточных сигнальных путей [162, 167, 169, 381].
Функция тропомиозина в отсутствие тропонина в гладкомышечной клетке не совсем понятна, однако в настоящее время существуют экспериментальные доказательства участия тропомиозина в регуляции цикла образования поперечных мостиков и в процессе ингибирования АТФ-азной активности актомиозина кальдесмоном [300].
Таким образом, если сравнивать сократительный аппарат гладкомышечной клетки со скелетной мышцей, то можно отметить, что отличительными структурными особенностями являются: 1) отсутствие саркомера; 2) неадекватное соотношение нитей актина и миозина в состоянии покоя: нитей актина значительно больше; 3) нити актина более длинные, чем в скелетной мышце; 4) аналогом Z-линии являются плотные тельца и плотные бляшки; 5) аналогом тропонина С является белок кальмодулин; 6) аналогом Т-трубочки – кавеолы; 7) саркоплазматический ретикулум в гладкомышечной клетке менее развит, чем в скелетной.
|
|