
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Метод конденсации
|
|
Эти методу весьма разнообразны и наиболее употребительны на практике. Остановимся на самых основных из них.
1. Метод замены растворителя заключается в замене одной дисперсионной среды, с которой вещество дисперсной Фазы образует молекулярный раствор, другой, в котором это вещество не растворимо. Так, например, при вливании спиртового раствора канифоли в большое количество воды, в которой канифоль не растворима, образуется прозрачный опалесцирующий золь.
2. Метод конденсации паров, разработанный С.З. Рогинским и А.И. Шальниковым, заключается в том, что при испарении в вакууме вещества, образующие две фазы, совместно конденсируются на охлаждённой поверхности. Таким образом могут быть получены золи высокой чистоты, например, органозоли Na, K, Hg, гидрозоли Hg, Cd, P, S.
3. Химические методы заключаются в образовании трудно растворимого вещества в результате химической реакции, протекающей в жидкой фазе, которая в дальнейшем служит дисперсионной средой. Стабилизатором обычно является одно из вступающих в реакцию веществ.
Опыт №1. ПОЛУЧЕНИЕ ЗОЛЯ ОКСОГИДРОКСИДА ЖЕЛЕЗА
Реакция получения оксогидроксида железа идёт по схеме:
FeCl3 + 2H2O 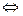 FeO(OH) + 3HCl
FeO(OH) + 3HCl
Поверхностные молекулы агрегата FeO(OH) вступают в химическое соединение с HCl:
FeO(OH) + HCl 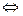 FeOCl + H2O
FeOCl + H2O
Молекулы FeOCl подвергаясь диссоциации, образуют ионы FeO+ и Cl-.
Руководствуясь правилом С.Ц. Липатова, заключающихся в том, что из растворов на поверхности коллоидных частиц адсорбируются ионы, близкие по своей природе к составу ядра, схематически можно изобразить строение частиц золя оксогидроксида железа следующим образом:
FeOCl 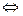 FeO+ + Cl-
FeO+ + Cl-
[mFeO(OH)] + nFeO+ + nCl- 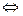 {[FeO(OH)]m nFeO+ (n-x) Cl-}x+ x Cl-
{[FeO(OH)]m nFeO+ (n-x) Cl-}x+ x Cl-
Практически это делается так. В конической колбе нагревают до кипения 85 мл дистиллированной воды. Не снимая колбы с сетки, в кипящую воду приливают по каплям 15 мл 2%-ного раствора хлорида железа (III). После нескольких минут кипячения получается в результате гидролиза красно-коричневый золь оксогидроксида железа (III).
При охлаждении реакция идёт в обратную сторону. Поэтому полученный гидрозоль рекомендуется ещё горячим подвергнуть диализу.
|
|