
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Коллоидные системы и предмет коллоидной химии
|
|
Электролитная коагуляция гидрофобных золей.Взаимная коагуляция золей.
КЛАССИФИКАЦИЯ КОЛЛОИДНЫХ СИСТЕМ
Классификация лиофобных коллоидных систем может быть дана, прежде всего, по агрегатному состояние каждой из двух фаз, образующих коллоидную систему. Беря за основу три агрегатных состояния дисперсное среды – газовое (Г), жидкое (Ж) и твёрдое (Т). Оствальд предложил классифицировать эти системы на три основных типа с подразделением каждого типа на классы по трём агрегатным состояниям дисперсной фазы (табл. 1).
Таблица 1
Классификация коллоидных систем по агрегатному состоянию фаз.
| Тип по дисперсной среде | Дисперсная фаза | Символ системы | Наименование системы |
| Аэрозоли (Г) | Жидкая | Ж - Г | Туман |
| Твёрдая | Т - Г | Дым | |
| Лиозоли (Ж) | Газовая | Г - Ж | Пена |
| Жидкая | Ж(1) - Ж(2) | Эмульсия | |
| Твёрдая | Т - Ж | Суспензоид | |
| Твёрдые золи (Т) | Газовая | Г - Т | Ксерогель |
| Жидкая | Ж - Т | Капиллярные системы | |
| Твёрдая | Т - Т | Стекло, самоцветы, сплавы. |
Наиболее изученными и практически важными из этих восьми классов коллоидов является лиозоли и именно им будет уделено основное внимание в вашем курсе. Лиозоли (жидкие золи), или собственно коллоидные растворы в зависимости от химического состава их дисперсной среды, принято разделять на гидрозоли, если дисперсной средой является вода (например, гидрозоли золота, серебра, описи железа), и органозоли; если дисперсионной средой является какая – либо органическая жидкость (например, алкогозоли, альдозоли).
Коллоидные системы и предмет коллоидной химии
Коллоидная химия - это наука об особых свойствах гетерогенных высокодисперсных систем и о протекающих в них процессах.
Дисперсной системой называется такая система, в которой вещество находится в состоянии более или менее высокого раздробления (дисперсности) и равномерно распределено в окружающей среде. Степень дисперсности D определяется, как величина, обратная величине размера (диаметра) дисперсной частицы а:
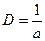 , м-1
, м-1
По степени дисперсности все микродисперсные системы можно разделить на три группы: грубодисперсные (а > 10-6 м), коллоидно-дисперсные (а = 10-6-10-8 м) и молекулярно(ионно)-дисперсные (а < 10-8 м).
Из трех групп наиболее всестороннему и глубокому изучению подвергались дисперсные системы третьей группы, известные под общим названием – истинных или молекулярных растворов. Системы эти сравнительно просты по составу и структуре (дискретными единицами в них являются либо простые молекулы, либо ионы), а поведение их определяется простыми и четкими закономерностями; образовываться они могут самопроизвольно и являются системами устойчивыми и термодинамически разновесными, подчиняющимися правилу фаз.
Вторая группа дисперсных систем, получивших название коллоиднодисперсных, являлась основным объектом изучения коллоидной химии, а системы приобрели название коллоидных систем. В этих системах кинетической и структурной единицами являются не ион и не молекула, а более высокоорганизованные единицы вещества – либо в виде сложного комплекса из обычных молекул, атомов или ионов, названных мицеллами, либо в виде макромолекул, т.е. молекул-полимеров гигантских размеров ~10-6–10-8 м.
В зависимости от того, какими путями достигается коллоидная степень дисперсности вещества дисперсной фазы, методы получения золей могут быть подразделены на две группы:
1) методы диспергирования (раздробления), если коллоидная степень дисперсности достигается путём раздробления грубодисперсного вещества;
2) методы конденсации, если коллоидная степень дисперсности достигается, наоборот, путём соединения атомов, ионов и молекул в более крупные частицы (агрегаты) коллоидных размеров, т.е. порядка 100–1 мкм.
Методы, применяемые для диспергирования, могут быть разделены на четыре группы.
1. Метод механического диспергирования заключается в энергичном и продолжительном растирании, размалывании, распылении и прочих чисто механических приёмах раздробления вещества дисперсной фазы и в дальнейшем или (одновременном) смешивании его с жидкостью, служащей дисперсной средой, а также в добавлении стабилизатора.
2. Метод электрического диспергирования заключается в распылении металла, служащего электродом (катодом) в вольтовой дуге, образуемой при сближении электродов внутри дисперсионной жидкости, в которой прибавляется немного щёлочи. Этим методом получают гидрозоли благородных металлов (золота, платины, серебра, ртути).
3. Метод химического диспергирования или метод пептизации, является наиболее важным и употребительным. Сущность пептизации заключается в том, что прибавление к свежеполученному рыхлому осадку диспергируемого вещества небольших количеств пептизатора (чаще всего – электролита) уменьшает взаимодействие между частицами осадка (например, путём сообщения им зарядов или повышения их сольватации) и облегчает их отделение друг от друга и перевод во взвешенное состояние – в состояние золя.
4. Метод ультразвука заключается в дроблении вещества, находящегося в дисперсионной среде, под действием ультразвуковых волн (с частотой 105 – 106 Гц), этот метод находит широкое промышленное применение для получения лиозолей, суспензий и эмульсий.
|
|