
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Класифікація вуглеводнів.
|
|
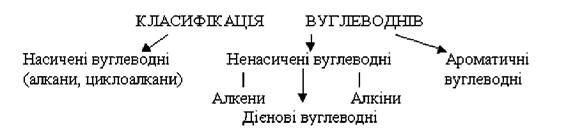
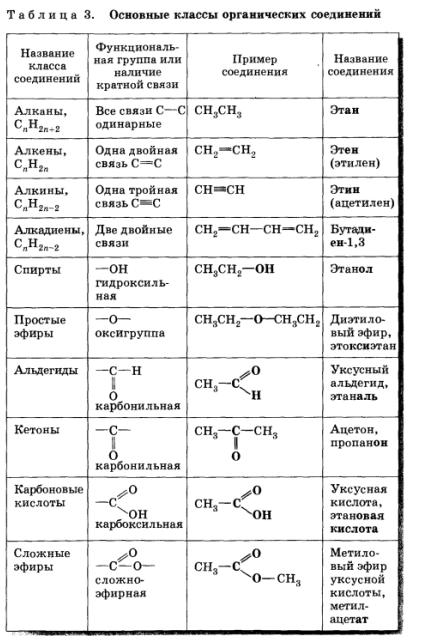
На прикладі насиченого вуглеводню пропану С3Н8 розглянемо, як скласти структурну формулу органічної речовини.
1. Зображуємо карбоновий кістяк. У даному випадку ланцюг складається з трьох атомів Карбону:
С—С—С
2. Карбон чотиривалентний, тому від кожного атома Карбону зображуємо недостатні риски таким чином, щоб поряд з кожним атомом було по чотири риски:
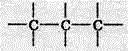
3. Дописуємо символи атомів Гідрогену:
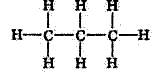
Часто структурні формули записують у скороченому вигляді, не зображуючи зв’язки С — Н. Скорочені структурні формули набагато компактніше, ніж розгорнуті:
СН3 - СН2 – СН3.
Структурні формули показують тільки послідовність з’єднання атомів, але не відображують просторової будови молекул, зокрема валентні кути. Відомо, наприклад, що кут між зв’язками С в пропані дорівнює 109, 5°. Проте структурна формула пропану виглядає так, начебто цей кут дорівнює 180°. Тому вірніше було б записувати структурну формулу пропану в менш зручному, але у більш правдивому вигляді:
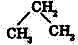
| Клас сполук | Загальна формула | Загальна формула з виокремленням функціональної групи |
| Алкани | СnН2n+2 | |
| Циклоалкани | СnН2n | |
| Алкени | СnН2n | |
| Алкадієни | СnН2n-2 | |
| Алкіни | СnН2n-2 | |
| Одноядерні арени (гомологічний ряд бензену) | СnН2n-6 | |
| Одноатомні насинені спирти | СnН2n+2О | СnН2n+1ОH |
| Багатоатомні спирти | СnН2n+2Оx | СnН2n+2-x(ОH)x |
| Альдегіди | СnН2nО | СnН2n+1CHO |
| Одноосновні карбонові кислоти | СnН2nО2 | СnН2n+1COOH |
| Естери | СnН2nО | СnН2n+1COOCnH2n+1 |
| Вуглеводи | Сn(Н2О)m | |
| Аміни первинні | СnН2n+3N | СnН2n+1NH2 |
| Амінокислоти | СnН2n+1NO | Н2NCnH2nCOOH |
Ізомери відрізняються один від одного будовою молекул, але ці відмінності можуть бути різними. Залежно від того, за якою ознакою відрізняється будова молекул ізомерів, розрізняють декілька видів ізомерії:
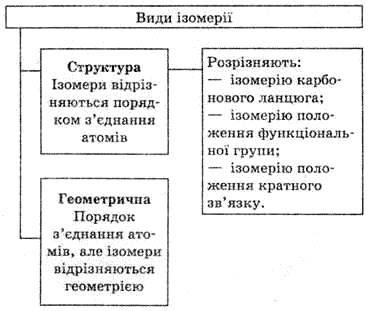
Усі різновиди ізомерії можна згрупувати у два типи: структурна і геометрична. Структурні ізомери відрізняються один від одного порядком з’єднання атомів, а у геометричних ізомерів порядок з’єднання однаковий, але геометрично молекули відрізняються одна від одної, наприклад:

Якщо два ізомери належать до одного класу органічних сполук, то вони можуть відрізнятися один від одного за різними ознаками. Найчастіше трапляється ізомерія карбонового ланцюга: в цьому випадку ізомери відрізняються порядком з’єднання атомів Карбону карбонового кістяка, як, наприклад: С4Н10
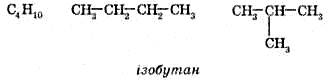
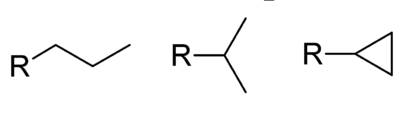
По порядку: 1-пропил, 2-изопропил, циклопропил
Нормальный или н-бутил: CH3-CH2-CH2-CH2- (систематическое название: бутил)
Вторичный бутил или втор-бутил: CH3-CH2-CH(CH3)- (систематическое название: 1-метилпропил)
Другой разветвлённый изомер бутана — изобутан, может быть замещённым по 3-ём терминальным атомам или по центральному
Изобутил: (CH3)2CH-CH2- (систематическое название: 2-метилпропил)
Третичный бутил, трет-бутил: (CH3)3C- (систематическое название: 1, 1-диметилэтил)
Багато сполук містять у своєму складі функціональні групи. Якщо карбоновий ланцюг має достатню довжину, то функціональна група може з’єднуватися з різними атомами Карбону в ланцюзі — це ізомерія положення функціональної групи:
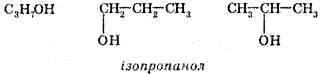
Якщо сполука з великим карбоновим ланцюгом також має кратні зв’язки (подвійні або потрійні), то такі зв’язки можуть бути утворені між різними атомами Карбону — це ізомерія положення кратного зв’язку:
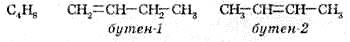
Структурні ізомери можуть належати не тільки до одного, але і до різних класів сполук. У такому випадку ізомерію називають міжкласовою. Так, розглянуті вже етанол і диметиловий етер є міжкласовими ізомерами: перша сполука належить до класу спиртів, а друга — до етерів. Також можуть існувати пари речовин, одна з яких є ненасиченим вуглеводнем, а друга — циклічним вуглеводнем:
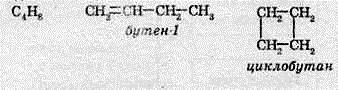
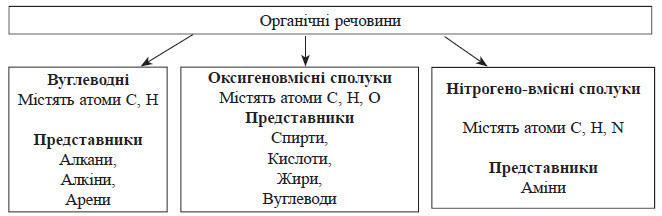
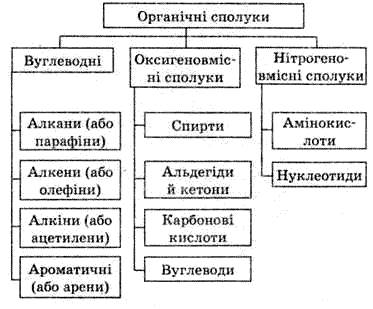
Всі органічні сполуки підрозділяються на три основні ряди, або класу: ациклічні, ізоциклічні і гетероциклічні. До першого класу (жирних, або аліфатичних) з'єднань відносять вуглеводні і їх похідні з незамкнутими ланцюгами: гомологічний ряд метанових вуглеводнів, званий також поруч насичених вуглеводнів, або алканов; гомологічні ряди ненасичених вуглеводнів — етилену (алкенов), ацетилену (алкінів), дієнов і ін. (див. Ациклічні з'єднання). До класу ізоциклічних (карбоциклічних) з'єднань відносять вуглеводні і їх похідні, в молекулах яких є цикли з атомів вуглецю: вуглеводні і їх похідні циклопарафінового, або поліметіленового, ряду, циклічні ненасичені сполуки (див. Аліциклічні з'єднання, Циклоалкани), а також ароматичні вуглеводні і їх похідні, що містять бензолові ядра (зокрема, і багатоядерні ароматичні з'єднання, наприклад, нафталін, антрацен). До класу гетероциклічних з'єднань відносять органічні речовини, в молекулах яких є цикли, що містять, окрім вуглецю, атоми Про, N, S, Р, As або ін. елементів.
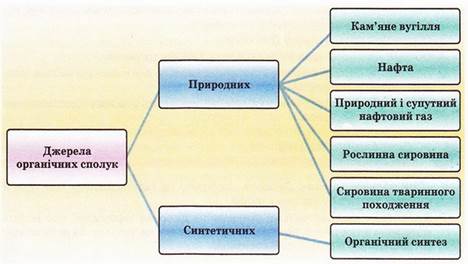
Від кожного вуглеводня утворений окремий генетичний ряд (див. Гомологічні ряди), представники якого формально виробляються шляхом заміни атома водню у вуглеводні тією або іншою функціональною групою, що визначає хімічні властивості з'єднання. Так, в генетичний ряд метану Ch 4 входять хлористий метил Ch 3 Cl, метиловий спирт Ch 3 ВІН, метиламін Ch 3 Nh 2, нітрометан Ch 3 No 2 і ін. Аналогічно представники генетичного ряду бензолу C 6 H 6 — хлорбензол C 6 H 5 Cl, фенол C 6 H 5 ВІН, анілін C 6 H 5 Nh 2, нітробензол C 6 H 5 No 2 і ін. Однойменно заміщені представники різних генетичних рядів складають гомологічні ряди похідних: галогенсодержащих з'єднань, спиртів, амінів, нітросполук і ін. Хімічні з зв'язки діляться на типи по принципу їх електронної будови.
|
|