
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Тема 3.3.Углеводороды
|
|
Основные понятия и термины по теме
Углеводороды. Предельные углеводороды. Непредельные углеводороды. Алкены. Алкины. Алкадиены. Ароматические соединения. связь, двойная связь, тройная связь.
План изучения темы
- Основные определения.
- Классификация углеводородов
- Предельные углеводороды.
- Строение, номенклатура, свойства, получение.
- Реакция замещения, горения, разложения.
- Непредельные углеводороды. Номенклатура, строение.
- Химические свойства непредельных углеводородов.
- Реакция полимеризации, присоединения.
- Применение углеводородов в органическом синтезе.
- Природные источники углеводородов. Нефть Татарстана.
Краткое изложение теоретических вопросов:
Углеводоро́ ды — органические соединения, состоящие исключительно из атомов углерода и водорода. Углеводороды считаются базовыми соединениями органической химии, все остальные органические соединения рассматривают как их производные.Поскольку углерод имеет четыре валентных электрона, а водород — один, простейший углеводород — метан (CH4).
При систематизации углеводородов принимают во внимание строение углеродного скелета и тип связей, соединяющих атомы углерода. В зависимости от топологии строения углеродного скелета углеводороды подразделяют на ациклические и карбоциклические. В зависимости от кратности углерод-углеродных связей углеводороды подразделяют на предельные (алканы) и непредельные (алкены, алкины, диены). Циклические углеводороды разделяют на алициклические и ароматические.
| Ациклические (с открытой цепью) | ||||
| предельные | непредельные | |||
| с одинарной связью | с двойной связью | с тройной связью | с двумя двойными связями | |
| ряд метана(алканы) | ряд этилена(алкены) | ряд ацетилена(алкины) | ряд диеновых углеводородов |
Предельные углеводороды
Алканы – основные представители органических веществ среди полезных ископаемых они составляет невосполнимую часть природных ресурсов. Алканы входят в состав природного газа и нефти. Современные представления о строении вещества не сводятся только к установлению порядка соединений атомов, но также включают рассмотрение пространственного строения молекул и электронной природы химических связей.
СН4 – молекулярная формула (качественный, количественный состав);
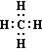 – электронная формула (ковалентная полярная связь);
– электронная формула (ковалентная полярная связь);
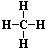 – структурная формула (порядок соединения атомов в молекуле).
– структурная формула (порядок соединения атомов в молекуле).
Но данные формулы не отражают истинного строения молекул метана. Молекула метана не имеет плоского строения, как можно представить на основании структурной формулы.
Молекула метана в действительности имеет форму тетраэдра. Тетраэдр – это пирамида, в основании которой лежит равносторонний треугольник. В центре тетраэдра находится атом углерода, а все его четыре валентности направлены к вершинам тетраэдра. Физическими методами исследования установлено, что валентные углы равны 109о28'.
Электронное строение атома углерода и молекулы метана.
С 1S2 2S2 2P2 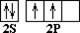 ––> C * 1S2 2S1 2P3
––> C * 1S2 2S1 2P3 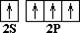
(основное состояние) (возбужденное состояние)
Так как на втором энергетическом уровне Р-подуровне есть свободная орбиталь, то на неё переходит один из 2S2-электронов. В результате этого атом углерода в возбуждённом состоянии имеет четыре неспаренных электрона, т.е. становится четырёхвалентным.

(негибридные электронные облака) (гибридные электронные облака)
Облака всех четырёх валентных электронов атома углерода выравниваются, становятся одинаковыми. При этом они принимают форму вытянутых в направлении к вершинам тетраэдра восьмёрок.
Явление, при котором происходит смешение и выравнивание по форме и энергии электронных облаков, называется гибридизацией.
Так как гибридизации подвергаются один S и три Р-электрона, то такое состояние называется SP3-гибридизацией.
Несимметричное распределение электронной плотности означает, что вероятность нахождения электрона по одну сторону от ядра больше, чем по другую. Гибридные электронные облака вытянуты в пространстве под углом 109о28' к вершинам воображаемого тетраэдра, и в этом направлении они перекрываются с электронными облаками атомов водорода.
Итак, молекула метана имеет тетраэдрическое строение, что обусловлено SP3-гибридизацией атома углерода, тетраэдрическим направлением четырёх гибридных электронных облаков атома углерода.
Сравнивая масштабную и шаростержневую модели молекул метана, можно отметить, что шаростержневая модель, появившаяся до возникновения электронной теории, более наглядно рассматривает строение молекулы метана.
Работа с таблицами “Строение метана” и “Строение этана и бутана”
Для гомологов метана характерно:
тетраэдрическое строение атома углерода (SP3-гибридизация);
одинаковое значение всех валентных углов;
наличие С – С и С – Н химических связей.
Анализ химических связей алканов
При рассмотрении второго вопроса плана обращается внимание на характер С – С и С – Н связей, являющихся ковалентными по характеру образования. Углерод-углеродные и углерод-водородные связи в алканах относятся к (сигма) связям.
(сигма) связь – это химическая связь, при образовании которой перекрывание электронных облаков происходит по прямой, соединяющей ядра атомов.Эти связи разнообразны.
Номенклатура углеводородов
Выделяют в структурной формуле наиболее длинную цепь атомов углерода и нумеруют эти атомы, начиная с того к которому ближе разветвление.1 2 3 4 5СН3 - СН - СН2 - СН2 - СН3 СН31 2 3 4СН3 – СН – СН – СН3 СН3СН3
Когда радикалов несколько и они равноудалены от концов главной цепи, то нумерацию начинают с того края, к которому ближе расположен простейший радикал.3. В названии вещества цифрой указывают, при каком атоме углерода находится радикал и называют его (начиная с простейшего). Если радикалы повторяются, то номер повторяют по числу этого радикала, а перед названием радикала приписывают приставку от греческого числительного («ди»-2, «три»-3, «тетра»-4 и т.д.)а) 2 - метил…б) 2, 3 – диметил…
Если радикалов несколько, то цифрами указывают каждого из них.5. Завершают название алкана по числу атомов углерода в нумерованной цепи.а) 2 – метилпентанб) 2, 3 –диметилбутан
|
|