
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Стволовые клетки и их использование
|
|
Последним направлением научных исследований является использование уникального лечебного и омолаживающего эффекта стволовых клеток (СК). Открытие их стоит в одном ряду с такими великими достижениями человечества, как открытие двуспиральной цепочки ДНК или расшифровка генома человека. ООН назвала 1999 год «годом стволовой клетки», а в 2007 году Нобелевская премия по физиологии и медицине была присуждена трем ученым: американцам Марио Капекки, Оливеру Смитису и британцу Мартину Эвансу. Они получили награду за достижения в области ген-направленного мутагенеза у мышей с использованием эмбриональных стволовых клеток.
Как говорится в пресс-релизе присуждающего премию Каролинского института (Швеция), Капекки, Эванс и Смитис сделали ряд основополагающих открытий, позволивших разработать методы избирательного подавления единичных генов, которые могут применяться для лечения рака, диабета, сердечно-сосудистых и нейродегенеративных заболеваний.
Однако до сих пор остаётся много неразрешённых вопросов и спорных мнений по поводу их применения. Данная глава ставит целью – раскрыть технологические особенности получения, криоконсервации и использования СК в биотехнологии. Осведомлённость и информированность в этом вопросе позволят студентам зооинженерного факультета сформировать правильное мнение о перспективах развития регенеративной клеточной биотехнологии, сулящей людям излечение от многих тяжёлых болезней.
Стволовая клетка – популяция клеток-предшественников, обладающих высоким пролиферативным потенциалом и способностью к дифференцировке в клетки обычно нескольких линий: в организме – в любые клетки данного органа, в эмбрионе – в любую клетку организма.
Преимущество СК в том, что они могут превращаться в один из 350 возможных типов клеток тканей. Это «стержень жизни», источник, из которого образуются все остальные клетки организма. При этом они не входят, в какую - либо тканевую структуру и сами непосредственно не выполняют каких - либо функций, а хранятся в состоянии покоя в специальных нишах до востребования.
Физиологические особенности развития эмбриональных СК. Стволовые клетки, т. е. бластомеры, находятся внутри зародыша и имеют диплоидный набор хромосом. Они образуются после слияния ядер двух гамет - яйцеклетки и сперматозоида. В результате дробления бластомеров образуется морула или бластоциста (рис. 6.1 а и 6.1 б).


А б
Рис. 6.1. Стадии развития эмбрионов
а - нормально развитая морула; б – нормально развитая бластоциста
Нормально развитые стволовые клетки заключены в зону пеллюцида (прозрачную оболочку) зародышей на ранней стадии развития, имеющих форму правильной сферы. Удваивание числа стволовых клеток (бластомеров) в них происходит через каждые 24 часа. Различия в степени дробления в ранний период их развития могут быть обусловлены растянутостью сроков овуляции фолликула в яичниках и выходом зрелых яйцеклеток в воронку яйцеводов. Бластомеры морул не обязательно должны иметь одинаковую величину, что зависит от возможной асинхронности процесса их деления (6.1а). На 7-8-й день после осеменения, например, коров-доноров в промывной жидкости обнаруживаются нормально развитые бластоцисты (рис. 6.1б). Они имеют толщину прозрачной оболочки, примерно, 12 мкм, число бластомеров может быть от 80 до 120, просматривается бластополость. Поверхность клеточной массы – гладкая, равномерная, что указывает на наличие соединительного комплекса между клетками трофобласта, перивителлиновое пространство маленькое. Стволовая клетка содержит не только информацию об организме, но и схему ее последовательного развития. В ходе эмбриогенеза оплодотворенная яйцеклетка делится и дает начало клеткам, не имеющим других функций, кроме передачи генетического материала в следующие клеточные поколения. Это эмбриональные стволовые клетки (ЭСК), геном которых находится в «нулевой точке»; механизмы, определяющие специализацию, еще не включены и из них потенциально могут развиться любые клетки.
Схема развития организма представлена на рис.6.2.

Рис. 6.2. Схема развития организма из СК
Во взрослом организме СК находятся, в основном, в костном мозге (стромальные) и, в очень небольших количествах, во всех органах и тканях. Они обеспечивают восстановление поврежденных участков органов и тканей. Высокодифференцированные клетки (кардиомиоциты, нейроны) практически не делятся, в то время как менее дифференцированные клетки – фибробласты, гепатоциты частично сохраняют способность к размножению и при определенных условиях делятся и увеличивают свое число. Общей закономерностью является то, что если клетка вышла на этап дифференцировки, то количество делений, которое она может пройти, ограничено. Так, например, для фибробласта лимит делений составляет 50, для стволовой клетки крови – 100. Описанное явление имеет большое биологическое значение: в случае, если произошла поломка в геноме клетки, мутация будет растиражирована в ограниченном количестве и не сыграет большой роли для организма в целом. Запас СК взрослого организма очень невелик. Поэтому случается так, что обновить утраченные клетки организм самостоятельно уже не в состоянии: или очаг поражения слишком велик, или организм ослаблен, или возраст уже преклонный. В настоящее время уже имеется возможность излечения больного от цирроза, инсульта, паралича, диабета, ряда заболеваний нервной системы. Уже сегодня ученые умеют направлять стволовые клетки " по нужному пути". Достижения в этой области биотехнологии клетки делают возможности терапевтического использования стволовых клеток практически безграничными. В процессе проявления своих наследственно - функциональных возможностей стволовые клетки имеют свою иерархию незрелых клеток живых организмов (рис. 6.3).
Стволовые клетки — это иерархия незрелых клеток живых организмов, каждая из которых способна дифференцироваться (получать специализацию). Корнем этой иерархии является тотипотентная зигота (морула). Первые несколько делений зиготы сохраняют тотипотентность и при потере целостности (разделении на половины) зародыша это приводит к появлению монозиготных близнецов.

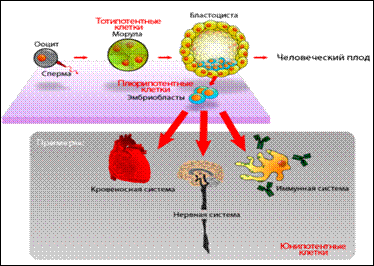
Рис. 6. 3. Иерархия стволовых клеток Рис. 6. 4. Стромальные СК
К ветвям иерархии относятся плюрипотентные (омнипотентные) и мультипотентные (бластные) СК. Листьями (конечными элементами) иерархии являются зрелые юнипотентные клетки тканей организма.
Нишами СК называются места в ткани, где постоянно залегают стволовые клетки, делящиеся по мере надобности для дальнейшей дифференциации.
Когда происходит созревание СК, то они проходят несколько стадий. В результате, в организме имеется ряд популяций стволовых клеток различной степени зрелости. В нормальном состоянии, чем более зрелой является клетка, тем меньше вероятность того, что она сможет превратиться в клетку другого типа. Такое превращение возможно благодаря феномену трансдифференцировки клеток (англ. Transdifferentiation).
В различных органах и тканях взрослого организма существуют частично созревшие СК, готовые быстро дозреть и превратиться в клетки нужного типа. Они называются бластными клетками. Например, частично созревшие клетки мозга – это нейробласты, кости – остеобласты и так далее. Дифференцировку могут запускать как внутренние факторы, так и внешние. Любая клетка реагирует на внешние раздражители, т.е. на специальные сигналы вещества цитокина. Например, есть сигнал цитокина, служащий признаком перенаселённости (клеток становится очень много), то происходит сдерживание дальнейшего их деления. В ответ на эти сигналы клетка может регулировать экспрессию генов.
Понятие «стволовые клетки» впервые ввёл в 1908 году русский гематолог из Санкт-Петербурга А. Максимов, который при изучении процесса кроветворения пришёл к выводу об их существовании. Однако не были известны их отличительные свойства. Сначала полагали, что во взрослом организме таких клеток нет, и существуют они лишь в самом раннем периоде эмбрионального развития. Значительный объём исследований стволовых клеток проведён биологами И. Чертковым и А. Фризенштейном в России, в 60-х годах 20-го века. Именно они впервые обнаружили стромальные стволовые клетки (ССК) в мезенхиме (строме) «взрослого костного мозга» и доказали их уникальную регенерационную способность. В дальнейшем их стали называть стромальными клетками.
Открытие это осталось практически незамеченным до 1981 года, когда американскому учёному М. Эвансу удалось выделить животную стволовую эмбриональную клетку из зародыша мыши. После этого усилия учёных были направлены на получение эмбриональной стволовой клетки из человеческого зародыша. Бум в исследованиях в этой области начался с 1998 года, когда американскими исследователями Дж. Томпсоном и Дж. Беккером были открыты эмбриональные стволовые клетки человека и доказана их способность дифференцироваться практически в любые типы клеток человеческого организма. Однако применение эмбриональных СК во всём мире, включая Беларусь, в настоящее время временно запрещено, поскольку не доказана их безопасность в плане онкогенности. Стромальные же (костные) стволовые клетки, напротив, находят всё большее применение в различных направлениях биотехнологии.
Отличие эмбриональных и стромальных СК заключается в том, что эмбриональные могут быть получены на ранней стадии развития эмбриона человека или животного (из внутренней массы бластомеров морулы или бластоцисты), а вторые встречаются в течение всей их жизни во всех его органах и тканях, но больше всего в костном мозге. Эмбриональные СК значительно активнее стромальных, обладают более высокой способностью к размножению, большим потенциалом дифференцировки.
Помимо стромальных СК выделяют ещё гемопоэтические клетки – предшественники клеток крови. Они встречаются в кровеносном русле в отличие от стромальных, которые в крови циркулируют только при серьёзных поражениях органов и систем организма. Отдельно можно выделить фетальные стволовые клетки, которые получают из абортивного материала. В большинстве стран применение этих клеток также запрещено по морально – этическим соображениям.
СК можно выделять и выращивать в питательной среде свойственной для данной ткани органа. При этом образуются шарообразные клеточные ассоциаты: скопление их называют эмбриоидными телами, а скопление нейральных клеток – нейросферами. Способность давать множество разнообразных клеточных типов (плюрипотентность) делает стволовые клетки важнейшим восстановительным резервом в организме, который используется для замещения удаленных в процессе операции пораженных участков органов искусственно выращенными.
Особое удивление биологов вызвало присутствие СК в центральной нервной системе. Как известно, сами нервные клетки утрачивают способность к размножению уже на самой ранней стадии нейральной дифференцировки (стадии нейробласта). СК в ответ на различные поражения нервной ткани начинают делиться с последующей дифференцировкой в нервные и глиальные клетки. Изолированные нейральные СК могут превращаться и в другие производные.
СК встречаются во всех органах и тканях, а не только в костном мозге. Костный мозг является основным депо гемопоэтических СК (рис 6.5). Он содержит и стромальные клетки, хотя содержание их в жире, например, заметно большее, чем в костном мозге.
Неправильное мнение некоторых о том, что нигде, кроме костного мозга, СК нет, сложилось по причине, что первыми они были обнаружены именно в костном мозге. Поэтому долгое время считалось, что именно костный мозг содержит едва ли не все СК организма. Позже их обнаружили в жире, коже, мышцах, печени, лёгких, сетчатке глаза, практически во всех органах и тканях организма. Стромальные стволовые клетки, полученные из различных тканей, практически ничем не отличаются. Отличие заключается только в содержании определённых прогениторных клеток, т.е. клеток находящихся на пути к дифференцировке; у каждой ткани они свои.

Рис. 6.5. Костный мозг, как депо гемопоэтических СК
В сформировавшемся организме человека имеется примерно 1012 клеток трёхсот различных типов. Они требуют постепенного замещения по мере их старения и отмирания. Эту восстановительную функцию выполняют стволовые клетки, заполняющие определённые ниши во всех тканях и органах. Например, в коже они располагаются в дермальном слое.
Механизм процесса замещения клеток. На поверхности СК располагаются специфические рецепторы, чувствительные к различным веществам (цитокинам), выделяющимся в местах повреждений. Уникальность и универсальность механизма замещения заключается в том, что СК сами находят дорогу к местам повреждений в организме. С годами количество СК снижается, потенциал их также угасает. Тем не менее, пока жив человек, живы его стволовые клетки, их можно выделить и вырастить и у очень пожилых людей. Конечно, у здоровых и молодых людей стволовых клеток, как правило, больше, но тенденция эта не абсолютна. Состояние СК зависит от состояния здоровья, образа жизни, а не только от возраста.
Применение СК для лечения и профилактики широкого спектра заболеваний привело к активному развитию клеточных технологий. В настоящее время в развитых странах созданы и функционируют многочисленные медицинские клиники различной специализации, которые используют стволовые клетки.
Оплодотворенная яйцеклетка тотипотентна – она обладает неограниченным потенциалом в том смысле, что ее одной достаточно для формирования и развития нормального плода при соответствующих условиях. В первые часы после оплодотворения она делится с образованием идентичных тотипотентных клеток (рис. 6.6), и любая из них, будучи имплантирована в матку женщины, способна дать начало развитию плода.

Рис. 6.6. Образование идентичных тотипотентных клеток
Примерно через четверо суток после оплодотворения, когда проходит несколько циклов клеточного деления, тотипотентные клетки начинают специализироваться с образованием сферической структуры, называемой бластоцистой. У бластоцисты есть наружный слой и внутренняя полость, где образуется внутренняя клеточная масса. Из наружного слоя развивается плацента и другие поддерживающие структуры, необходимые для формирования плода, а из внутренней клеточной массы – практически все органы и ткани самого плода. Клетки внутренней клеточной массы плюрипотентны – их наличие является необходимым, но ещё не достаточным условием формирования плода. Если их сразу имплантировать в матку женщины, то беременность не наступит.
Плюрипотентные клетки подвергаются дальнейшей специализации с образованием стволовых клеток, которые дают начало уже полностью специализированным клеткам, обладающими специфическими функциями. Так, из кроветворных (гемопоэтических) стволовых клеток развиваются эритроциты, лейкоциты и тромбоциты, а из стволовых клеток кожи – различные типы клеток этой ткани (рис. 6.7).

Рис. 6.7. Дифференцировка плюрипотентных клеток
Так, гемопоэтические СК, находящиеся в основном в костном мозге, а также в небольшом количестве циркулирующие в крови, ответственны за постоянное образование новых клеток крови взамен разрушенных, и этот процесс продолжается всю жизнь.
В настоящее время линии плюрипотентных клеток человека получают из трёх источников с помощью методов, отработанных на животных моделях.
а) Плюрипотентные клетки выделяют непосредственно из внутренней клеточной массы эмбриона человека на стадии бластоцисты. Сам эмбриональный материал получают в больших количествах в клинической практике для осуществления экстракорпорального оплодотворения, всякий раз письменное спрашивая разрешение, на его использование, у обоих доноров. Клетки внутренней клеточной эмбриональной массы культивируют и получают линию плюрипотентных клеток (рис. 6.8).

Рис. 6.8. Получение культивированных плюрипотентных клеток
б) Во втором случае выделяют плюрипотентные клетки из ткани плода. Разрешение на это даётся обоими супругами уже после того, как они сами приняли решение прервать беременность. Клетки отбирают из той области плода, которая должна была развиться в яичники или семенники.
Несмотря на то, что плюрипотентные клетки в двух указанных случаях происходят из разных источников, полученные клеточные линии являются идентичными.
в) Третьим способом получения плюрипотентных клеток может стать метод, основанный на переносе в энуклеированную (лишенную ядра) яйцеклетку ядра соматической клетки. Соответствующие опыты уже проведены на животных. Сама яйцеклетка с новым ядром и ее непосредственные «потомки» способны при соответствующих условиях развиться в полноценный организм, т.е. являются тотипотентными. Из них формируется бластоциста, которая и служит источником плюрипотентных клеток (рис. 6.9).

Рис. 6.9. Процесс формирования плюрипотентной клетки
Возможное применение плюрипотентных клеток. Изолированные плюрипотентные клетки человека – очень ценный материал для исследователей и клиницистов (рис. 6.10). Эксперименты с их использованием могут помочь разобраться в сложнейших процессах развития человеческого организма, и, прежде всего в том, что именно влияет на принятие клеткой решения о переходе от стадии роста и деления к стадии дифференцировки.

Рис. 6. 10. Области применения плюрипотентных СК
Известно, что ключевым моментом здесь является «включение» и «выключение» специфических генов, но мы мало что знаем и о самих этих генах, и о том, какие события предшествуют их переключению. Разобравшись в функционировании клетки в норме, мы сумеем понять, какие сбои в ее работе приводят к фатальным для организма последствиям.
Выделение плюрипотентных клеток человека открывает новые возможности перед исследователями, занимающимися поисками новых лекарственных веществ и их тестированием. Разнообразные клеточные линии (например, линии раковых клеток) используются в этих целях уже сейчас, а культура плюрипотентных клеток позволяет проводить тестирование сразу на нескольких типах клеток. Это не заменяет тестирование на уровне целого организма, но значительно облегчает поиск новых лекарственных веществ.
Одно из самых впечатляющих применений плюрипотентных клеток человека – это так называемая «клеточная терапия». Многие заболевания человека обусловливаются нарушением функционирования клеток или целых органов, и сегодня для устранения дефекта в таких случаях используется метод трансплантации. К сожалению, нередко повреждения носят множественный характер, и заменить все затронутые ими органы не представляется возможным. Плюрипотентные СК, стимулированные к дифференцировке с образованием строго специализированных клеток, могут служить возобновляемым источником не затронутых поражением клеток, замещающих выбывшие из строя дефектные клетки. Это открывает широкие возможности для лечения самых разных заболеваний человека, включая такие серьезные, как болезнь Паркинсона, болезнь Альцгеймера, сердечно-сосудистые заболевания, ревматоидный артрит, диабет и др.
Еще более впечатляющее применение стволовых клеток человека – генная терапия ex vivo. В этом случае в организм больного можно инфузировать не обычные СК, а генетически модифицированные, которыми и замещают дефектные клетки. СК можно получать от самого пациента или от совместимых с ним доноров. Следует отметить, однако, что генная терапия ex vivo с применением стволовых клеток человека делает лишь первые шаги. Гораздо более реальным является использование модифицированных эмбриональных СК для создания трансгенных животных.
Соответствующие эксперименты уже широко проводятся на мышах (рис. 6.11).

Рис. 6.11. Использование модифицированных эмбриональных
|
|