
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Цель работы: определение точной концентрации приготовленного раствора гидроксида натрия титрованием его 0,1 М раствором серной кислоты.
|
|
КРАТКИЕ ТЕОРЕТИЧЕСКИЕ ОСНОВЫ РАБОТЫ
Раствором называется
____________________________________________________________________________________________________________________________________
Концентрация раствора определяется
____________________________________________________________________________________________________________________________________
Способы выражения концентрации растворов:
1._________________________________________________________________2._________________________________________________________________3._________________________________________________________________4._________________________________________________________________
5._________________________________________________________________
Титрование – это
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Титрованный раствор – это
__________________________________________________________________
Опыт 1. Приготовление раствора гидроксида натрия заданной нормальной концентрации.
Нормальная концентрация Сн определяется
______________________________________________________________________________________________________________________________________________________________________________________________________и измеряется_______________________________________________________
Молярная масса эквивалента МЭ сложного вещества рассчитывается по формуле
__________________________________________________________________и измеряется_______________________________________________________
МЭ гидроксида натрия = _____________________________________________
Масса NaOH, необходимая для приготовления 0, 5 л 0, 05 н раствора
m = __________________________________________________________________
Опыт 2. Определение точной концентрации приготовленного раствора титрованием его серной кислотой известной концентрации.
Используемая при титровании реакция:
__________________________________________________________________
Точка эквивалентности
____________________________________________________________________________________________________________________________________устанавливается с помощью
______________________________________________________________________________________________________________________________________________________________________________________________________
Метиловый оранжевый в щелочном растворе окрашен ___________________
в кислом растворе окрашен __________________________________________
Таблица 3.1
| № п/п | Объем щелочи V1, мл | Объем кислоты V2, мл |
Cреднее значение объема кислоты = 


По формуле 
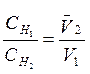 , где
, где 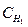 – концентрация щелочи,
– концентрация щелочи, 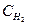 - концентрация кислоты, рассчитайте нормальную концентрацию щелочи.
- концентрация кислоты, рассчитайте нормальную концентрацию щелочи.
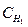 (NaOH) =
(NaOH) =
Вывод:
____________________________________________________________________________________________________________________________________
|
|