
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Протолитические равновесия
|
|
Основные формулы, используемые для расчетов в аналитической химии
Использование законов термодинамики и кинетики для описания реальных гомогенных и гетерогенных систем
- Формула для расчета ионной силы раствора
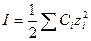
- Математическая запись предельного закона Дебая-Хюккеля (I< 0, 01)
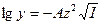 ,
,
где А – коэффициент, зависящий от температуры и диэлектрической проницаемости растворителя (для разбавленных водных растворов при Т=298К А=0, 509).
3. Расширенное уравнение Дебая-Хюккеля (при ионных силах порядка 0, 01 - 0, 1 )
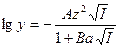 ,
,
где В приблизительно 0, 328 при Т=298К, а – эмпирическая константа, характеризующая размер ионной атмосферы.
4. Уравнение Дэвиса (ионная сила до 1)
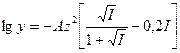
- Формулы для расчета констант равновесия
термодинамической (К0) – 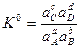
концентрационной реальной (К) – 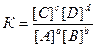
концентрационной условной (К ׳ ) – 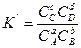
- Формулы, связывающие различные константы между собой:
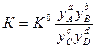
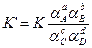
Протолитические равновесия
|
|