
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Катализдік процесстердің жіктелуі
|
|
Азақ стан Республикасы Денсаулық сақ тау министрлігі
Оң тү стік Қ азақ стан Мемлекеттік Фармацевтика Академиясы
Фармацевтикалық жә не токсикологиялық кафедрасы
СӨ Ж
Тақ ырыбы: Тасымалдағ ыштар, белсендіргіштер.Контакт аппараттар.Катализдік процесстерді жіктеу.Ә ртекті катализдік процесстердің ең жә й жү ретін сатысын анық тау.
Орындағ ан: Мусабекова Ж.
Тобы: 301 «А» ТФП
Абылдағ ан: Қ ыдыралиева А.
Шымкент 2015
Жоспар
IКіріспе
IIНегізгі бө лім
a)Тасымалдағ ыштар
ә)Белсендіргіштер немесе промоторлар
б)Катализдік процесстерді жіктеу
с)Ә ртекті катализдік процесстердің ең жә й жү ретін сатысын анық тау.
д)Ә р текті катализдік процесстер
е) Катализ жә не катализатор
Пайдаланғ ан ә дебиеттер
Тасымалдағ ыштар -температурағ а тө зімді, инертті, кеуекті заттар.Тасымалдағ ыштар катализатор қ асиетін жақ сартады жә не арзандатады.Тасымалдағ штар ретінде қ олданылатын кеуекті заттар-пемза, ә к, силикагель жә не т.б.
Белсендіргіштер немесе промоторлар -ө здері активтілік кө рсетпейтін, бірақ негізгі катализаторлардың активтілігін арттыратын заттар.Мысалы, сілтілік металдар оксидтері темір катализаторларының, ванадий катализаторларының активтілігін арттырады яғ ни жоғ арлатады.
Катализаторлар-реакцияның жылдамдығ ын ө згертіп, бірақ реакция нә тижесінде ө здері химиялық ө згермей қ алатын заттар.Катализатор қ атысуымен болатын процесстер жаратылыстада, ө неркә сіптеде ө те кө п.Қ азіргі заманның ө неркә сібінде, ә сіресе химиялық ө неркә сіпте, катализаторлар ерекше орын алуда.
Ә рбір реакцияғ а ө зіне тә н, лайық катализатор болады.Кей жағ дайда тү рлі катализатор қ олдану арқ ылы, бір заттан ә р тү рлі ө німдер алуғ а болады.
Al2 O3 C2H4+H2O (этилен)
C2H5OH H3PO4 C2H5OCH+H2O (диэтил эфирі)
MgO; K2O CH4CHO+H2 (сірке альдегиді)
Реакцияғ а катализатор қ атысқ анда ондағ ы актив молекулалар саны ө седі, содан барып реакция жылдамдайды.Екінші жағ ынан катализатор қ атысқ анда активтендіру энергиясы кемиді.
Ө ндірісте кө бінесе қ олданылатын катализатор кү рделі қ оспадан қ ұ ралады, осы себептен оларды контакт массасы деп атайды.Контакт масса қ ұ рамында: катализатор (активтік фаза), тасымалдағ ыш жә не активатор болады.
Катализдік процесстердің жіктелуі
Катализдік процесстерді жіктеу келесі белгілері бойынша жү зеге асырылады:
1) процесске қ атысатын бастапқ ы заттардың, ө німдердің жә не қ олданылатын катализаторлардың агрегаттық кү йі бойынша: біртекті жә не ә ртекті катализ.
Біртекті катализ газды немесе сұ йық фазада жү реді.Біртекті катализдің механизімі бойынша реагенттер мен катализаторлар тұ рақ сыз аралық қ осылыстар тү зеді, олар ыдырағ аннан кейін реакция ө німі тү зіледі, ал катализатор бастапқ ы қ алпына келеді.
Біртекті катализатордың жылдамдығ ына ә рекеттесуші заттар мен катализатордың концентрациясы, температура, қ ысым жә не араластыру дә режесі ә сер етеді.Олардың ә сері біртекті процестердің жалпы кинетикалық заң дылық тарына сә йкесті болады.Бірақ біртекті катализдің негізгі кемшілігі реакциялық қ оспадан катализаторды бө ліп алу болғ андық тан, ол ө неркә сіптік жағ дайда сирек қ олданылады. Ә р текті катализ ө неркә сіпте кең інен қ олданылады.Кө бінесе ө ндірістік ә ртекті катализді процесстер қ атты катализаторлардың қ олданылуымен газды заттардың арасында жү ретін реакцияларғ а негізделген.
2) автокатализді процесстер -бұ л процесстерде жартылай немесе соң ғ ы ө німдердің біреуі катализатор ретінде қ олданылады.Мысалы қ опарғ ыш заттардың кейбір ыдырау реакцияларын, жану, полимеризация жә не т.б.реакцияларды келтіруге болады.
3) микрогетерогенді катализ дегеніміз біртекті катализдің ә ртекті катализге ауысу кезіндегі катализ.
4) катализаторлардың ә сері бойынша:
а) оң катализ -катализатор негізгі химиялық реакцияның жылдамдығ ын жоғ арылату ү шін қ олданылады.
ә) теріс катализ -катализаторлар жанама реакцияларының жылдамдығ ын тө мендету ү шін қ олданылады.Жанама реакциялардың жылдамдығ ын тө мендететін катализаторлар ингибиторлар деп аталады.Мысалы, сақ тау барысында сұ йық отындарды тотығ удан қ орғ ау ү шін олардың қ ұ рамына ингибиторлар қ осады.
б)процесстердің жылдамдығ ына ә сер етпейтін, біраұ оның температурасын тө мендететін катализаторларды қ олдану.Мысалы фосфордың жану процесін келтіруге болады: оттегінің артық мө лшерін қ олдану процестің жылдамдығ ын 3500 С-ден шамамен 1700 С-ге дейін тө мендетеді.
Ө ндірісте қ олданылатын катализаторлар газ, сұ йық жә не қ атты кү йде болады.Мысал ретінде, газды катализаторларғ а кү кірт қ ышқ ылын нитрозалық ә діспен алуда қ олданылатын азот оксидтері, сұ йық қ а-органикалық синтезде қ олданылатын кү кірт жә не фосфор қ ышқ ылдарын немесе аммиак суын келтіруге болады.Ө ндірістік жағ дайда қ атты катализаторлар ө те кө п қ олданылады.Оларғ а металдар, олардың оксидтері мен тұ здары жатады.Мысалы, платина, темір, темір оксиді, ванадий оксиді жә не т.б.
Катализатордың жұ мыс температурасы-катализатордың ә сер ету температурасының ең тө мен мә ні.
Ө ндірістік жағ дайда жұ мыс температурасы тө мен катализаторларды қ олдану тиімді, себебі бұ л жағ дайда реакциялық қ оспаны қ ыздыруғ а шығ ындалатын энергияның мө лшері азаяды.Мысалы, кү кірт диоксидін тотық тыру ү шін жұ мыс температурасы 550˚ темір оксидті (Fe2O3) немесе 440˚ ванадий оксиді (V2 O5 ) катализаторлар қ олданылуғ а болады.Ванадий окиді катализаторларды қ олдану тиімді жә не тотығ у дә режесі шамамен 99% қ ұ райды, ал темір оксиді катализатор қ олданғ ан кезде тотығ у дә режесі шамамен 75% қ ұ райды.
Ә ртекті катализдік процесстердің ең жә й жү ретін сатысын анық тау.
Ә ртекті процестің қ арқ ындылығ ын жоғ арылату ү шін оның анық таушы сатысын білу ө те маң ызды.Процестің анық таушы сатысын тә жірибе жү зінде ә рекеттесуші заттардың айналдыру дә режесінің (Хк) немесе процестің жылдамдығ ының (ώ) ә рекеттесу уақ ытына, бө лшектердің ө лшемдеріне немесе температурағ а тә уелділігін тауып анық тауғ а болады.3.11 суретте айналдыру дә режесінің берілген ө лшемдегі бө лшектің салыстырмалы ә рекеттесу уақ ытына теориялық тә уелділігі кө рсетілген.Тә жірибелік мә ліметтер бойынша алынғ ан қ исық тарды 3.11 суретте кө рсетілген теориялық қ исық тармен салыстыру арқ ылы процестің анық таушы сатысын анық тауғ а болады.
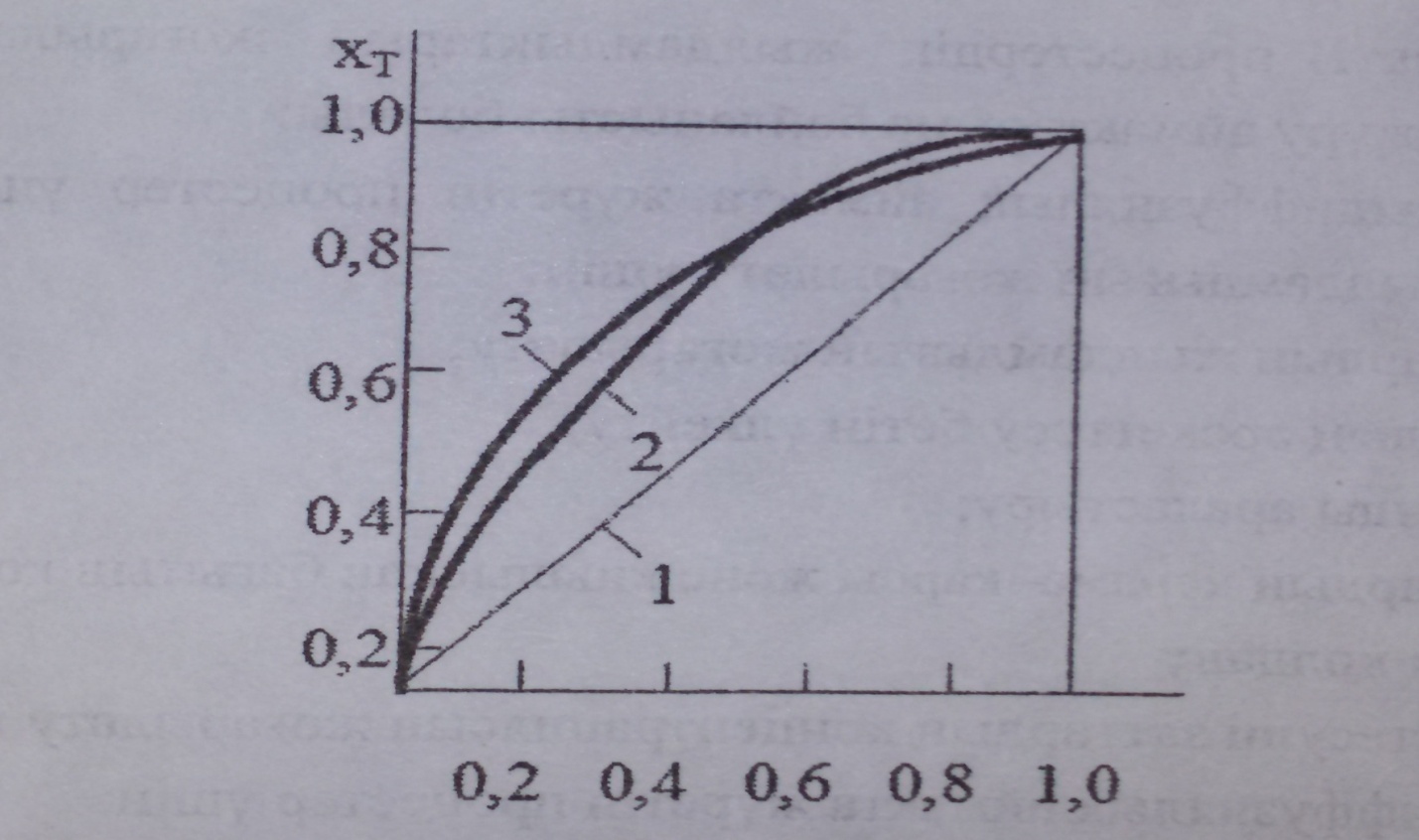
Анық таушы саты: 1-сыртқ ы диффузия; 2-ішкі диффузия; 3-химиялық реакция.3.11 сурет-Айналдыру дә режесінің Хт салыстырмалы ә рекеттесу уақ ытына тә уелділігі.

Ә р текті- катализдік процестер
Химиялық технологияда катализдік процестер кең інен қ олданылады. Катализаторлардың қ олданылуымен химиялық реакциялардың жылдамдығ ын мың дағ ан жә не де миллиондағ ан есе ү детуге болады.Химиялық ө ндірістің процесстерінің шамамен 70%-ң қ ұ рамына катализдік сатылар кіреді.Кө птеген ө ндірістік процесстер тек қ ана катализаторлардың қ атысуымен жү реді, мс: аммиак, азот жә не кү кірт қ ышқ ылдарының ө ндірісі, синтетикалық каучук ө ндірісі.
Кө птеген қ айтымды экзотермиялық реакцияларда температураның жоғ арылауы тепе-тең дікті кері бағ ытқ а ығ ыстырады, бұ л жағ дайларда катализаторларды қ олдану процесті тө мен температурада жү ргізуге мү мкіндік береді, мысалы аммиак синтезі, кү кірт диоксидінің тотығ уы жә не т.б Кү рделі реакцияларды жү зеге асырудағ ы катализаторлардың рө лі ө те маң ызды, себебі олардың таң даушылық қ асиетінің ә серінен тек қ ана қ ажетті реакцияның жылдамдығ ына ә сер етуге болады.Мс, аммиакты тотық тыру процесінде таң даушылық ә сері бар платиналы катализаторлар қ олданылады, олар тек қ ана негізгі реакцияның (NO газын алу) жылдамдығ ын жоғ арылатып, жанама реакциялардың жылдамдық тарына ә сер етпейді.Катализаторлар органикалық синтезде, мұ най ө ң деу процесстерінде де кең інен қ олданылады.
Катализ -катализаторлардың қ атысуымен химиялық реакцияның жылдамдығ ын жоғ арылату процесі.
Катализаторлар -бастапқ ы реагенттермен аралық қ осылыстар тү зу арқ ылы реакцияғ ы қ атысып, реакцияның механизімін ө згерту арқ ылы активтілік энергияны тө мендетіп, тепе-тең дікке жету жылдамдығ ын жоғ арылатып, процестің соң ында бастапқ ы химиялық қ ұ рамын қ алпына келетін заттар.
дебиет:
1. Ы.Қ.Тойбаев, Қ.А.Жұ банов, Ү.Ә.Садық ов, Ә.Қ.Қ оқ анбаев, Ж.Х.Ташмұ хамбетова Химиялық технологияның ториялық негіздері.
|
|