
Главная страница Случайная страница
Разделы сайта
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Реакции 1-ого порядка
|
|
 А В CH3OCH3® CH4 + H2 + CO
А В CH3OCH3® CH4 + H2 + CO
Кинетическое уравнение реакции первого порядка
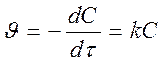 .
.
Разделим переменные и проинтегрируем
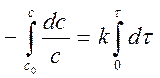
lnC – lnC0 = -kt Þ lnC = lnC0 - kt
С0 – исходная концентрация
С - концентрация в момент времени t
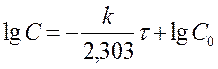
Кинетическая кривая реакций 1-ого порядка
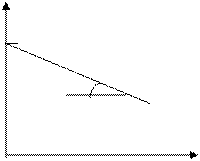 lg C
lg C
lg C o tga = - 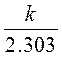
a
t, с
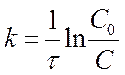 или
или 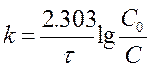 . [ k ] = [с-1]
. [ k ] = [с-1]
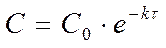 .
.
период полупревращения τ 1/2:
|
C = 0, 5C0 Þ 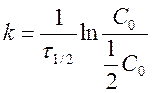
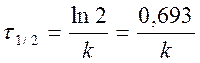 - не зависит от С о
- не зависит от С о
Реакции 2-ого порядка
A + B → продукты или 2А ® продукты
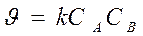
пусть C0 A = C0 B
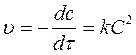
разделим переменные и проинтегрируем:
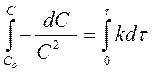
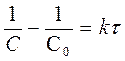
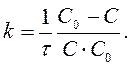 [л× моль-1× с-1]
[л× моль-1× с-1]
Кинетическая кривая реакций 2-ого порядка
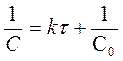
 1/C
1/C
a tga = k
1/C0
t
Период полупревращения для реакций 2-ого порядка
C = ½ C0
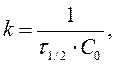
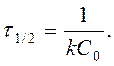
t ½ - обратно пропорционально начальной С0
Реакции 0-ого – порядка: С = С0 - kt; t1/2 = С0 /2k
Реакции 3-его порядка: 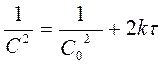 ;
; 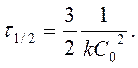
Методы определения порядка реакции
|
|